Clear Sky Science · sv
Hydrerad metallladdningstäthet som en universell beskrivare som förklarar mekanistiska variationer i periodataktivering för nedbrytning av föroreningar
Rensa vatten med smart kemi
Många läkemedel och industrikemikalier passerar konventionella vattenreningsverk och hamnar i floder och dricksvatten. Denna studie undersöker ett lovande sätt att bryta ner sådana svårnedbrytbara föroreningar med hjälp av en vanlig oxiderande reagens, periodat, och visar att en enkel egenskap hos metalljoner i vatten kan förutse hur väl — och hur säkert — denna kemi kommer att fungera. Att förstå denna regel kan hjälpa ingenjörer att utforma renare, effektivare reningssystem för olika typer av verkligt vatten.
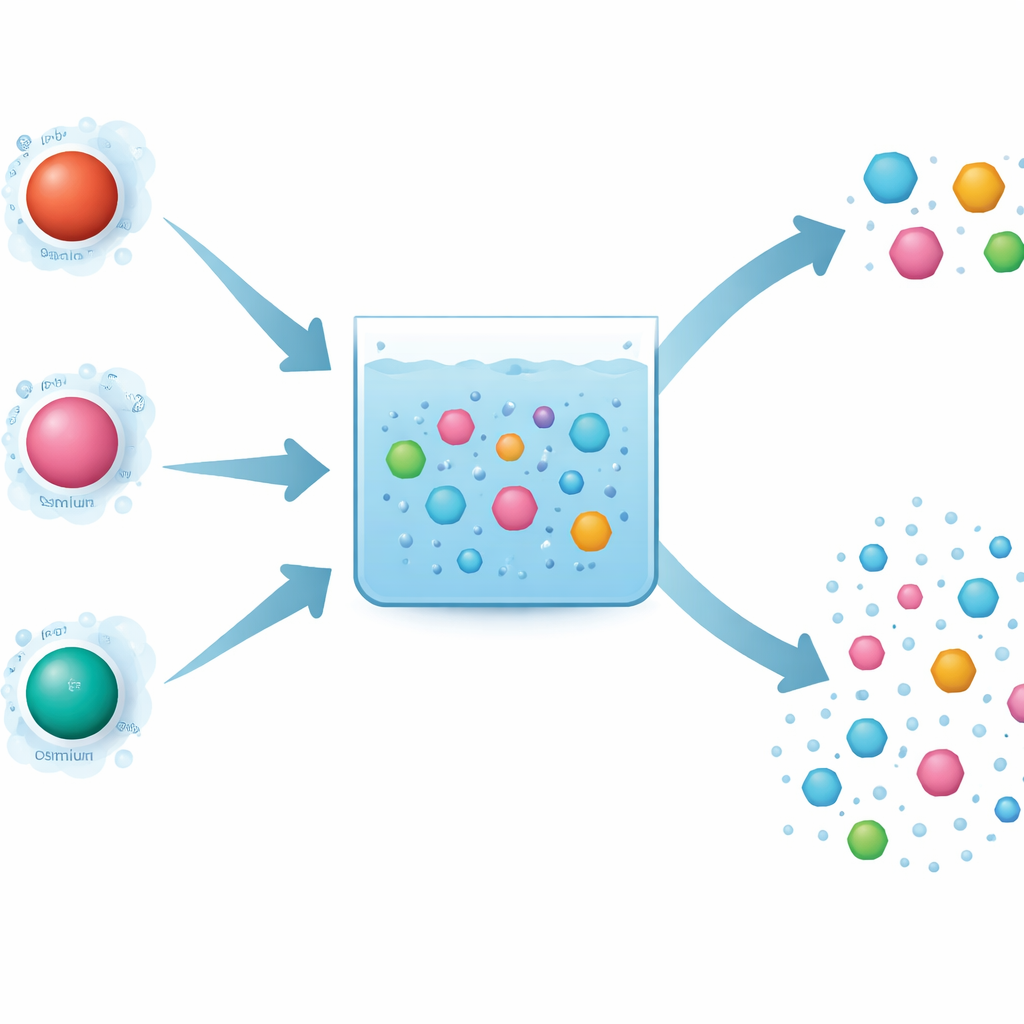
Varför metalvalet spelar roll för nedbrytning av föroreningar
Avancerade oxidationsprocesser använder kraftfulla reaktiva arter för att slita isär organiska molekyler. Periodat är ett sådant oxidationsmedel, och det kan "slås på" av lösta metalljoner. Författarna jämförde tre nära besläktade metaller — järn, rutenium och osmium — som tillhör samma kolumn i det periodiska systemet och som man kanske skulle förvänta sig uppträder lika. Alla tre kan aktivera periodat och hjälpa till att förstöra en testläkemedelsförorening, karbamazepin. Ändå visade experimenten slående skillnader: rutenium fungerade extremt snabbt, järn var långsammare och osmium hamnade däremellan. Ännu mer förbryllande var att osmium avlägsnade en mängd olika föroreningar utan stor preferens, medan järn och rutenium var mer selektiva och attackerade vissa föreningar mycket lättare än andra.
Två mycket olika kemiska vägar
För att ta reda på vad som låg bakom dessa skillnader följde teamet vilka kortlivade oxiderande arter som uppträdde i varje metall–periodatsystem. Med järn och rutenium var de dominerande aktörerna "metall–syre-enheter" som fungerar som precisionverktyg och överför en syreatom direkt till specifika positioner på en förorening. Dessa vägar tenderade att bilda epoxiprodukter — ringsstrukturer som tillför en enstaka syreatom — vilket visar att reaktionen är ganska selektiv. I osmiumsystemet däremot var huvudaktörerna hydroxylradikaler, extremt reaktiva fragment som attackerar nästan vilken närliggande organisk molekyl som helst, vilket leder till hydroxylerade produkter och små ringöppnade fragment. Tester med kemiska prober och spinfångstspektroskopi bekräftade att hydroxylradikaler och närliggande reaktiva syrearter, snarare än högvalenta osmium–syre-enheter, driver större delen av föroreningsnedbrytningen när osmium är närvarande.
Hur vattenförhållanden påverkar reaktionerna
Teamet undersökte också hur pH och naturliga vattenkomponenter påverkar dessa processer. För osmium ökade föroreningsborttagningen när vattnet blev mer alkalisk, där koordinering av extra hydroxidjoner runt metallen gör det lättare för elektroner att röra sig och radikaler att bildas. Vid höga metall‑ eller oxidantdoser "självdämpade" dock osmiumsystemet då de nybildade radikalerna fångades upp av överskott av kemikalier snarare än av föroreningarna. Naturligt organiskt material, som ofta stör oxidationsreaktioner, hade förvånansvärt liten inverkan på osmiumdriven nedbrytning, vilket tyder på att radikalvägen förblir robust i realistiska vatten. Däremot fungerade järn och rutenium bäst i sura förhållanden, och naturligt organiskt material undertryckte starkt deras aktivitet genom att suga upp de viktiga metall–syre-oxidanterna.
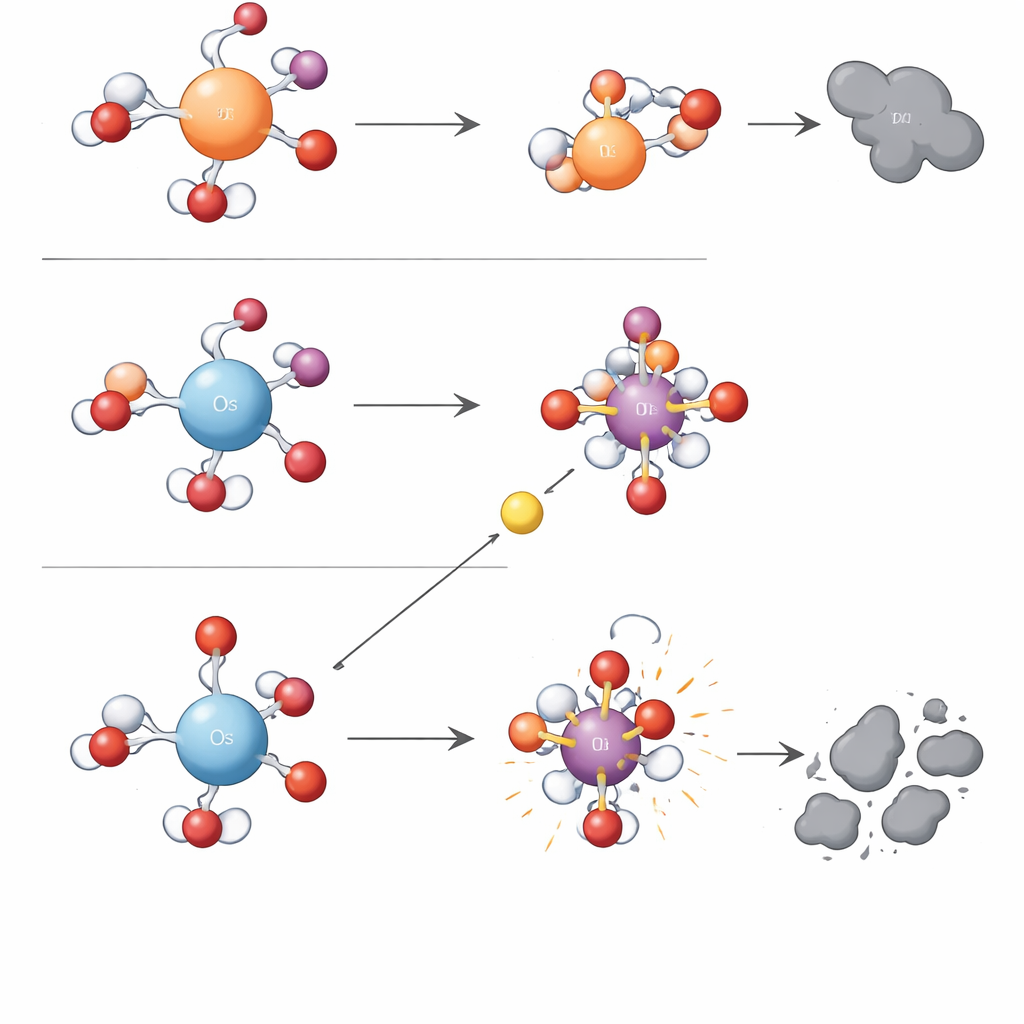
En enkel laddningsregel bakom komplex kemi
För att gå bortom försök‑och‑fel vände sig forskarna till kvantkemiska beräkningar. De fann att en enda elektronisk egenskap — den positiva laddningstätheten hos det hydrerade metallcentret — kunde förklara uppdelningen mellan de två reaktionstyperna. Osmium i vatten bär en högre koncentrerad positiv laddning än järn eller rutenium. Detta starka positiva centrum håller hårt i sin bundna syreatom, vilket gör dess metall–syre-enhet stabil men trög för direkt syreöverföring. Samtidigt sänker den starka dragningen på närliggande vatten och joner energibarriären för enkel‑elektronsteg som i slutändan bryter en syrebinding i periodat och frigör hydroxylradikaler. Metaller med lägre laddningstäthet, som järn och rutenium, håller elektroner mer tätt och gynnar bildning och användning av selektiva metall–syre-oxidanter istället för fria radikaler. Författarna kallar denna organiserande idé för "Charge Density Control Mechanism" och visar att den också rationaliserar trender som rapporterats för andra metaller, som mangan.
Utforma bättre vattenbehandling med en enda ratt
Genom att knyta en svår uppsättning observationer till en enkel beskrivare — laddningstätheten hos en metall omgiven av vatten — erbjuder detta arbete en vägkarta för att skräddarsy avancerade oxidationsprocesser. Metaller med hög laddningstäthet bör gynna bred, radikalbaserad nedbrytning av komplexa föroreningsblandningar, särskilt i alkaliska eller organiskrika vatten. Metaller med lägre laddningstäthet passar bättre när selektiv, mildare oxidation önskas, till exempel för att omvandla specifika kontaminanter utan att överreagera med allt annat som finns närvarande. I praktiska termer innebär detta att kemister och ingenjörer kan skärma eller designa katalysatorer för vattenrening genom att justera hur tätt metallcentra håller laddning i sin vattenomgivning, istället för att optimera varje system genom enbart försök.
Citering: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Nyckelord: avancerade oxidationsprocesser, periodataktivering, vattenbehandling, övergångsmetallkatalys, hydroxylradikaler