Clear Sky Science · sv
Höggenomströmnings kemisk proteomik‑arbetsflöde för att kartlägga protein‑citrullineringens dynamik
Varför förändringar i proteinens byggstenar spelar roll
Våra celler finjusterar ständigt hur proteiner fungerar genom att lägga till små kemiska modifieringar efter att de har producerats. En sådan modifiering, kallad citrullinering, förändrar subtilt laddningen hos en vanlig aminosyra och kan omforma hur proteiner viks, fäster vid DNA eller interagerar med andra molekyler. Dessa små ändringar kopplas i ökande grad till autoimmuna sjukdomar, infektioner, cancer och hjärnfunktion — men de är notoriskt svåra att upptäcka. Denna studie presenterar ett höggenomströmningslaboratoriearbetsflöde som slutligen gör det möjligt att kartlägga citrullinering över tusentals proteiner, och visar när och var det uppstår i vävnader och immunceller.
En dold strömbrytare på proteiner
Citrullinering sker när enzymer som kallas PADs kemiskt modifierar aminosyran arginin och tar bort dess positiva laddning. Den till synes lilla förändringen kan luckra upp hur DNA packas, förändra styvheten i strukturella proteiner eller ändra hur immunförsvaret känner igen kroppens egna vävnader. Onormal citrullinering har kopplats till reumatoid artrit, neurodegenerativa sjukdomar, virusinfektioner och cancer. Citrullinerade proteiner är dock sällsynta och lätt att förväxla med andra, vanligare modifieringar, så standardmetoder inom masspektrometri missar dem ofta. Resultatet har blivit att forskare endast haft en fragmentarisk bild av kroppens ”citrullinom” — den fullständiga uppsättningen citrullinerade proteiner.
En tvåstegs "tagga‑och‑fånga"‑strategi
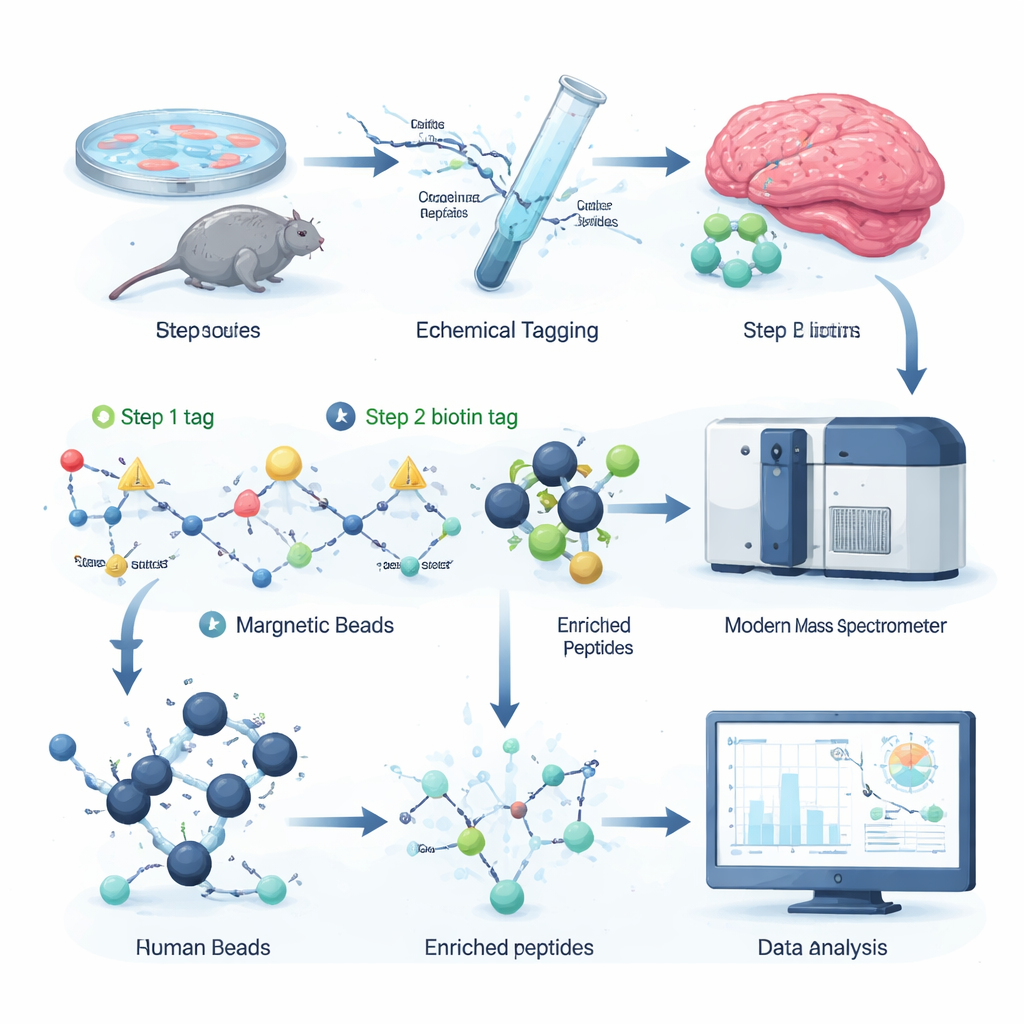
Författarna utvecklade en kemisk märkningsstrategi som selektivt fäster ett avtagbart ”handtag” på citrullinerade platser i peptider, de proteinfragment som analyseras med masspektrometri. I första steget känner en liten reaktiv molekyl igen citrullin och monterar en liten tagg. I andra steget kopplas en större biotintagg på med en klickreaktion, vilket gör att de märkta peptiderna kan fångas ur en komplex blandning med streptavidin‑pärlor, ett vanligt biokemiskt verktyg. En mild kemisk behandling kapar sedan av den skrymmande delen av taggen, vilket lämnar en liten, väldefinierad massförskjutning som masspektrometern lätt kan detektera. Eftersom alla reagenser finns kommersiellt och hela protokollet ryms i 96‑brunnsplattor är arbetsflödet snabbt, skalbart och kompatibelt med befintliga proteomikuppsättningar.
Se mer av citrullinomet
Genom att spika in kända citrullinerade peptider i cellextrakt och systematiskt späda dem visade teamet att deras berikningsstrategi förstärker signalen från citrullinerade peptider mer än tiofalt, även när de utgör mindre än en av tusen molekyler. I komplexa prover ökade både antalet detekterade citrullinerade platser och deras uppmätta intensiteter dramatiskt efter berikning. När metoden tillämpades på mushjärnvävnad upptäcktes två till tre gånger fler distinkta citrullineringsplatser än med en tidigare ledande metod, inklusive många på myelinbasiskt protein som isolerar nervfibrer och på proteiner involverade i synaptisk kommunikation. Detta tyder på att citrullinering kan påverka både hur nervceller signalerar och hur hjärnans kopplingar upprätthålls.
Immunceller som kastar klibbiga protein‑nät
Neutrofiler, en framträdande typ av vita blodkroppar, kan bekämpa inkräktare genom att släppa ut klibbiga nät av DNA och proteiner kallade neutrofilernas extracellulära fällor, eller NETs. NET‑bildning är beroende av PAD4, ett citrullinerande enzym som luckrar upp kromatin så att DNA kan spillas ut. Med sitt nya arbetsflöde följde forskarna hur citrullineringen förändrades i humana neutrofiler exponerade för ökande doser av en kemisk aktivator. De detekterade upp till 1 700 citrullinerade peptidefragment över 580 proteiner, med hundratals platser som ökade eller minskade i dosberoende mönster medan de övergripande proteinnivåerna förblev konstanta. Histoner — proteinerna som paketerar DNA — visade omfattande citrullinering, inte bara vid några få klassiska platser, och varianter av länkhistonen H1 var särskilt modifierade. Strukturella proteiner som aktinregulatorer och lamin B, som formar kärnmembranet, blev också starkt citrullinerade, vilket pekar på en koordinerad mjukning av både kromatin och cellens stomme under NET‑frisättning.
En kärn‑citrullinering‑signatur vid infektion
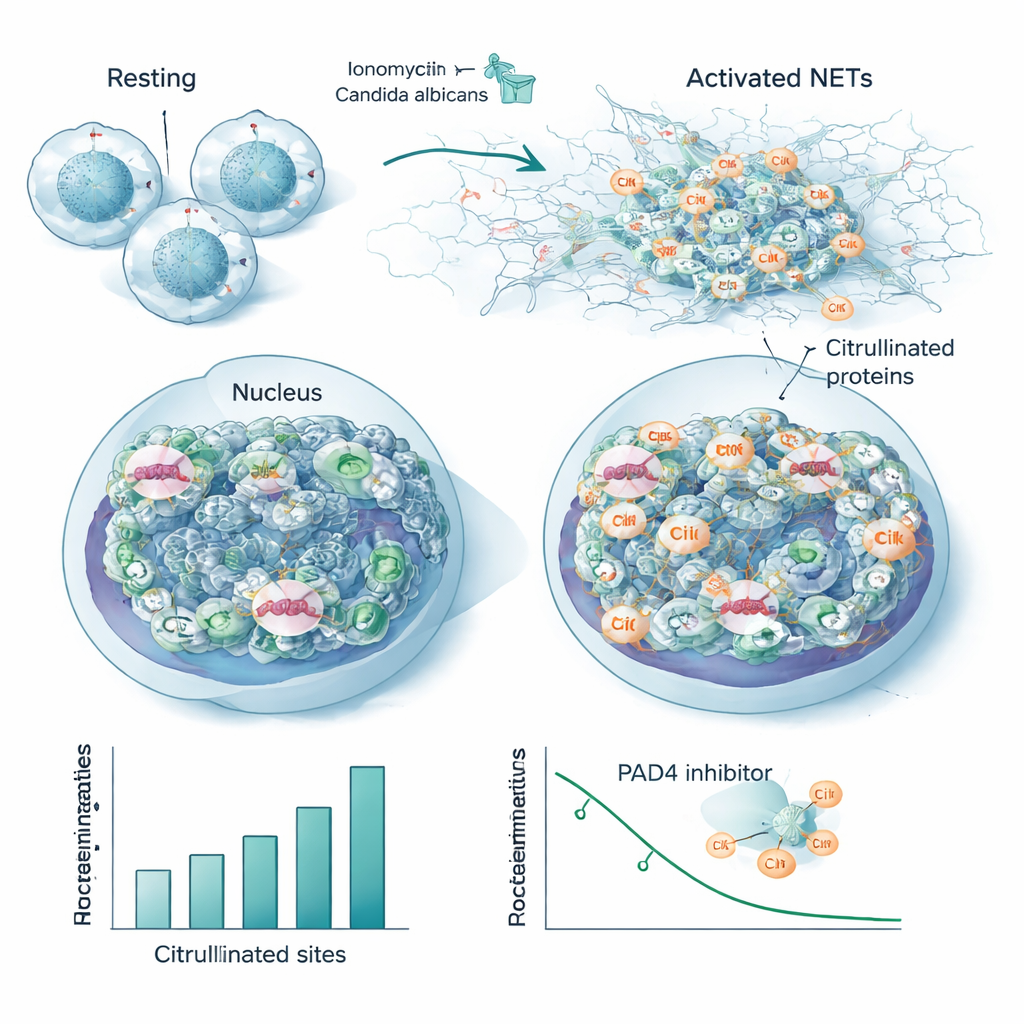
För att efterlikna en verklig infektion stimulerade teamet neutrofiler med värmedödade Candida albicans, en vanlig svamppatogen. Även om detta gav färre modifierade platser totalt än den starka kemiska aktivatorn, överlappade majoriteten av de citrullinerade proteinerna och positionerna mellan de två utlösarna. Denna överlappning definierar ett bevarat ”kärn‑citrullinom” kopplat till NET‑bildning, inklusive många nukleära och cytoskelettala proteiner samt flera kända autoantigen — precis de mål som antikroppar riktar sig mot i autoimmuna sjukdomar. När forskarna tillsatte ett PAD4‑blockerande läkemedel förlorade många av dessa samma platser sin citrullinering i dosberoende grad, vilket direkt knyter dem till enzymets aktivitet och tyder på att de kan fungera som känsliga avläsningar av PAD4‑inhibering.
Vad detta betyder för hälsa och sjukdom
Genom att förvandla en svårfångad modifiering till en mätbar signal gör detta arbetsflöde det möjligt att kartlägga var och när citrullinering sker i vävnader, immunsvar och sjukdomsmodeller. För icke‑specialister är huvudbudskapet att citrullinering fungerar som en subtil molekylär dimmer på proteiner, och att kunna se dess mönster i hög detalj kan hjälpa till att förklara hur autoimmuna sjukdomar uppstår, hur infektioner omformar immunceller och hur hjärnans proteiner förändras över tid. Metodens skalbarhet och beroende av standardlaboratorieutrustning innebär att den kan tas i bruk i stor skala, vilket öppnar dörren för att upptäcka nya läkemedelsmål, precisa diagnostiska verktyg och en djupare förståelse för hur små kemiska ändringar kan få stora biologiska konsekvenser.
Citering: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Nyckelord: citrullinering, autoimmun sjukdom, neutrofilernas extracellulära nätverk, masspektrometri, post‑translationell modifiering