Clear Sky Science · sv
En generell referens definierad av konsensus-toppar för analys av single-cell ATAC-seq-data
Varför det är viktigt att kartlägga DNA:s öppna dörrar
Varje cell i din kropp bär i stort sett samma DNA, ändå beter sig nervceller, blodceller och tumörceller mycket olika. En viktig förklaring är att endast vissa DNA-avsnitt är exponerade och ”öppna” för användning vid en given tidpunkt. Nya single-cell-tekniker kan nu mäta denna öppenhet över hela genomet, men hittills har de saknat en gemensam referenskarta—något som en standardatlas—för att jämföra resultat mellan experiment och laboratorier. Denna studie bygger en sådan karta, kallad cPeaks, och visar hur den kan skärpa vår bild av celltyper, utveckling och cancer.
Att förvandla många experiment till en delad karta
Författarna började med att samla 624 högkvalitativa experiment som mätte öppet kromatin—de åtkomliga delarna av DNA—över mer än 40 mänskliga organ. I varje experiment hade datorprogram redan markerat ”toppar” där DNA:t var särskilt exponerat. Istället för att behandla varje dataset separat lade teamet noggrant ovanpå varandra alla dessa toplistor längs genomet och slog ihop överlappande regioner. De undersökte sedan hur ofta varje liten position inom dessa sammanslagna regioner kallades öppen i de olika experimenten, vilket förvandlade varje region till en karakteristisk form som speglade hur konsekvent den förekom. När en sammanslagen region faktiskt innehöll flera tätt liggande öppna platser delade de upp den i flera enklare enheter. Dessa enheter—omkring 1,4 miljoner totalt—blev de observerade konsensus-topparna, eller cPeaks, ett kandidatreferenskatalog för mänsklig kromatinåtkomst. 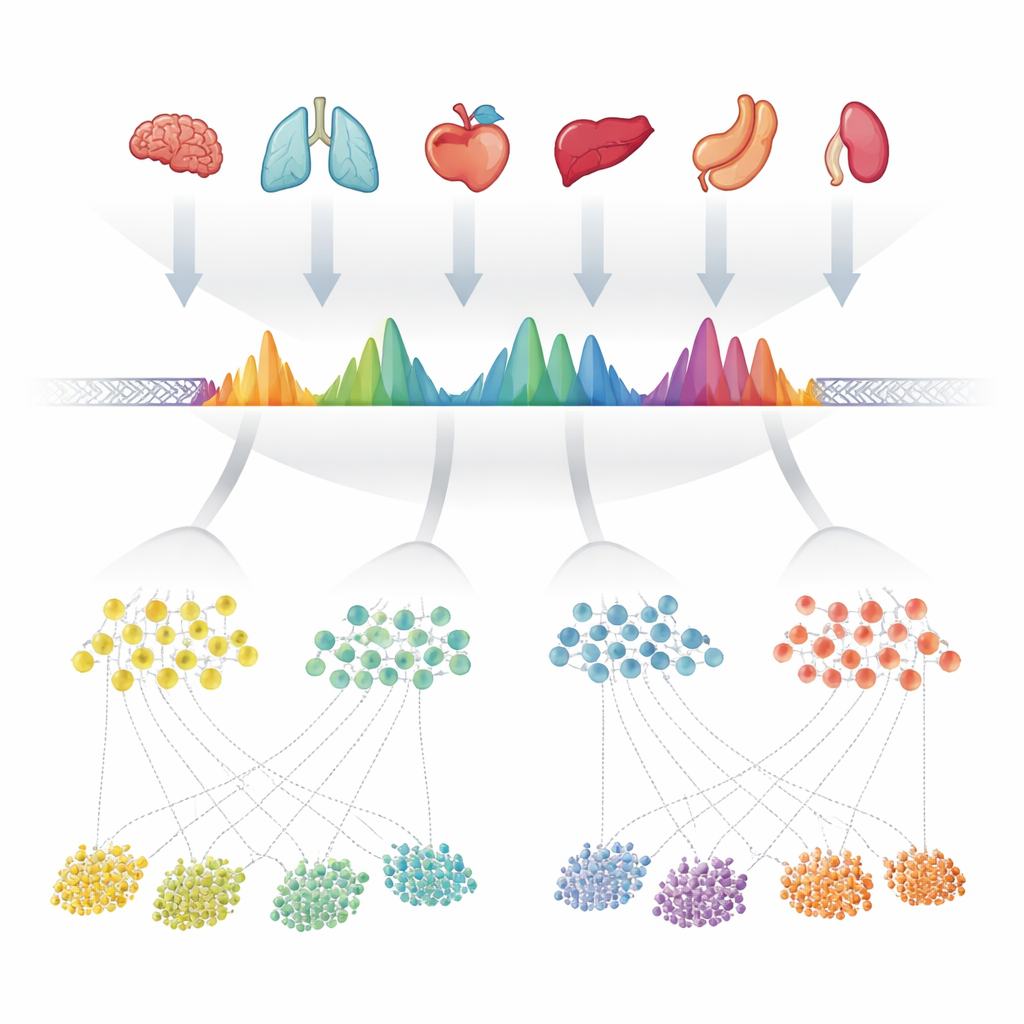
Ett stabilt fingeravtryck över vävnader och tekniker
För att vara en användbar referens måste dessa cPeaks representera genuina, upprepbara kännetecken i genomet, inte egenheter hos enskilda prov eller mjukvara. Författarna testade detta genom att återskapa sina sammanslagna regioner med endast blodprover, endast fasta vävnader, separata publika databaser och till och med olika laborationsmetoder för att undersöka öppet DNA. I varje fall gav samma genomiska lägen förvånansvärt liknande toppformer, och de flesta single-cell-datasets de granskade överlappade mer än 90 % av sina egna toppar med cPeak-katalogen. Avläsningar från många organ samlades exakt runt cPeak-centra, vilket visar att dessa regioner tillförlitligt fångar var kromatin är öppet. Jämfört med tidigare referensuppsättningar baserade på närliggande teknologier täckte cPeaks mer av det åtkomliga DNA som fångas upp av ATAC-seq-experiment, och fångade nästan lika mycket signal som toppar definierade färskt i varje dataset—trots att de är fasta och återanvändbara.
Att lära ett neuralt nätverk att hitta saknade regioner
Även hundratals befintliga prover kan inte täcka alla tänkbara celltyper. För att utvidga sin karta till regioner som ännu inte observerats använde teamet djuplärande. De tränade ett endimensionellt konvolutionellt neuralt nätverk på DNA-sekvenser: exempel inom observerade cPeaks användes som positiva, medan slumpvis valda bakgrundsregioner användes som negativa. Modellen lärde sig att särskilja dessa med hög noggrannhet, vilket antyder att cPeaks bär igenkännbara sekvensmönster. När forskarna avsiktligt gömde toppar specifika för en vävnad i taget återhämtade nätverket dem ändå från sekvensen ensam, inklusive sällsynta, vävnadsspecifika platser. De sköt sedan ett litet fönster över resten av genomet, poängsatte varje segment och lade till omkring 280 000 högpoängande nya regioner i katalogen som predikterade cPeaks, vilket särskilt förbättrade täckningen i vävnader som var underrepresenterade i den ursprungliga datan.
Att koppla öppna regioner till gener, celltyper och sällsynta celler
Med en rikare referens i handen frågade författarna vad dessa regioner gör. Många cPeaks ligger nära geners start- och slutpositioner eller överlappar kända regulatoriska element som promotorer, enhancers och bindningsställen för arkitekturella proteiner som CTCF. En liten undergrupp är åtkomlig i nästan varje dataset; dessa längre ”housekeeping”-cPeaks tenderar att sitta i kärnpromotorregioner för gener som behövs för grundläggande cellunderhåll. Teamet klassificerade också cPeaks efter hur skarpa och konsekventa deras kanter är över prover, vilket speglar hur precist närliggande DNA är paketerat i nukleosomer. Regioner med skarpt definierade gränser är berikade för särskilda familjer av transkriptionsfaktorer som är kända för att omforma kromatin och driva utveckling. När cPeaks användes som features för att analysera flera single-cell-datasets förbättrade de noggrannheten i celltypsetiketteringen, och var särskilt hjälpsamma för att identifiera sällsynta celltyper och subtila undertyper som tidigare toppuppsättningar eller enkla genomiska rutnät ofta suddade ihop.
Att följa utveckling och cancer med ett gemensamt språk
Kraften i en standardreferens blir tydlig när man jämför mycket olika biologiska sammanhang. Med cPeaks omanalysserade författarna single-cell-data från utvecklande mänsklig näthinna, stora atlaser av fostra och vuxna vävnader, och flera cancerformer. De kunde rekonstruera utvecklingstrajektorier och se att andelen skarpt avgränsade, ”väl positionerade” cPeaks tenderar att öka under övergångsstadier, för att sedan sjunka när celler etablerar stabila identiteter. Ett liknande mönster framträdde över tumörstadier: intermediära cancerformer visade en högre andel av dessa strukturerade regioner, vilket antyder intensiv regulatorisk ombyggnad. I en ovarietumör hjälpte cPeaks att avslöja två distinkta cancercellsunderkloner med olika DNA-kopienummerförändringar, vilket visar hur referensen kan exponera dold komplexitet i sjukdom.
Vad detta betyder för framtida genomforskning
För icke-specialister kan cPeaks betraktas som en standardiserad uppsättning koordinater som markerar var genomet mest sannolikt är fysiskt öppet och aktivt över många mänskliga celltyper. Genom att anpassa nya single-cell-kromatinexperiment till denna delade karta kan forskare jämföra resultat mellan studier, lättare upptäcka sällsynta eller övergångsbaserade celltillstånd och börja bygga storskaliga modeller för genreglering—på samma sätt som standardiserade genkataloger möjliggjorde framväxten av single-cell RNA-atlaser. Den nuvarande cPeak-katalogen är ett första utkast som kommer att växa när ny data tillkommer, men den ger redan ett gemensamt språk för att beskriva kromatinåtkomst och för oss närmare en enhetlig bild av hur DNA-packning styr utveckling, hälsa och sjukdom. 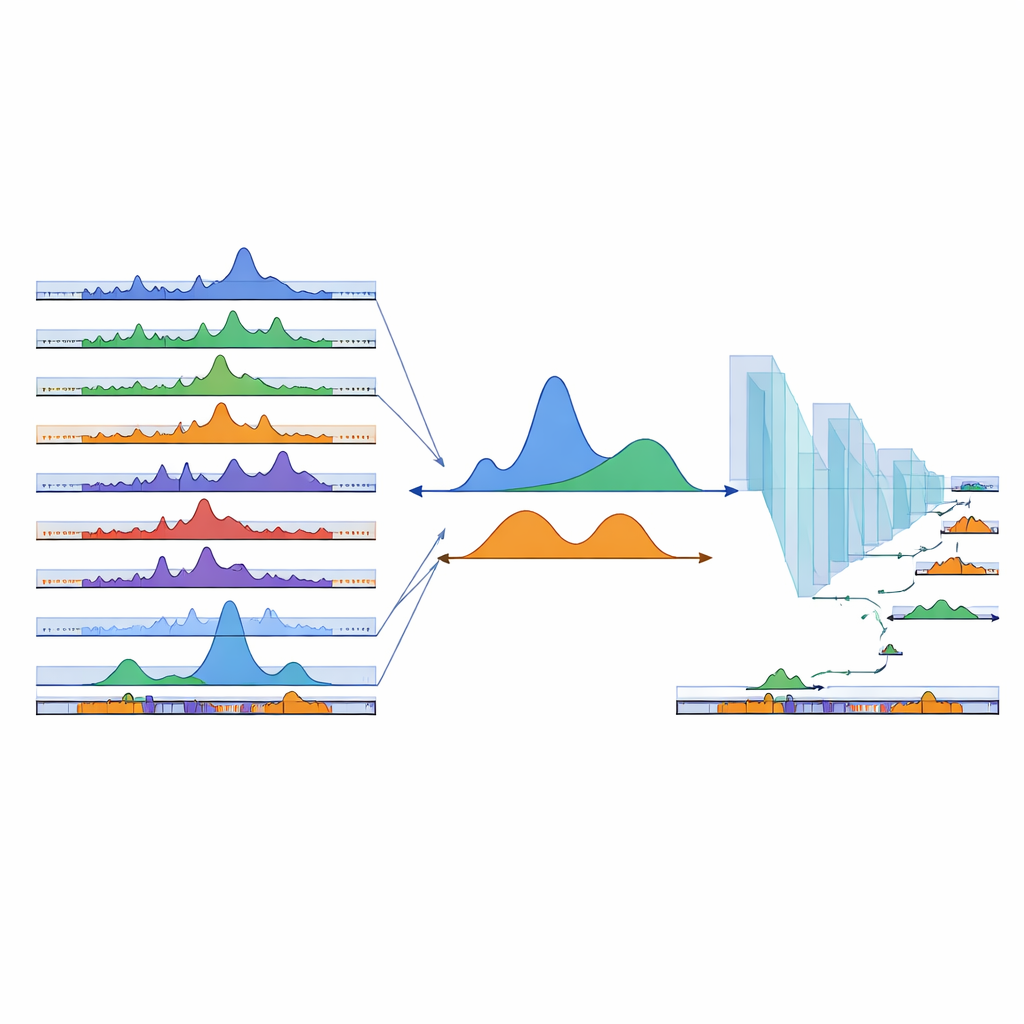
Citering: Meng, Q., Wu, X., Chen, W. et al. A generic reference defined by consensus peaks for single-cell ATAC-seq data analysis. Nat Commun 17, 2522 (2026). https://doi.org/10.1038/s41467-026-69461-6
Nyckelord: kromatinöppning, single-cell ATAC-seq, konsensus-toppar, genreglering, djuplärande i genomik