Clear Sky Science · sv
Trippelriktad stimulering av STING, TGF-β och PD-L1 förstärker CXCL16–CXCR6‑signalering för kraftfull antitumörrespons
Göra kalla tumörer varma
Cancerimmunterapi har förändrat behandlingen för vissa patienter, men många tumörer står fortfarande emot dessa kraftfulla läkemedel. Denna studie undersöker varför vissa cancerformer resistenta mot moderna immunkontrollläkemedel och föreslår en smart, tredelad strategi som väcker kroppens försvar, lockar till sig elitmördande T‑celler och håller dem aktiva inne i tumören.
Varför dagens immunläkemedel inte räcker
De flesta godkända immunterapier riktar in sig på en enskild broms på immunceller, till exempel PD‑1/PD‑L1‑vägen. En nyare klass läkemedel försöker gå längre genom att även blockera TGF‑β, ett molekylärt hinder som kraftigt dämpar immunitet i avancerade cancerformer. Ett sådant läkemedel, YM101, kombinerar TGF‑β‑ och PD‑L1‑blockad i en enda antikropp och visade lovande resultat i möss. Men även i genetiskt identiska djur krympte vissa tumörer knappt alls. Genom att jämföra behandlingskänsliga och resistenta tumörer fann forskarna att framgångsrik behandling gick hand i hand med stark "innat" immunaktivering, särskilt signalering via en väg kallad STING, som känner igen avvikande DNA och utlöser alarmliknande antivirala signaler.
Lägga till en tredje spak: STING‑vägen
Misstänks att svag innat aktivering var den saknade delen kombinerade teamet YM101 med en tablettlik STING‑agonist kallad MSA‑2 i flera mus-tummodeller, inklusive typiskt svårbehandlade "kalla" tumörer. Den tredubbla strategin — STING‑aktivering plus TGF‑β‑ och PD‑L1‑blockad — krympte tumörer mer effektivt, förlängde överlevnad och skyddade ofta mössen från tumörtillväxt vid återutmaning, vilket indikerar långvarigt immunminne. Detta överträffade den mer konventionella kombinationen av STING‑agonist och PD‑L1‑blockad ensam, och förstärkte till och med STING‑agonistterapin när endast TGF‑β blockerades, vilket visar att TGF‑β i sig fungerar som en stor broms på STING‑driven immunitet. 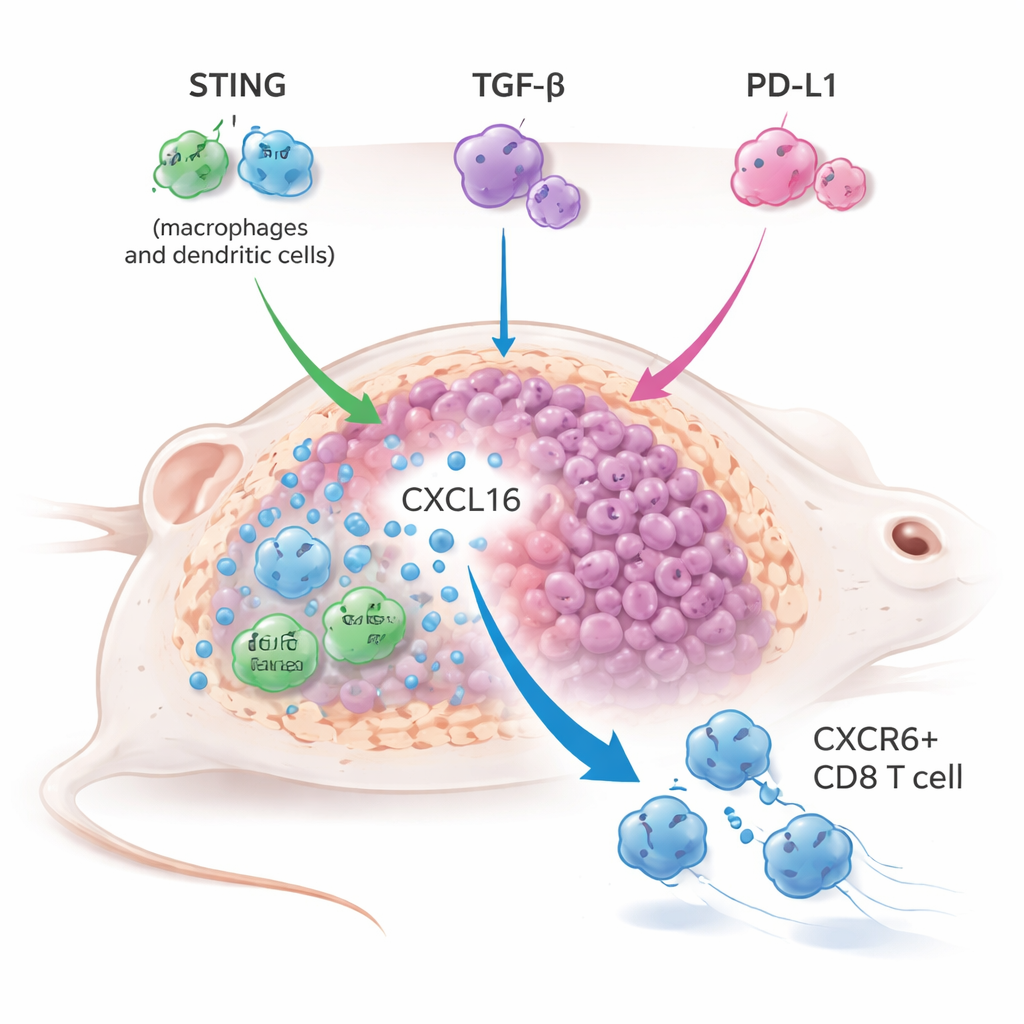
Rekrytera ett specialistmördarlag
För att förstå hur denna tredubbla strategi fungerade använde forskarna single‑cell RNA‑sekvensering och detaljerad immunprofilering av behandlade tumörer. De upptäckte en påtaglig expansion av en särskild mördande T‑cellssubtyp markerad av receptorn CXCR6. Dessa CXCR6+ CD8‑T‑celler var väl beväpnade, uttryckte höga nivåer av granzym, perforin och inflammatoriska molekyler, och visade starka tecken på aktivering och proliferation. Samtidigt ökade tumörassocierade makrofager och dendritiska celler produktionen av en kemokin kallad CXCL16, som binder CXCR6 och hjälper till att behålla dessa T‑celler i tumören. När CXCL16–CXCR6‑länken bröts — antingen genom blockad av CXCL16 eller genom genetisk borttagning av CXCR6 i T‑celler — förlorade den kombinerade behandlingen till stor del sin antitumöreffekt, vilket bevisar att denna axel är central för terapiens framgång.
Hur signal‑kaskaden slås på
Närmare undersökning visade hur STING‑aktivering och TGF‑β‑blockad gemensamt ökar CXCL16. I mänskliga och musimmunceller ökade STING‑agonister starkt CXCL16 och den antivirala cytokinen IFN‑β, medan tillsatt TGF‑β skarpt minskade båda. Forskarna visade att STING utlöser IFN‑I‑signalering, vilket aktiverar transkriptionsfaktorn STAT1; STAT1 binder sedan direkt till kontrollregionen för CXCL16‑genen och slår på den. TGF‑β stör denna kedja genom att påverka ett nyckelsteg i STING‑signaleringen, troligen via ett protein kallat HDAC4 och reaktiva syreföreningar, vilket dämpar IRF3‑aktivering och därmed minskar IFN‑β‑ och CXCL16‑produktion. Genom att blockera TGF‑β tas denna broms bort, vilket tillåter STING‑agonister att fullt ut tända STAT1–CXCL16‑vägen i myeloida celler och därigenom förse CXCR6+ T‑celler med de signaler som behövs för att stanna kvar och bekämpa tumören.
Bygga ett enda precist läkemedel
För att göra detta komplexa regimen mer praktisk och tumörfokuserad konstruerade forskarna en enda "immunstimulerande antikroppskonjugat" kallad Y101S. Denna molekyl kombinerar den dubbla TGF‑β/PD‑L1‑blockerande antikroppen med en STING‑agonist fäst via en klyvbar länk. Y101S riktar sig till PD‑L1‑positiva myeloida celler i tumören, tas upp och frigör sedan STING‑läkemedlet inuti dessa celler. I flera muscancerformer matchade eller överträffade Y101S effekten av att ge YM101 plus en högdos fri STING‑agonist, trots att den bar bara en liten bråkdel av den STING‑dosen. Den ökade antalet CXCL16+ makrofager och dendritiska celler, expanderade CXCR6+ CD8‑T‑celler, inducerade hållbart immunminne och koncentrerade inflammatoriska signaler i tumörer samtidigt som friska organ skonsades, med en gynnsam säkerhetsprofil i möss. 
Vad detta betyder för framtida cancerbehandling
För icke‑specialister är huvudbudskapet att angripa cancer med bara en eller två immunswitchar kanske inte räcker — särskilt när tumörer aktivt tystar tidiga larmsystem. Detta arbete visar att kombination av STING‑aktivering med blockad av TGF‑β och PD‑L1 kan omskola tumörmiljön, kraftfullt attrahera och upprätthålla en specialiserad grupp mördande T‑celler och uppnå djupare, mer bestående svar i prekliniska modeller. Den tredubbla riktade antikropp–läkemedelskandidaten Y101S förkroppsligar denna strategi i ett enda, riktat läkemedel och erbjuder en färdplan för nästa generations immunterapier riktade mot tumörer som idag är resistenta mot standardens kontrollpunktläkemedel.
Citering: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Nyckelord: cancerimmunterapi, STING‑väg, TGF‑beta‑blockad, PD‑L1‑antikropp, CXCL16 CXCR6 T‑celler