Clear Sky Science · sv
En makrofag‑inducerad subpopulation av mesenkymala celler som uttrycker Fcer1g bidrar till skademedierad fibros
Varför vissa sår lämnar bestående ärr
De flesta av oss bär märken efter skärsår, operationer eller olyckor, men varför vissa sår läker smidigt medan andra lämnar tjocka, upphöjda ärr har länge varit ett mysterium. Den här studien tar sig an frågan genom att zooma in på de celler som bygger upp skadad hud. Forskarna avslöjar en tidigare oigenkänd grupp ärrbildande celler som aktiveras tidigt efter skada, under inflytande av immunceller kallade makrofager. Att förstå detta dolda samspel kan peka mot behandlingar som låter huden läka med mindre ärrbildning samtidigt som såret sluts effektivt. 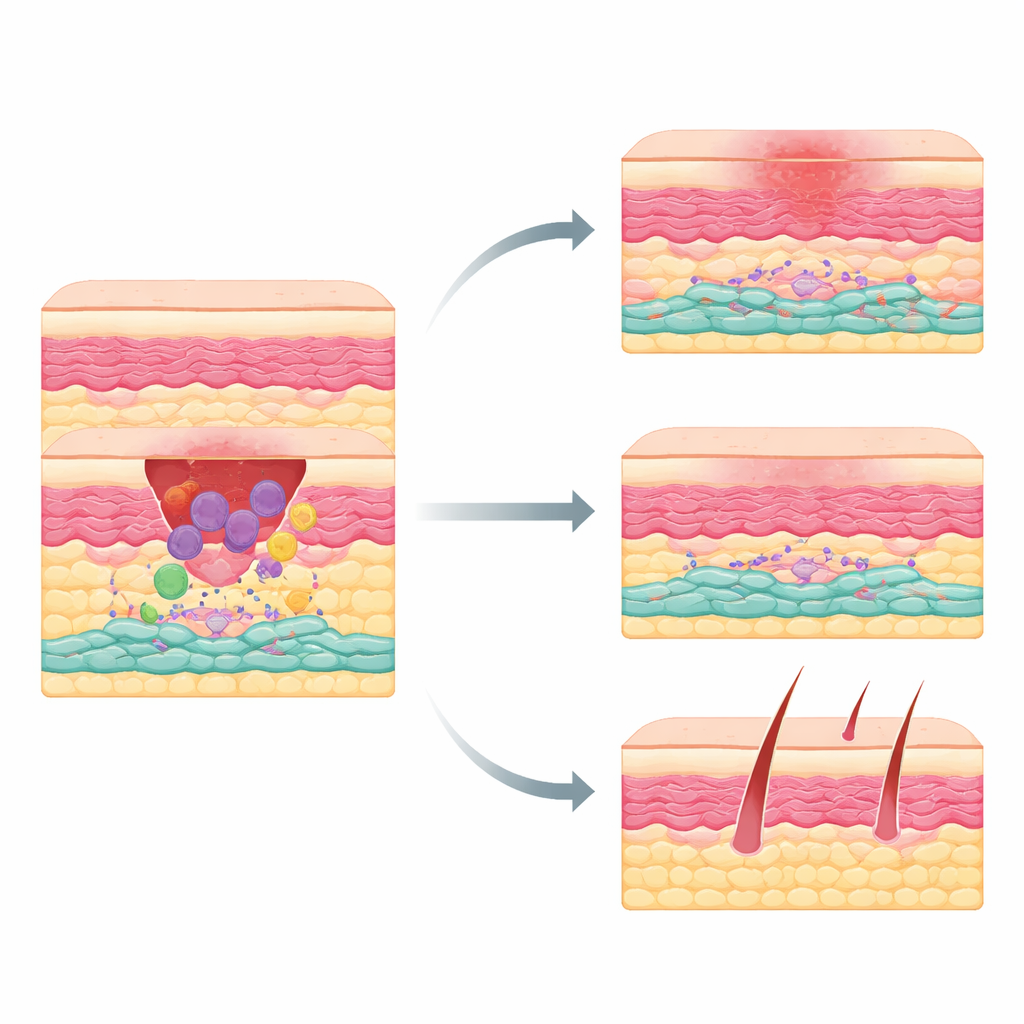
De dolda aktörerna i läkande hud
När huden skadas rör sig kroppen genom en koreograferad sekvens: först inflammation för att städa upp skadan, sedan vävnadstillväxt och slutligen ombyggnad. Makrofager anländer tidigt för att avlägsna skräp och sända kemiska signaler som samlar andra celler. Bland de svarande finns mesenkymala celler—fibroblastlika byggare som lägger ner kollagen och annat stödmaterial. Dessa byggare är inte alla likadana: vissa främjar regeneration medan andra tenderar att överproducera ärrvävnad. Fram till nu hade forskare inte klart identifierat vilka mesenkymala celler i vuxen hud som stod för tjocka ärr.
Immunceller som tyst förbereder scenen för ärrbildning
För att undersöka hur makrofager påverkar ärrbildning använde teamet möss där makrofager kan tas bort selektivt under de första dagarna efter sårbildning. När dessa tidiga makrofager avlägsnades stängdes såren fortfarande, men bildade mycket mindre ärr med mindre tät kollagen. Enkelcells‑RNA‑sekvensering—ett sätt att profilera genaktivitet cell för cell—visade att de flesta mesenkymala undergrupper var oförändrade vid makrofagförlust. Ett undantag stack ut: en tydlig subset av PDGFRα‑positiva mesenkymala celler som slog på genen Fcer1g. Denna subset försvann nästan när makrofagerna saknades, vilket tyder på att makrofager krävs för att skapa eller bibehålla dessa celler.
En snabbväxande, ärrdrivande cellpopulation
Ytterligare experiment kartlade var och när dessa Fcer1g‑positiva mesenkymala celler dyker upp. I oskadad hud var de sällsynta, men efter skada expanderade de snabbt, först runt sårkanterna och sedan koncentrerade i sårbädden, där de utgjorde majoriteten av PDGFRα‑positiva celler vid dag sju. Dessa celler delade sig snabbare än andra mesenkymala celler och visade låg migration, vilket tyder på att lokal proliferation driver deras ökning. När forskarna använde ett smart genetiskt system för att selektivt eliminera celler som uttryckte både PDGFRα och Fcer1g, fortskred sårläkningen normalt—men ärren krympte med mer än 20 procent, kollageninnehållet sjönk med omkring 30 procent, och den reparerade hudens kollagennätverk liknade mer oskadad hud. Hårfolliklar var vanligare i dessa avlägsnade sår, vilket antyder en mer regenerativ läkning. 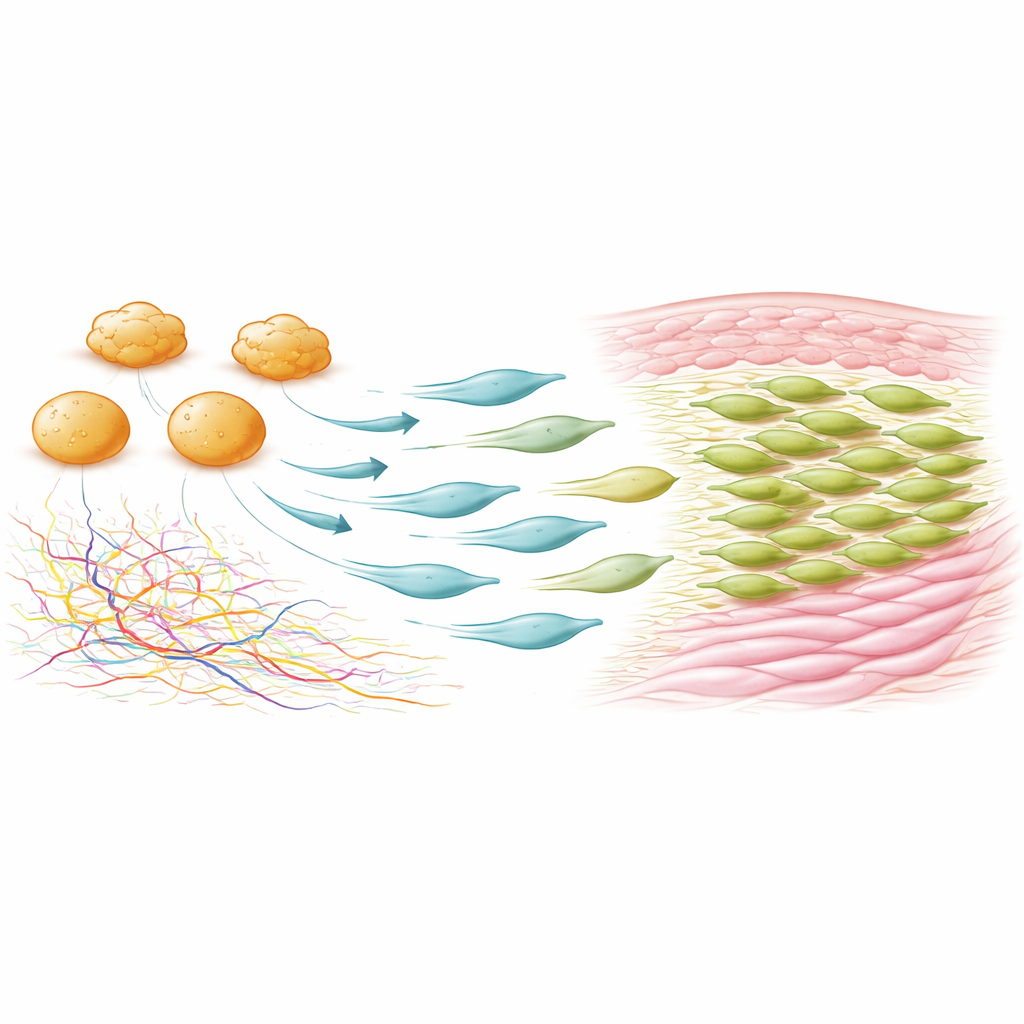
Hur makrofager signalerar till byggarna att överärrbilda
För att förstå hur makrofager utlöser detta ärrbenägna tillstånd analyserade teamet sannolika kommunikationsvägar mellan celltyper. En ledande kandidat var fibronectin, ett klibbigt protein som ingår i den temporära matrisen i färska sår. Makrofager i tidiga sår var en viktig källa till fibronectin, och nivåerna sjönk kraftigt när makrofager togs bort. I möss designade att sakna en sårassocierad form av fibronectin (EDA‑formen) minskade Fcer1g‑positiva mesenkymala celler kraftigt och ärren var lindrigare. I kultur räckte direktkontakt med makrofager för att omvandla vanliga dermala fibroblaster till Fcer1g‑positiva, PDGFRα‑positiva celler, vilket understryker att makrofager kan inducera detta tillstånd direkt.
Ett delat ärrprogram hos möss och människor
För att se om denna celltyp spelar roll hos människor granskade forskarna befintliga human‑data för hudsår på enkelcells‑ och helvävnadsnivå. De fann en motsvarande mesenkymal undergrupp i mänskliga sår som uttryckte FCER1G och ett liknande genmönster, med en topp ungefär en vecka efter skada—samma tidpunkt som i möss. Över mer än hundra mänskliga prov som inkluderade normal hud, akuta sår, kroniska sår och upphöjda ärr separerade FCER1G‑kopplade genprogram tydligt skadad och ärrad vävnad från oskadad hud och var starkast tidigt efter sårbildning. Denna tvärarts‑likhet antyder att det nydefinierade celltillståndet är en evolutionärt bevarad drivkraft för fibrotisk reparation.
Mot mjukare läkning med färre ärr
Tillsammans avslöjar resultaten en tidigare underskattad händelsekedja: tidigt anländande makrofager berikar fibronectin i såret, fibronectin hjälper till att omvandla lokala mesenkymala celler till ett snabbt delande FCER1G‑positivt tillstånd, och denna specialiserade subset avsätter sedan överskott av kollagen som blir ärrvävnad. Eftersom borttagning av dessa celler hos möss minskade ärrbildning utan att sakta ner sårslutningen, utgör de ett tilltalande mål för framtida terapier. Läkemedel eller biologiska medel som stör signalerna som skapar eller upprätthåller detta celltillstånd—kanske genom att modulera makrofagers beteende eller fibronectin‑miljön—skulle en dag kunna hjälpa patienter att läka hudskador med minimala, mindre synliga ärr.
Citering: Ma, X., Wang, E., Puviindran, V. et al. A macrophage-induced subpopulation of mesenchymal cells expressing Fcer1g contributes to wound-induced fibrosis. Nat Commun 17, 2686 (2026). https://doi.org/10.1038/s41467-026-69449-2
Nyckelord: sårläkning, hudfibros, makrofager, fibroblaster, ärrbildning