Clear Sky Science · sv
Positiv kooperativitet mellan RAS-bindande och cysteinrika domäner reglerar RAF:s membranbindningskinetik via lateral återbindning
Varför denna lilla molekylära dans spelar roll
Inuti våra celler fattas livsavgörande beslut om tillväxt, delning och överlevnad ofta vid ytan av cellmembranet. En nyckelaktör i dessa beslut är ett protein som heter RAF, som hjälper till att vidarebefordra tillväxtsignaler och ofta är felkopplat vid cancer. Denna studie avslöjar, med enastående kinetisk detalj, hur RAF hakar i cellmembranet, hur länge det stannar där och varför täta ansamlingar av ett annat protein, RAS, kan hålla RAF aktivt längre än väntat.
Signaler som möts vid cellytan
RAF verkar i en huvudled för signalering känd som MAPK-vägen, som kopplar yttre signaler såsom tillväxtfaktorer till förändringar i genaktivitet. I sitt vilande tillstånd flyter RAF i cellens inre i en veckad, självhämmad form. Det aktiveras först när det möter RAS, en liten molekylär strömbrytare förankrad i den inre ytan av cellmembranet. RAS måste vara i sitt “på”-tillstånd och inbäddad i rätt typ av lipider för att RAF ska rekryteras och aktiveras. Eftersom RAF-molekyler är relativt få jämfört med många andra signaleringskomponenter påverkar exakt hur de engagerar membranet och undviker för tidig frisättning starkt om en cell kommer att svara svagt eller kraftigt på en tillväxtsignal.
Två händer för att greppa membranet
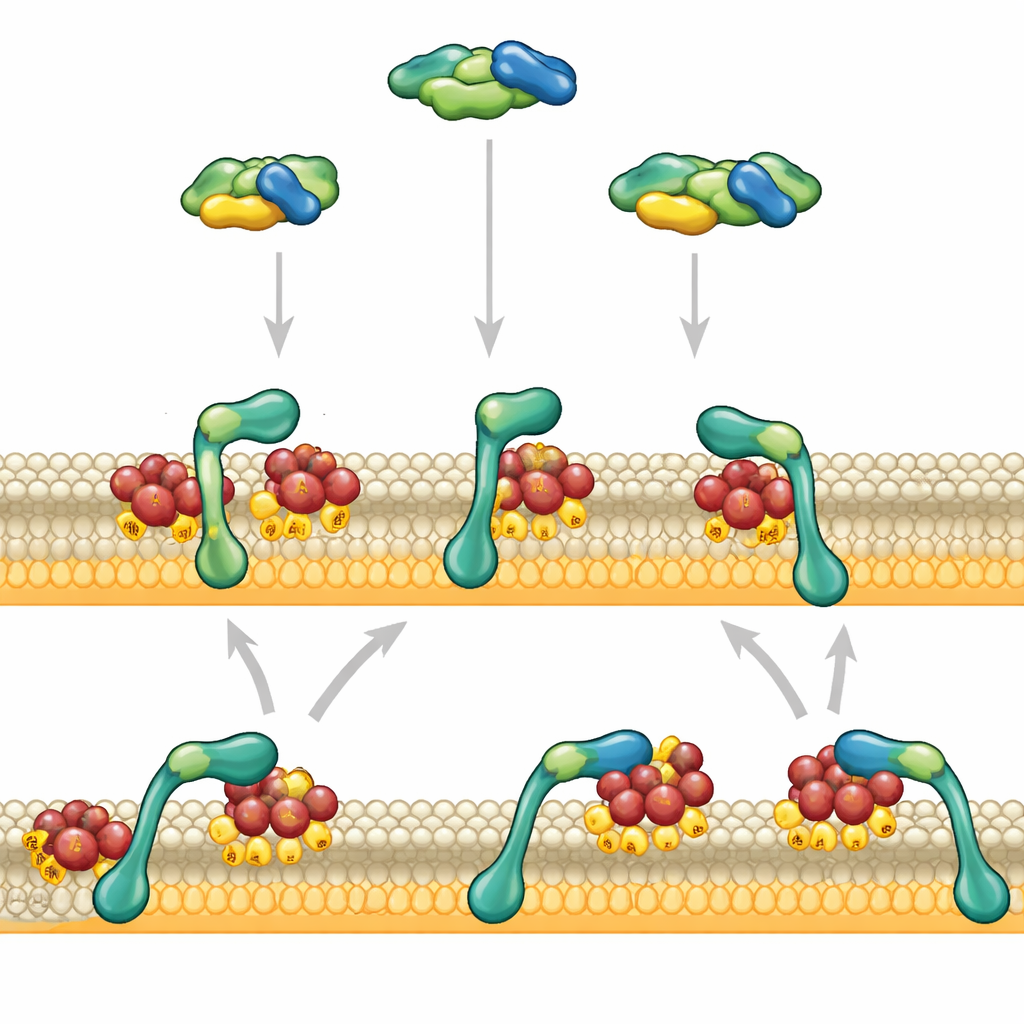
Författarna fokuserade på två regioner i RAF:s främre ände: en som greppar RAS och en som föredrar negativt laddade membranlipider. Med hjälp av konstgjorda membran och renade proteiner iakttog de individuella RAF-fragment som bundit till RAS-dekorerade ytor med avancerad mikroskopi. När den RAS-bindande regionen agerade ensam, vidrörde den membranet kort och släppte efter ungefär en sekund. Lipidälskande regionen, ensam, fäste knappt alls. Men när dessa två regioner var länkade ihop uppträdde de mycket annorlunda: RAF fäste nu starkt och dröjde kvar på membranet i tiotals sekunder, särskilt när membranet bar många negativt laddade lipider liknande dem i verkliga celler.
Samverkan som saktar upp avgången
Denna dramatiska förändring uppstod inte för att RAF hittade membranet snabbare, utan för att det lämnade det långsammare. Först känner RAF:s RAS-bindande segment igen aktiverat RAS och dockar RAF vid membranet. Först efter denna första handskakning engagerar den lipidbindande regionen fullt ut de omgivande lipiderna, vilket saktar RAF:s sidledsrörelse och förankrar det mer bestämt. Denna andra kontakt stabiliserar i sin tur den ursprungliga RAS–RAF-interaktionen och skapar en positiv återkopplingsslinga mellan protein–protein- och protein–lipidkontakter. Experiment där den korta länken som förbinder de två regionerna ändrades visade att deras täta rumsliga samordning är avgörande: att göra länken mer flexibel eller längre försvagade RAF:s förmåga att stanna kvar på membranet.
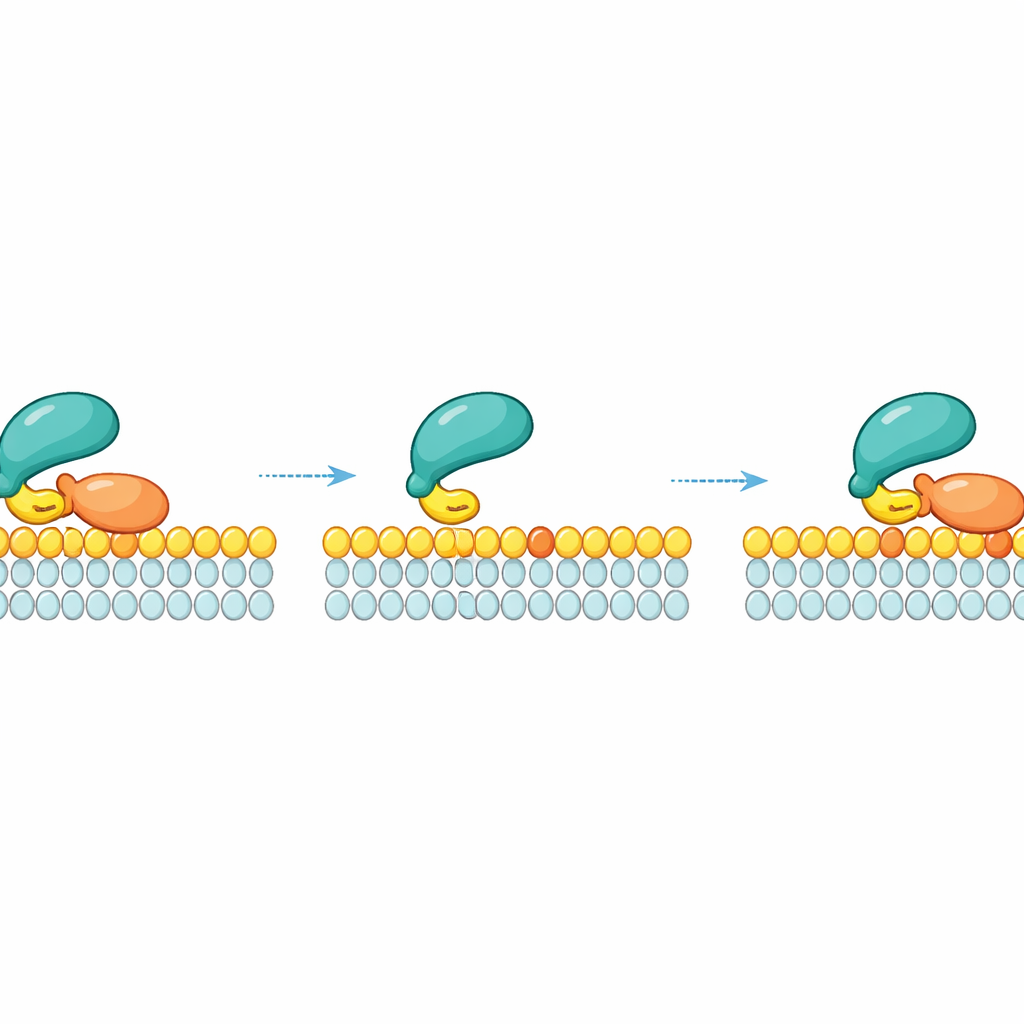
Lateral återbindning: glida istället för att falla av
En viktig insikt i arbetet är att RAF inte helt enkelt lossnar ut i omgivande vätska när det släpper taget om en viss RAS-molekyl. Istället kan RAF, efter att RAS släppt, förbli kortvarigt förankrat vid membranet genom sin svaga lipidkontakt och glida sidledes. Medan det befinner sig i detta övergående tillstånd kan det ”greppa om” en närliggande RAS-molekyl på samma membranfläck. Denna laterala återbindning skapar ett kinetiskt säkerhetsnät: vid hög lokal RAS-densitet—såsom i nanokluster där RAS-molekyler packas tätt—har RAF många chanser att återengagera RAS innan det driver bort. Mätningar och simuleringar visade att ju högre densiteten av aktiverat RAS på membranet är, desto längre förblir RAF membranbundet på grund av dessa upprepade lokala återfästan.
Från förlängda besök till pålitlig aktivering
Den förlängda tid som RAF spenderar på membranet har viktiga konsekvenser. RAF-aktivering är inte en enstaka händelse utan en flerstegssekvens som innefattar formförändringar, borttagning av hämmande taggar och parning av två RAF-molekyler till en aktiv dimer. Studien antyder att endast de RAF-molekyler som vistas på membranet tillräckligt länge kan slutföra denna sekvens, en form av ”kinetisk korrektur” som hjälper celler att undvika oavsiktlig aktivering från flyktiga, svaga signaler. Genom att belysa hur samspelet mellan RAS-bindning, lipidengagemang och lateral återbindning bestämmer RAF:s membranvistelse tid skisserar arbetet en allmän strategi som celler kan använda för att med många små, svaga interaktioner på membran finjustera kraftfulla signalvägar.
Citering: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Nyckelord: RAS, RAF-kinas, cellsignalering vid cellmembran, lateral återbindning, kinetisk korrektur