Clear Sky Science · sv
Sekvensering av DNA-metylering och hydroksymetylering vid samtidigt förekommande kromatinfunktioner
Läsa cellernas kemiska anteckningar
Varje cell i kroppen bär på samma DNA, ändå beter sig nervceller, hudceller och stamceller mycket olika. En förklaring är att celler skriver kemiska ”anteckningar” på DNA och dess paketeringsproteiner, vilket hjälper till att slå gener på eller av. Hittills har forskare haft svårt att läsa flera av dessa anteckningar samtidigt på samma DNA-sträcka, vilket lämnat ett tomrum i vår förståelse för hur de samarbetar. Denna studie presenterar ett nytt sätt att läsa både den genetiska koden och viktiga kemiska markeringar på en gång, och visar hur de samverkar för att kontrollera viktiga DNA-brytare kallade enhancers.
Varför DNA behöver blyertsmärken
DNA verkar inte ensam. Det är lindat runt proteiner som kallas histoner för att bilda kromatin, och både DNA och histoner kan prydas med små kemiska grupper. Två viktiga märkningar på DNA är metyl- och hydroksymetylgrupper som fästs på bokstaven C (cytosin). Dessa märkningar påverkar hur tätt DNA är packat och om närliggande gener är aktiva. I stora drag förknippas metylmärken ofta med genavstängning, medan hydroksymetylmärken tenderar att förekomma där gener är aktiva. Men effekten av dessa märken beror på deras lokala omgivning: exakt var de sitter i genomet och vilka histonmärken de ligger intill.
Problemet med separata kartor
Existerande sekvenseringsmetoder kan kartlägga metyl- och hydroksymetylmärken över hela genomet, och andra metoder kartlägger histonmärken som signalerar aktiva eller tysta regioner. Dessa görs dock vanligtvis i separata experiment och jämförs sedan i datorn. Det berättar vilka funktioner som tenderar att ligga i samma område, men inte om de verkligen samexisterar på just samma DNA-bit i en enskild cell. Äldre försök att kombinera dessa mätningar förlitade sig på hård kemisk behandling som skadar DNA och—avgörande—inte pålitligt kunde skilja metyl från hydroksymetyl i samma läsning. Som följd saknade forskare en klar, molekylär bild av hur kombinationer av märkningar samverkar.
En ny metod för flerskiktsläsning
Författarna utvecklade en metod kallad 6-base-CUT&Tag som kan läsa alla fyra DNA-bokstäver plus två kemiska tillstånd av cytosin—plain, metylerad och hydroksymetylerad—på DNA-fragment som är fysiskt bundna till valda kromatinfunktioner. Först använder de antikroppar som molekylära krokar för att fånga upp DNA som är lindat runt histoner med en specifik märkning, till exempel en markör för aktivt kromatin. Ett ingenjörsmodifierat enzym fäster sedan särskilda adaptrar och förvandlar varje fångat DNA-fragment till en liten slinga som överlever rengöringssteg som förstör lösa bitar. En förfinad kemisk och enzymatisk process omvandlar därefter cytosintillstånden till distinkta sekvenssignaler som moderna sekvenserare kan läsa. På så vis rapporterar en enda läsning var fragmentet kom ifrån, vilken histonmärkning det bar och vilka cytosiner på det som var metylerade eller hydroksymetylerade.
Zooma in på genbrytare
Med mus-embryonala stamceller som fallstudie tillämpade teamet 6-base-CUT&Tag på flera nyckelhistonmärken som etiketterar olika typer av regulatoriskt DNA. De fokuserade på enhancers—DNA-sträckor som fungerar som brytare för att kontrollera när och var gener slås på. Enhancers kan befinna sig i ”aktiva”, ”primade” eller ”beredda” tillstånd, åtskilda av särskilda histonmärken. Forskarna fann att enhancers märkta endast med ett histonmärke kallat H3K4me1 (ofta betraktat som ”primat”) bar de högsta nivåerna av både metylering och hydroksymetylering på DNA, särskilt när man undersökte direkt vid H3K4me1-bundna nukleosomer. Däremot bar enhancers med ytterligare tecken på stark aktivitet eller repression mindre av dessa DNA-märkningar eller visade en förskjutning mot hydroksymetylering, vilket an antydan om pågående utradering av metylmärken.
Avkoda enhancer-tillstånd med större detalj
Eftersom alla enhancer-typer delar H3K4me1-märket frågade teamet om det detaljerade mönstret av DNA-märkningar specifikt vid H3K4me1-märkt DNA i sig kunde skilja enhancer-tillstånden åt. De tränade en maskininlärningsmodell med 6-base-CUT&Tag-data för att klassificera enhancers som aktiva, primade eller beredda, enbart baserat på hur mycket metyl och hydroksymetyl de bar vid den enda histonfunktionen. Denna modell överträffade en i övrigt identisk modell tränad på standarddata över hela genomet som inte är begränsad till något histonmärke. Med andra ord ger läsning av DNA-märken i den omedelbara kontext där de uppträder en skarpare bild än att ta ett genomsnitt över allt DNA i cellen.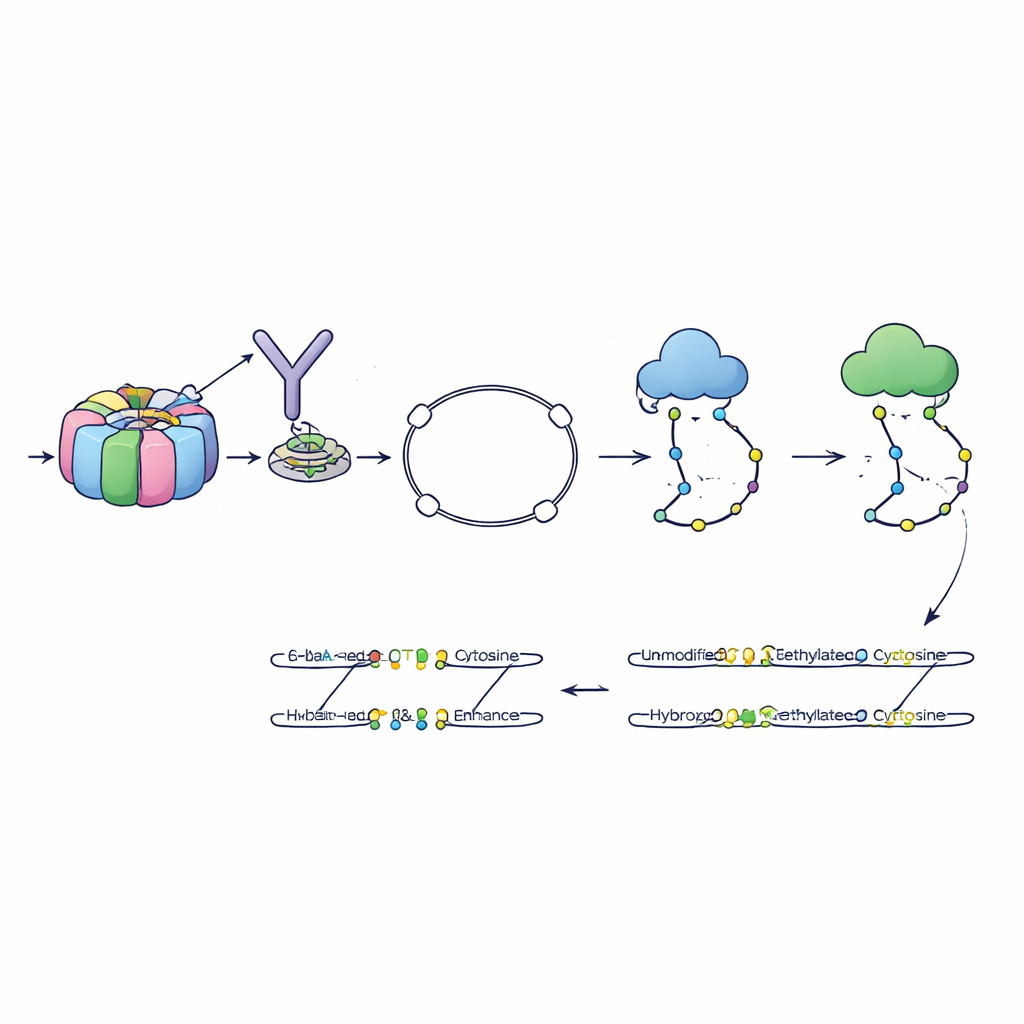
Vad detta betyder för förståelsen av cellidentitet
För en icke-specialist är huvudbudskapet att denna metod låter forskare läsa flera informationslager—DNA-sekvens, DNA-märkningar och histonmärken—på samma molekyl. Denna finmaskiga vy visar hur särskilda kombinationer av kemiska etiketter definierar beredskapen hos genbrytare i stamceller. Eftersom 6-base-CUT&Tag är mer effektivt och mindre skadligt än äldre tillvägagångssätt kan det avslöja subtila mönster som tidigare låg dolda. Med tiden kan denna flerskiktsläsning av kromatin hjälpa till att förklara hur celler minns sin identitet, hur de förändras under utveckling eller sjukdom, och hur vi mer precist kan rikta in den regulatoriska koden i terapier.
Citering: Araujo Tavares, R.d.C., Dhir, S., He, X. et al. Sequencing DNA methylation and hydroxymethylation at co-occurring chromatin features. Nat Commun 17, 2591 (2026). https://doi.org/10.1038/s41467-026-69429-6
Nyckelord: epigenetik, DNA-metylering, kromatin, enhancers, stamceller