Clear Sky Science · sv
Strukturell och molekylär grund för allosterisk reglering och katalytisk koppling hos mänskligt phosphoribosylformylglycinamidine-syntas
Varför detta enzym är viktigt för hälsan
Varje cell i din kropp är beroende av puriner, små molekyler som driver reaktioner, lagrar energi och bär genetisk information. Cancerceller, som delar sig snabbt, är särskilt hungriga på puriner och ändrar ofta hur de tillverkas. Denna studie fokuserar på ett mänskligt enzym kallat FGAMS, en nyckelspelare i att bygga puriner från grunden. Genom att avslöja FGAMS tredimensionella struktur och hur dess delar rör sig och kommunicerar, visar författarna hur enzymet slås på och av och hur det kan riktas för att bromsa tumörtillväxt.
Livets byggstenar under kontroll
Cellers syntes av puriner sker genom en krävande monteringslinje känd som de novo-vägen, som använder energi och flera enzymer för att sätta ihop en komplex ringstruktur. FGAMS utför det fjärde steget i denna sekvens och ligger i centrum för en större enzymklunga kallad purinosomen, som hjälper till att kanalisera ingredienser effektivt. Eftersom snabbt växande cancerceller ofta förstärker denna väg är enzymer som FGAMS attraktiva läkemedelsmål: att blockera dem kan svälta ut tumörer från de nukleotider de behöver medan friska celler kan förlita sig mer på återvinningsvägar.
En formskiftande molekylär maskin
FGAMS är uppbyggt av tre sammanlänkade delar, eller domäner, som vardera utför olika uppgifter och måste samarbeta i en noggrant ordnad följd. En domän frigör ammoniak från aminosyran glutamin, en annan använder den ammoniaken för att modifiera en liten sockerbaserad molekyl, och en tredje domän fungerar som en regulatorisk nav. Med högupplösande kryo-elektronmikroskopi fångade forskarna FGAMS i tre distinkta arbetstillstånd: med ett energibärande ämne bundet, med ett kortlivat reaktionsintermediär fångat, och med flera substrat och intermediärer närvarande samtidigt. Jämförelse av dessa tillstånd visade att flexibla slingor och en N-terminal ”arm” rör sig dramatiskt och omkonfigurerar enzymet i takt med att kemin framskrider.
En dold tunnel och molekylära portar
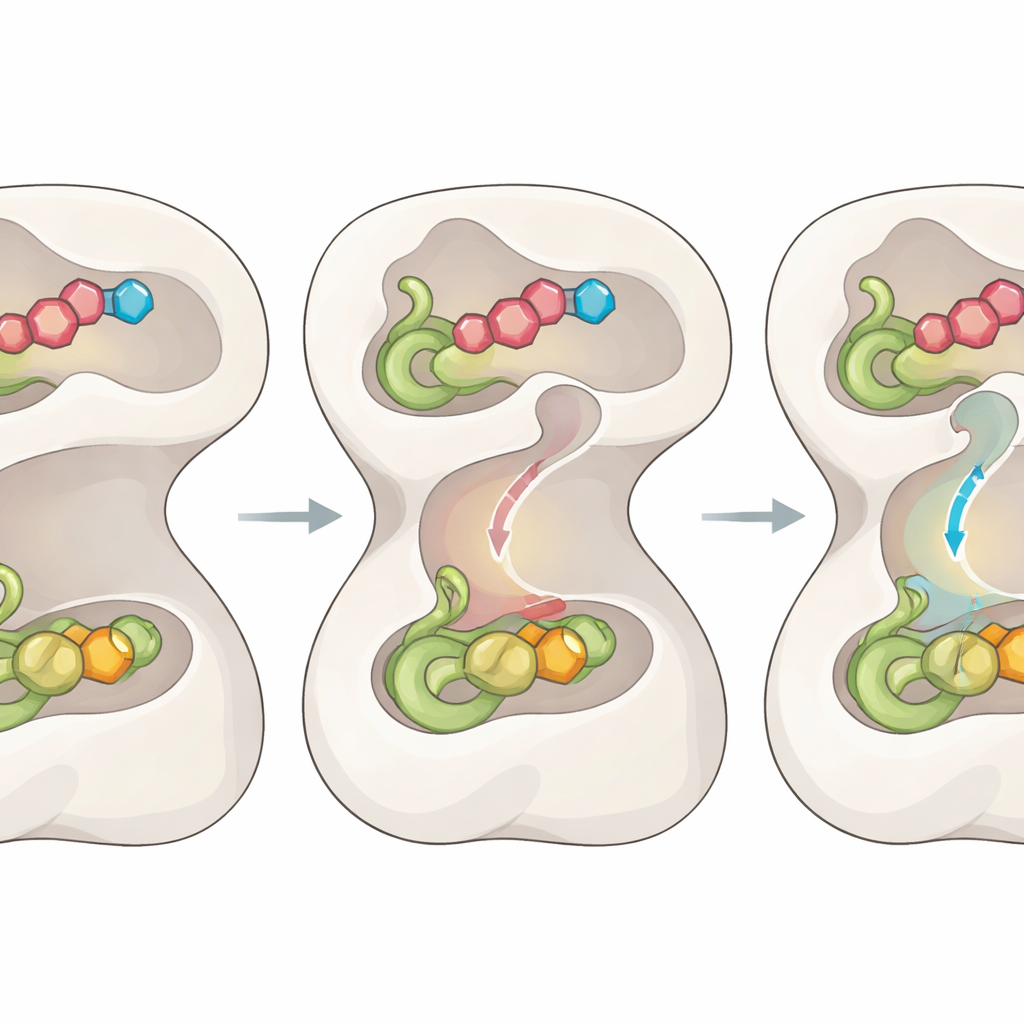
En central gåta har varit hur ammoniaken som frigörs i en domän färdas säkert till den avlägsna platsen där den används, utan att diffundera bort och orsaka skada. De nya strukturerna exponerar en tidigare osedd intern tunnel som förbinder de två platserna, tillsammans med en serie ”portar” bildade av specifika aminosyror. När rätt substrat binder och intermediären bildas, knäpper en central slinga in i en ordnad position, drar i N-terminaldomänen och omarrangerar närliggande slingor i den katalytiska domänen. Denna koreografi öppnar två ingångsportar så att glutamin kan bearbetas och omformar tillfälligt en region som stabiliserar det högenergiska intermediär som krävs för bindningsbrytning.
Koppling av kemi genom rörelse
När reaktionen fortskrider väntar enzymet inte passivt; det använder varje kemiskt steg som en signal. När en kovalent tioesterintermediär bildas i den ammoniakproducerande domänen, vänds de tidigare rörelserna delvis. Detta slappnar av den centrala slingan och ompositionerar portarna för att stänga avflyktvägar, medan två ytterligare portar i varje ände av tunneln svänger upp. Subtila förskjutningar i ett fåtal ”trångsynthets”-residuer vidgar den inre passagen, vilket tillåter en ammoniakmolekyl att färdas genom tunneln direkt in i den andra aktiva siten, där den reagerar med det fångade intermediäret för att producera slutprodukten. Mutationer i portresiduerna orsakar att ammoniak läcker eller att de två reaktionshalvorna kopplas isär, vilket bekräftar att detta port- och kanalsystem är avgörande för effektiv katalys.
Från strukturell insikt till terapeutiska möjligheter
Genom att följa FGAMS genom dess katalytiska cykel lägger studien fram en detaljerad bild av hur domänrörelser, flexibla slingor, interna portar och en tillfällig tunnel är sammankopplade för att koordinera kemin. För en allmän publik är slutsatsen att enzymet beter sig som en liten programmerbar fabrik: det öppnar bara sina dörrar och sitt interna transportband när alla rätta delar är på plats, vilket säkerställer snabbhet och säkerhet. Eftersom FGAMS stöder purintillverkning i cancerceller och har kopplats till sämre överlevnad vid levertumörer, erbjuder de strukturella ritningarna och de nyidentifierade kontrollpunkterna flera möjligheter för att utforma läkemedel som blockerar tunneln, fryser portarna eller fångar viktiga intermediärer, vilket potentiellt kan ge en ny klass av riktade anticancerterapier.
Citering: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Nyckelord: purinsyntes, allosterisk reglering, ammoniakanalisation, cancermetabolism, kryo-EM-struktur