Clear Sky Science · sv
Molekylär verkningsmekanism för småmolekylen SMT-738 på bakteriella lipoproteintransportören LolCDE
Varför detta nya antibiotikum är viktigt
När fler sjukhusinfektioner blir okänsliga för våra bästa antibiotika behöver läkare snabbt läkemedel som kan döda farliga bakterier utan att förstöra de nyttiga mikroberna vi bär med oss. Denna studie klargör hur en lovande experimentell förening, kallad SMT-738, stänger av en avgörande transportmaskin i det yttre skalet hos vissa svårbehandlade bakterier. Genom att visa exakt var och hur drogen biter sig fast i maskineriet pekar arbetet ut vägar mot smartare antibiotika som slår mot superbakterier samtidigt som mycket av tarmfloran skonas.
De dåliga bakteriernas yttre pansar
Många av de mest oroande sjukhuspatogenerna tillhör en grupp som kallas Gramnegativa bakterier. De är svåra att döda eftersom de omsluts av ett dubbellager av yttre skydd. Detta yttre lager byggs upp och underhålls av flera molekylära maskiner som för viktiga byggstenar från det inre membranet, där de tillverkas, ut till ytan. En viktig last är lipoproteiner, som hjälper till att hålla det yttre skalet intakt och stöder processer som näringsupptag och antibiotikaresistens. Ett transportsystem som kallas Lol-vägen, och i synnerhet en pump som heter LolCDE, extraherar lipoproteiner från det inre membranet och överlämnar dem till chaperoner som levererar dem till ytan. Eftersom dessa steg är nödvändiga är de attraktiva mål för nya antibiotika.
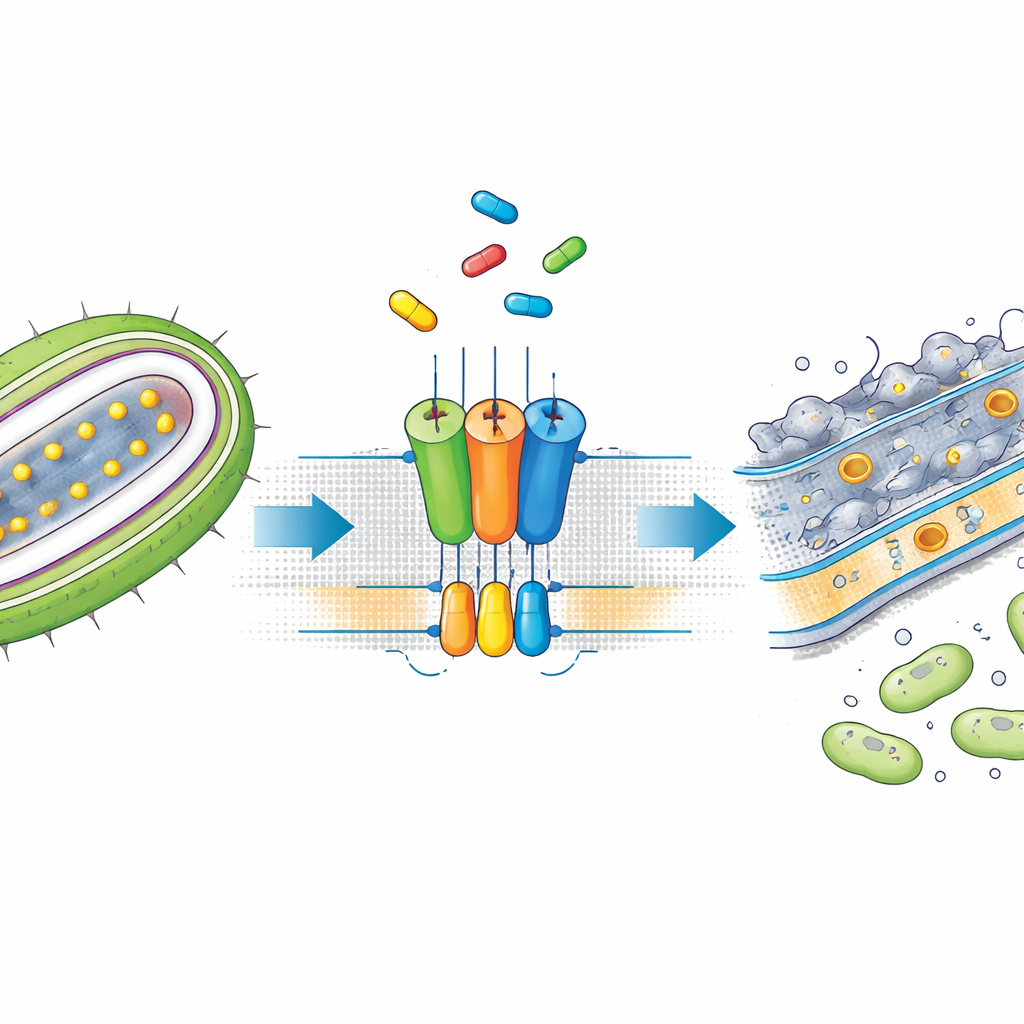
En småmolekyl som stoppar transportbandet
SMT-738 framkom i tidigare screens som en potent blockare av Gramnegativa patogener inom familjen Enterobacteriaceae, inklusive multiresistenta stammar av Escherichia coli och Klebsiella pneumoniae. Men dess precisa verkningsmekanism var oklar. Författarna visade först att SMT-738 förhindrar att ett testlipoprotein släpps av LolCDE i konstruerade bakterier, vilket bekräftar att drogen verkligen stannar transportsteget. Viktigt är att när bakterier bar vissa mutationer i generna för LolCDE-komplexet blev de resistenta mot SMT-738, vilket antyder att drogen verkar genom att binda direkt till denna pump. Dessa observationer banade väg för en strukturell fördjupning i hur föreningen interagerar med transportören.
Blockering av pumpen inifrån
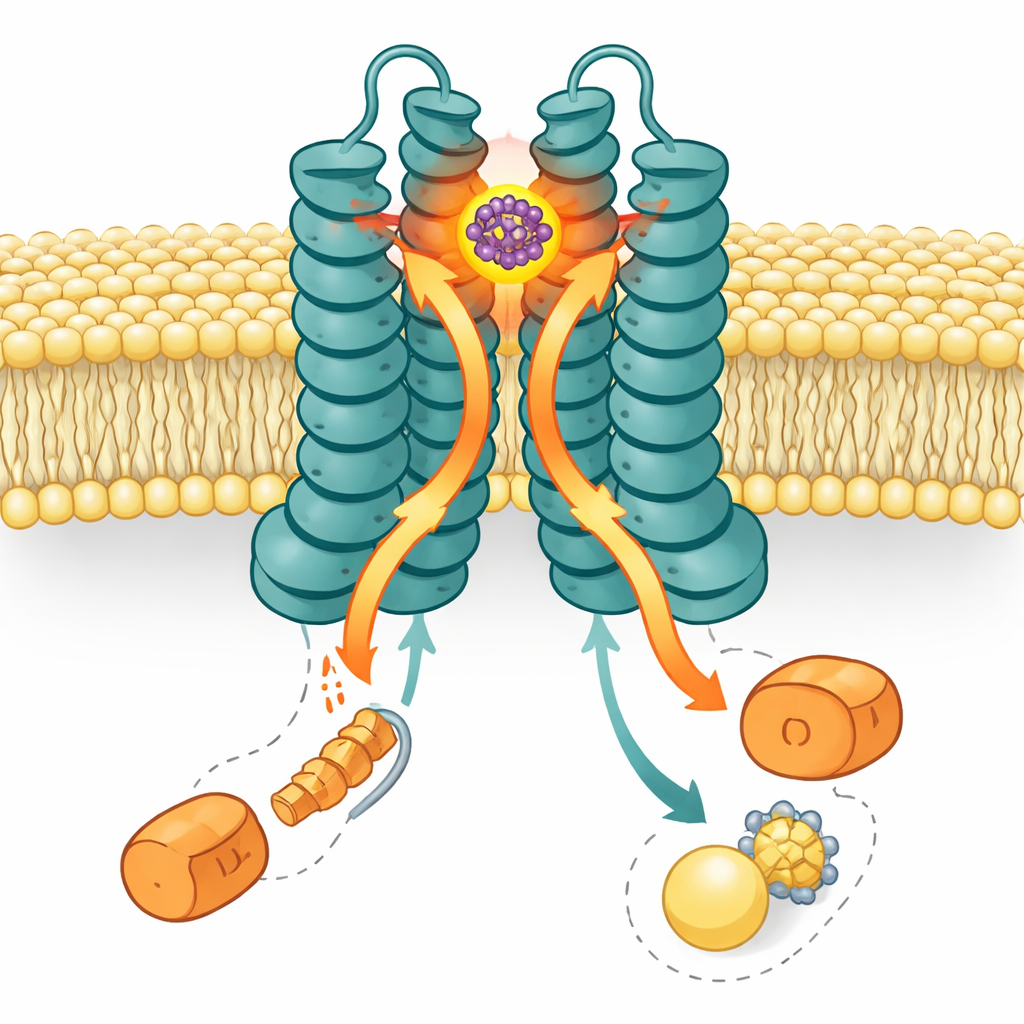
Med hjälp av högupplöst kryo-elektronmikroskopi fångade forskarna en tredimensionell bild av LolCDE med SMT-738 låst på plats. Strukturen visar att drogen kilas in i en ficka i den periplasmiska änden — sidan som vetter mot utrymmet mellan det inre och yttre membranet — mellan två kärnsubenheter, LolC och LolE. Denna plats överlappar det normala dockningsområdet för lipoproteinlast. När SMT-738 upptar denna ficka förskjuts omgivande aminosyror i LolC och LolE med upp till omkring en nanometer. Dessa rörelser skapar steriska kollisioner med där lipoproteinet och dess fettkedjor normalt skulle sitta, vilket effektivt blockerar lasten från att komma in i pumpen. Mutationer i många av dessa fickfodrande rester försvagade antingen drogbindningen eller gjorde bakterierna resistenta, vilket väl överensstämmer med den strukturella bilden.
Utlösning av en ensidig sammanbrott
Berättelsen slutar inte vid bindningsstället. LolCDE drivs av två kopior av en motor(sub)enhet som kallas LolD, vilka sitter på den cytoplasmatiska sidan och förbrukar ATP för att driva transporten. Anmärkningsvärt nog, i SMT-738-bundna strukturen, satt endast en LolD kvar; partnern hade dissocierat. Biokemiska geler och ATPas-assays bekräftade att bindning av SMT-738 orsakar förlust av en LolD och kraftigt minskar pumpens energikonverterande aktivitet. Datorsimuleringar av transportören i ett membran stärkte denna bild: när SMT-738 satte sig i sin ficka spred sig konformationella förändringar nedåt och puttade på kopplingshelixar som förbinder LolC och LolE med LolD. Dessa förskjutningar pressade den LolD som var bunden till LolC in i en ogynnsam kollision, vilket fick den att släppa, medan LolD bunden till LolE stannade kvar. Resultatet är en asymmetrisk, "fastlåst" maskin som inte längre kan förflytta lipoproteiner.
Varför vissa bakterier träffas medan andra skonas
SMT-738 har en önskvärd egenskap: den attackerar starkt läkemedelsresistenta Enterobacteriaceae men lämnar många andra Gramnegativa arter i tarmen i stort sett opåverkade. För att förstå denna selektivitet jämförde teamet sekvenser av LolE från känsliga och resistenta bakterier och koncentrerade sig på positioner som kommer i kontakt med SMT-738. Två rester i LolE, särskilt en motsvarande position D264 i E. coli, stack ut. I känsliga patogener matchade dessa positioner den drogkontakterande versionen i E. coli, medan de i många resistenta tarmkommensaler var ersatta av andra aminosyror. När forskarna konstruerade E. coli med sådana substitutioner blev bakterierna starkt resistenta mot SMT-738 samtidigt som de fortfarande uttryckte LolCDE. Simulationer föreslog att dessa förändringar ändrar den lokala flexibiliteten runt fickan och minskar SMT-738:s förmåga att binda. Intressant nog förlitade sig en annan LolCDE-hämmare, lolamicin, på endast delvis överlappande kontaktpunkter och visade ett annat resistensmönster, vilket antyder olika sätt att angripa samma pump.
Nya ritningar för framtida antibiotika
Genom att kombinera strukturell avbildning, muteringsskanningar, biokemiska tester och datorsimuleringar visar detta arbete att SMT-738 inte bara är ett propp i en kanal. Istället hakar den sig fast på den periplasmiska sidan av LolCDE-pumpen, blockerar lipoprotein-inträdesstället och utlöser sedan långväga skift som slår av en av de två motorenheterna, vilket fryser transportören i ett icke-fungerande tillstånd. Denna "allosteriska fastlåsning"-mekanism representerar ett nytt sätt att inaktivera en bakteriell maskin och hjälper till att förklara varför SMT-738 kan rikta in sig på farliga patogener samtidigt som mycket av mikrobiomet skonas. Den detaljerade kartan över bindningsfickan och den viktiga selektivitetsresten i LolE erbjuder nu en rationell ritning för att designa nästa generations antibiotika som utnyttjar samma sårbarhet med ännu större potens och precision.
Citering: Li, H., Zhu, X., Zhang, D. et al. Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE. Nat Commun 17, 2540 (2026). https://doi.org/10.1038/s41467-026-69411-2
Nyckelord: antibiotikaresistens, Gramnegativa bakterier, lipoproteintransport, LolCDE-hämmare, kryo-EM-struktur