Clear Sky Science · sv
Konstruerade exosom-nanovesiklar för leverans av antikroppar för behandling av inflammatorisk tarmsjukdom
Nytt hopp för en seglivad tarmsjukdom
Inflammatorisk tarmsjukdom (IBD) kan göra vardagen till en ständig kamp mot smärta, diarré och trötthet, och ökar dessutom den långsiktiga risken för koloncancer. Många av dagens läkemedel lugnar skov men återställer inte de felaktiga immunreaktionerna som driver sjukdomen, så symtomen kommer ofta tillbaka. Denna studie presenterar en intelligent konstruerad ”smart” nanopartikel som färdas i blodomloppet, hittar inflammerade områden i tarmen och levererar en tvådelad behandling som både dämpar skadlig inflammation och återbygger varaktig immunbalans.
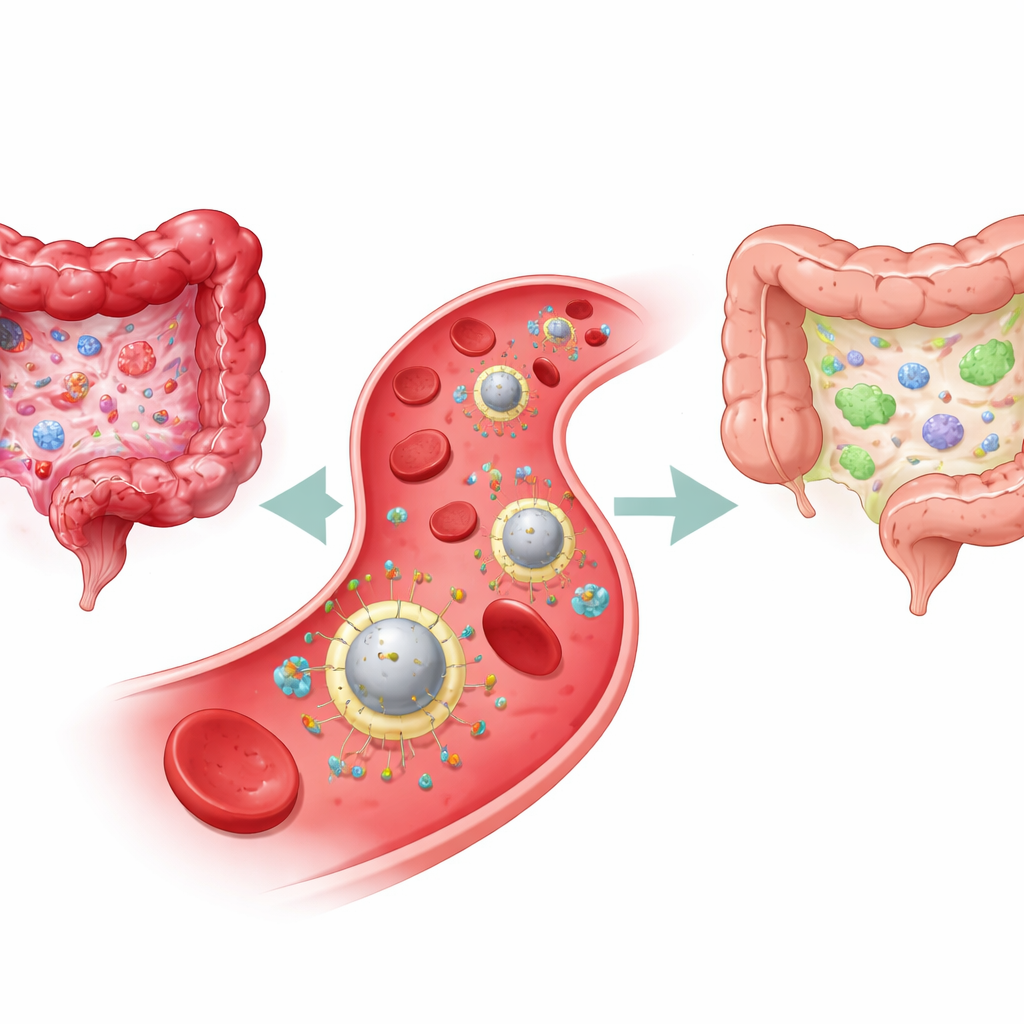
Varför nuvarande behandlingar räcker till kort
IBD, som innefattar Crohns sjukdom och ulcerös kolit, har sin grund i ett kroniskt dragkamp i tarmens immunsystem. Å ena sidan finns aggressiva immunceller och inflammatoriska molekyler som skadar tarmens slemhinna; å andra sidan finns regulatoriska celler som normalt håller denna respons i schack. Standardterapier—såsom steroider, immunosuppressiva medel och biologiska läkemedel—försöker i huvudsak dämpa inflammation över hela kroppen. De kan lindra symtomen, men gör ofta lite för att återställa den underliggande immunbalansen, och bred immunosuppression kan öka risken för infektioner. Även nyare antikroppsbehandlingar som blockerar en viktig inflammatorisk signal kallad interleukin‑23 (IL‑23) hjälper bara en del av patientgruppen och cirkulerar fortfarande brett i kroppen, inte bara där de behövs.
Att bygga ett målinriktat, formförändrande läkemedel
Forskarna ville utforma en behandling som skulle uppföra sig mer som en levande cell än ett enkelt läkemedel. De började med små blåsor som naturligt frigörs av regulatoriska T‑celler—immunceller som främjar tolerans och fredlig samexistens. Dessa blåsor, kallade exosomer, bär proteiner och genetiskt material som kan få andra immunceller att växla till ett lugnande läge. Teamet fusionerade dessa exosomer med fragment av trombocytmembran, och lånade därmed trombocyternas förmåga att fästa vid skadade blodkärl i inflammerad vävnad. På ytan av detta hybridhölje fäste de IL‑23‑blockerande antikroppar med en molekylär ”snöre” som kan klippas av enzymer (matrixmetalloproteinaser) som är rikliga endast i inflammerad tarmslemhinna. Resultatet, kallat PrEXO‑a23, är en nanovesikel som cirkulerar i blodet, hakar fast vid skadade tarmkärl och sedan avger sitt antikroppsinnehåll endast där sjukdomen är aktiv.
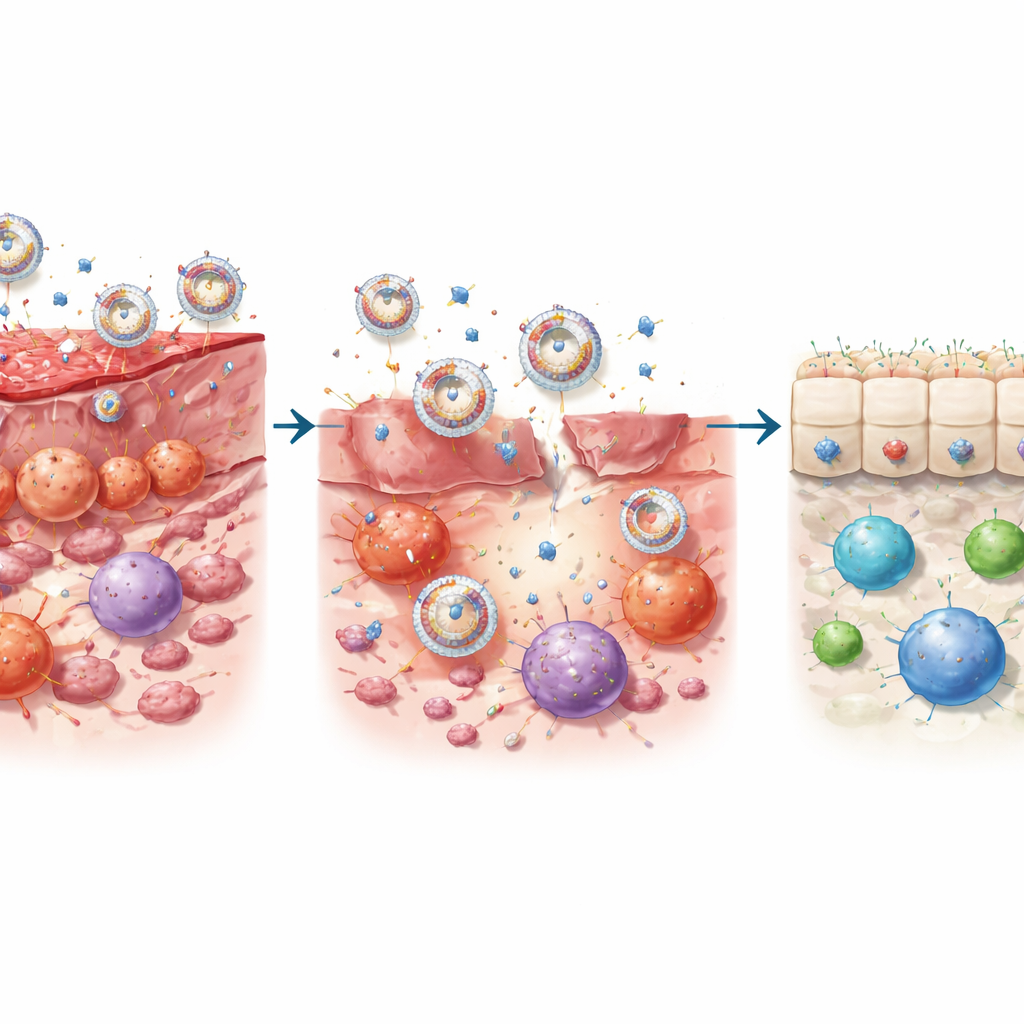
Omprogrammering av tarmens immennärmiljö
I cellstudier överträffade PrEXO‑a23 antingen antikroppen eller exosomerna ensamma. Den minskade starkt bildningen av inflammatoriska T‑hjälpar 17 (Th17)‑celler och frigörandet av skadliga cytokiner som skadar tarmens slemhinna, samtidigt som den skyddade humana tarmepitelceller från celldöd. Samtidigt förde den dendritiska celler—portvakter som instruerar T‑celler—bort från ett fientligt, aktiverande tillstånd mot ett ”tolerant” tillstånd som uppmuntrar tillväxten av regulatoriska T‑celler. I musmodeller av kolit lokaliserade nanovesiklarna effektivt till inflammerad kolonvävnad, togs upp av flera immuncellstyper och frigjorde antikroppar som svar på lokal enzymaktivitet. Denna dubbla verkan—att blockera IL‑23‑driven inflammation och förstärka toleransfrämjande signaler—förde inflammationsmarkörer nära normala nivåer och återställde en hälsosammare blandning av T‑cellstyper.
Reparation av vävnad och förebyggande av långsiktig skada
Mus med kemiskt inducerad kolit som fick PrEXO‑a23 tappade mindre vikt, hade längre, friskare kolon och visade mindre mjältförstoring, ett tecken på systemisk inflammation. Mikroskopisk undersökning visade bevarad tarmarkitektur och tätare fogar mellan epitelceller, vilket indikerar en reparerad barriär. Behandlingen hjälpte också till att återbalansera tarmbakterierna, genom att öka familjer associerade med tarmhälsa och minska de som kopplats till sjukdom. I en mer allvarlig modell som efterliknar övergången från kronisk kolit till koloncancer lindrade PrEXO‑a23 inte bara den pågående inflammationen utan förhindrade fullständigt tumörutveckling och begränsade förtjockning och ärrbildning av tarmväggen som kännetecknar fibros. Molekylära analyser pekade på återställande av det skyddande p53‑signalsystemet—en central väktare mot cancer—vilket visade sig vara viktigt för den anti‑cancerogena effekten.
Mot smartare, mer långvarig IBD‑vård
För en icke‑specialist är huvudbudskapet att detta arbete går bortom att bara ”dämpa” inflammation. Genom att kombinera målinriktad leverans, lokalt antikroppsutsläpp och immundämpande exosominnehåll i ett litet paket, lugnar PrEXO‑a23 både aktiv sjukdom och hjälper till att ombilda immunsystemet mot varaktig tolerans. Hos möss ledde detta inte bara till symtomlindring utan också till skydd mot ärrbildning och koloncancer, två av de mest fruktade komplikationerna vid långvarig IBD. Mycket testande återstår innan en sådan terapi kan nå patienter, men studien visar hur biologiskt inspirerade nanomediciner en dag kan erbjuda mer precis och varaktig kontroll över komplexa immunsjukdomar som IBD.
Citering: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
Nyckelord: inflammatorisk tarmsjukdom, nanomedicin, immunologisk tolerans, exosomer, förebyggande av kolorektal cancer