Clear Sky Science · sv
Strukturella defekter i amyloid-β-fibriller driver sekundär nukleation
Varför små brister i hjärnproteiner spelar roll
I Alzheimers och närliggande hjärnsjukdomar klumpar vissa proteiner ihop sig till långa, trådlika strukturer som kallas amyloidfibriller. Dessa fibriller är inte bara ett kännetecken för sjukdomen; de bidrar också till att generera nya, mycket toxiska proteinpartiklar som kan skada hjärnceller. Denna studie ställer en enkel men kraftfull fråga: fungerar sällsynta strukturella "fel" i amyloidfibriller som huvudvärmeställen som tänder ny skadlig tillväxt? Svaret kan peka mot nya sätt att bromsa eller stoppa sjukdomarna genom att rikta in sig på bara ett fåtal kritiska platser istället för på hela proteinsytan. 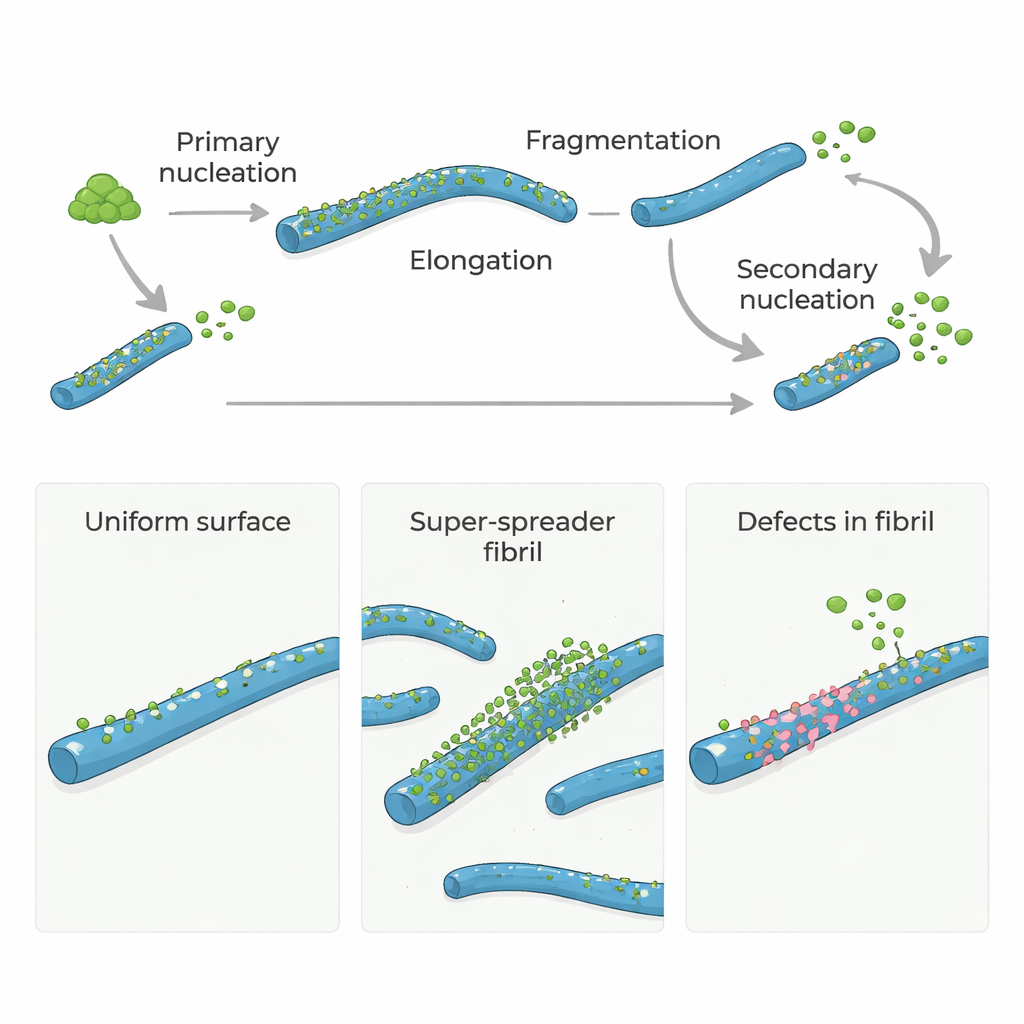
Från tyst protein till okontrollerad kedjereaktion
Amyloid-β (Aβ)-proteiner, centrala för Alzheimers sjukdom, bildar normalt inte snabbt kluster på egen hand. För att komma igång måste några monomerer långsamt sätta ihop sig till de första små fibrillerna, ett steg som kallas primär nukleation. När dessa initiala fibriller finns, växer de snabbt eftersom fler monomerer lägger till vid deras ändar. Ännu viktigare är att befintliga fibriller kan utlösa framväxten av nya fibriller på sina ytor i en process som kallas sekundär nukleation. Detta ytdrivna steg kan översvämma systemet med nya fibriller och små, toxiska oligomerer och förvandla en långsam ström till en okontrollerad kedjereaktion.
Är alla fibrilytor lika farliga?
Många modeller har antagit att hela ytan på en amyloidfibrill är lika effektiv på att katalysera sekundär nukleation. Nya experiment har dock antytt att endast en liten del av ytan verkligen är aktiv. För att undersöka detta använde författarna ett naturligt molekylärt "chaperon" kallat Brichos, känt för att blockera sekundär nukleation av Aβ40 och Aβ42 (två viktiga former av amyloid-β). Genom att noggrant mäta hur mycket fluorescensmärkt Brichos som binder till fibrillerna fann de att det binder hårt men i mycket små mängder: ungefär en Brichosmolekyl per 100–150 Aβ-molekyler i en fibrill. Ändå var denna glesa täckning tillräcklig för att undertrycka mer än 90% av den sekundära nukleationen, vilket betyder att endast sällsynta, lokaliserade platser—snarare än hela ytan—dominerar produktionen av nya toxiska aggregat.
Undersöka rollen för dolda defekter
Dessa fynd föreslog att de avgörande nukleationsställena kan vara strukturella defekter—små oregelbundenheter som bildas när fibriller växer, såsom felanpassade lager eller delvis exponerade inre kärnor. För att testa denna idé direkt odlade forskarna Aβ40-fibriller under två olika förhållanden. En uppsättning, "kontroll"-fibrillerna, bildades under typiska, starkt översaturerade förhållanden som gynnar snabb tillväxt och kinetisk fångst av defekter. Den andra uppsättningen skapades med en långsam, temperaturkontrollerad härdningsprocedur: fibrillerna växte med mycket låg drivkraft, nära deras löslighetsgräns, där felaktiga strukturer kan lösas upp eller repareras innan de låses in. Högupplöst kryo-elektronmikroskopi visade att båda fibrilluppsättningarna i allt väsentligt såg identiska ut vad gäller form och vridning, vilket indikerar att härdningsprocessen inte förändrade den grundläggande morfologin. 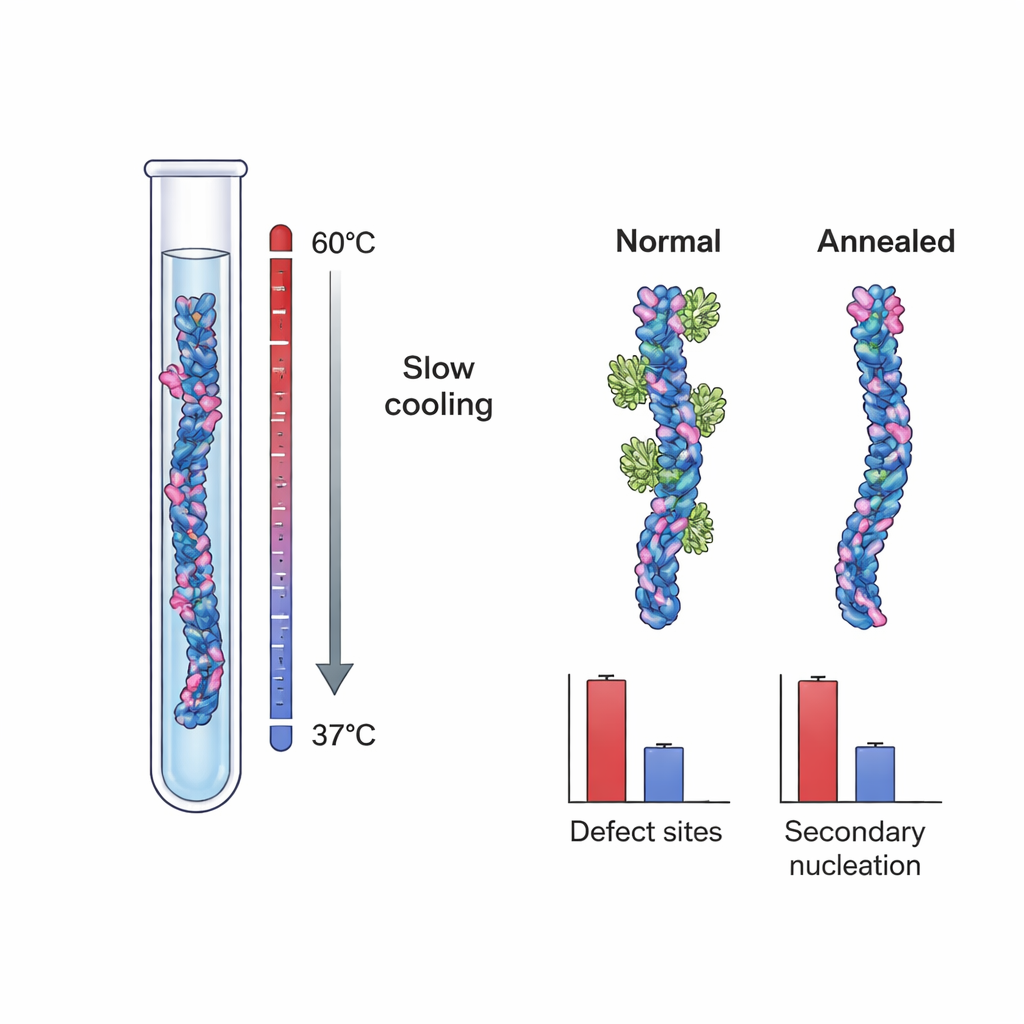
När teamet mätte Brichosbindning till dessa två fibriltyper upptäckte de en slående skillnad. Kontroll-Aβ40-fibriller hade cirka en Brichos-bindningsplats per ~100 monomerer, vilket återigen indikerar sällsynta men viktiga platser. Härdade fibriller hade däremot bara ungefär en plats per ~800 monomerer—en nästan 90% minskning i platsfrekvens. I separata tester där dessa fibriller tillsattes som "frön" i färska Aβ40-lösningar var härdade fibriller mycket mindre effektiva på att utlösa ny aggregering, även när deras totala massa matchades med kontrollfibrillerna. Detaljerad kinetisk modellering visade att denna minskning i förmåga att fröa inte kunde förklaras enbart av skillnader i fibrillängd. Istället stämde den kvantitativt överens med det reducerade antalet Brichos-bindningsplatser, vilket starkt stöder idén att tillväxtdefekter fungerar som huvudmotorer för sekundär nukleation.
En allmän princip med terapeutiskt löfte
Genom att kombinera termodynamiska argument, omanalys av tidigare arbete och jämförelser mellan flera amyloidbildande proteiner hävdar författarna att sällsynta tillväxtdefekter sannolikt är centrala för sekundär nukleation i många system, inte bara Aβ relaterat till Alzheimers. Dessa defekter exponerar delvis fibrillens tätt packade inre kärna och erbjuder ett färdigt skelett där nya oligomerer och fibriller kan bildas mycket lättare än på en slät yta. Att identifiera dessa defekter som de viktigaste bovarna öppnar nya vägar för läkemedelsdesign. Istället för att försöka blockera alla möjliga interaktioner på en fibrilyta kan terapier sikta på att skydda eller reparera just dessa sällsynta defektställen, eller att minska de förhållanden som skapar dem från början. I praktiken kan det innebära att sänka den effektiva koncentrationen av amyloidbildande proteiner i hjärnan eller att designa molekyler, inspirerade av Brichos, som känner igen och neutraliserar defektdrivna nukleationshotspots. Lyckas man med sådana strategier kan man kapa huvudkällan till toxiska oligomerer och bromsa utvecklingen av amyloidsambandade sjukdomar.
Citering: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Nyckelord: amyloidfibriller, Alzheimers sjukdom, sekundär nukleation, proteinigaggregation, Brichos-chaperon