Clear Sky Science · sv
Tävlande vätebindningsordningar driver vattnets anomalösa ytspänning
Varför vattnets yta är märkligare än den ser ut
Vattnets yta tillåter insekter att gå på dammar, formar regndroppar och styr hur bubblor bildas och brister. När forskare mäter hur ”spänd” den ytan är — ytspänningen — upptäcker de dock att vatten beter sig förvånansvärt märkligt när det blir kallare, särskilt när det kyls under sin normala fryspunkt. Den här artikeln använder avancerade datasimuleringar för att avslöja hur den dolda organiseringen av vattenmolekyler vid ytan förklarar detta länge olösta mysterium.
Två dolda typer av flytande vatten
Även om vi upplever vatten som en enkel, homogen vätska kan dess molekyler lokalt ordna sig på två kontrasterande sätt. Den ena ordningen är mer tätpackad och oordnad; författarna kallar detta ρ-tillståndet. Den andra är mer öppen och symmetrisk, där varje molekyl är omgiven i en ungefär fyrvägs, tetraedrisk ordning; detta kallas S-tillståndet. Tidigare arbete har föreslagit att balansen mellan dessa två lokala mönster hjälper till att förklara många av vattnets ovanliga bulkegenskaper. Här undersöker författarna hur samma tvåtillståndsbild spelar ut vid gränsen mellan luft och vatten, där ytspänningen uppstår.
Hur ytan drar molekylerna i linje
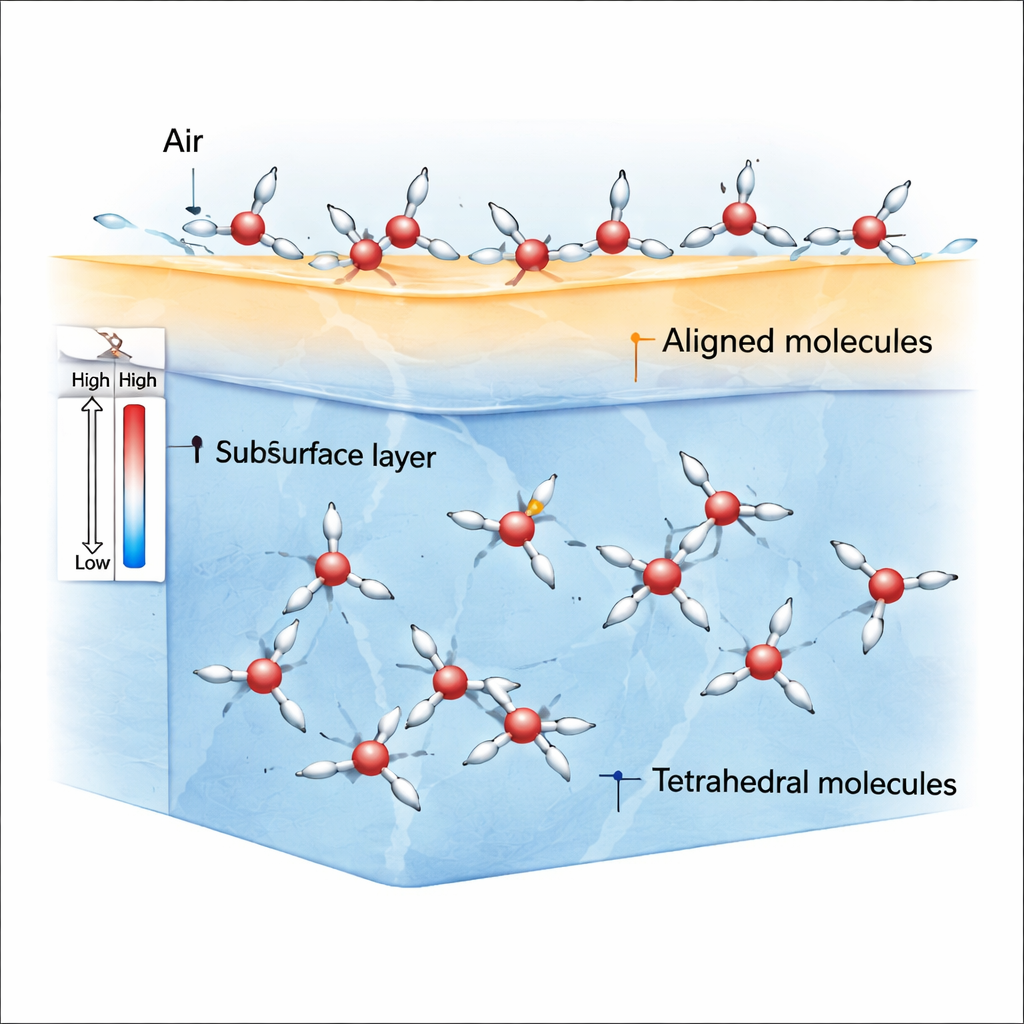
Vid gränsytan mellan luft och vatten upplever molekylerna inte längre lika drag i alla riktningar. Denna brutna symmetri gynnar ρ-tillståndets molekyler, vars väteatomer och molekylära dipoler lätt kan luta åt en föredragen riktning. Simuleringar visar att nära rumstemperatur och något under blir det allra översta skiktet av vattnet packat med dessa inriktade ρ-molekyler, medan S-tillståndets molekyler är vanligare strax under ytan och i bulkfasen. Eftersom ρ-molekylerna linjerar upp sig kraftigt skapar de en obalans i krafterna — stressanisotropi — som genererar en relativt stor ytspänning jämfört med vanliga vätskor som bensin.
Varför kylning först bromsar, sedan snabbar upp ytspänningen
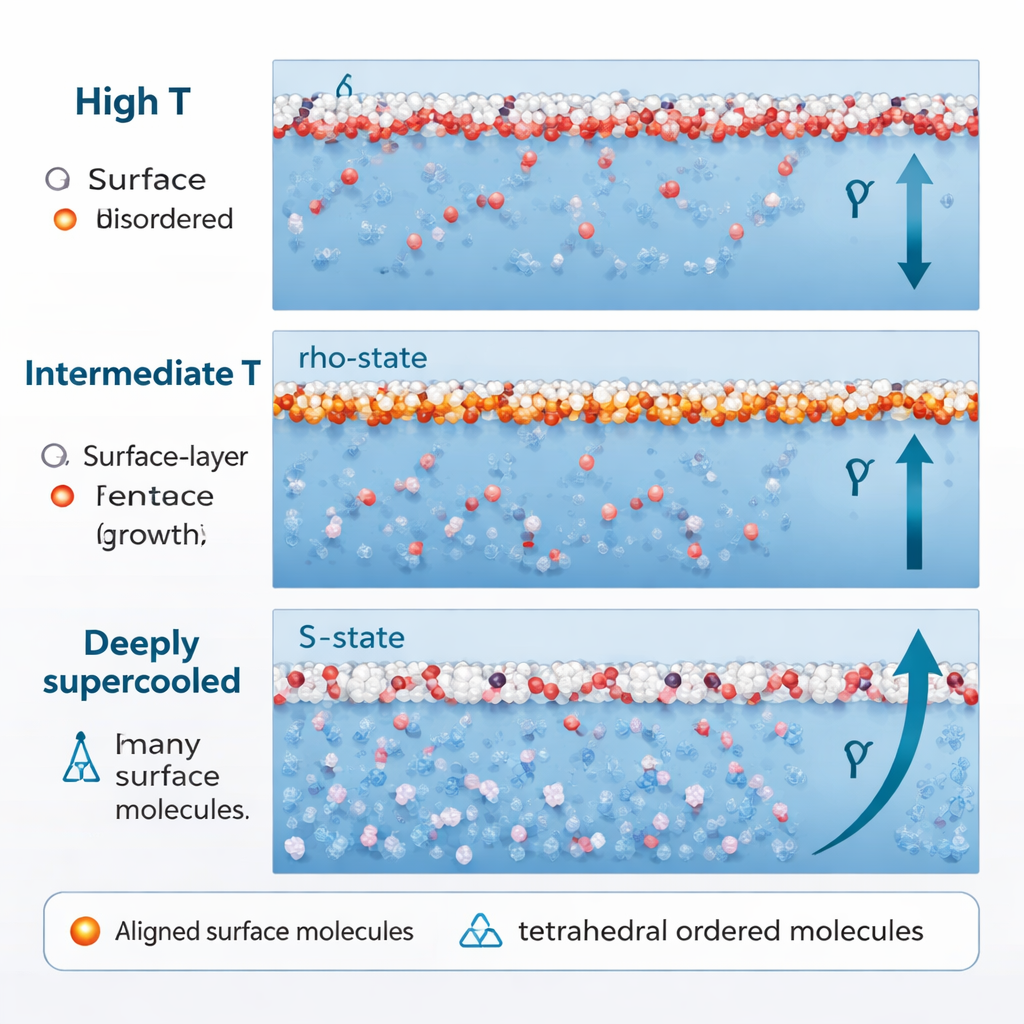
I de flesta enkla vätskor gör kylning ytan stadigare i en nästan linjär ökning av ytspänningen. Vatten gör detta bara vid högre temperaturer. När det kyls mot ungefär –0,15 °C (275 K) börjar ökningen av ytspänningen avta. Simuleringarna visar att denna avmattning sker eftersom ρ-molekylerna vid ytan redan har blivit så inriktade som möjligt; ytterligare kylning förändrar knappt deras bidrag. Samtidigt förblir S-molekylerna i underskiktet till största delen slumpmässigt orienterade, så de gör lite för att öka ytspänningens stress. Nettoresultatet är en slags platå: temperaturen fortsätter sjunka, men ytspänningen växer bara trögt.
Djup överkylning utlöser en andra åtstramning
När vatten kyls mycket längre, långt under sin normala fryspunkt in i det djupt överkylta området (runt 250 K och lägre), förändras dess beteende igen. Andelen S-tillståndets tetraedriska strukturer ökar kraftigt, även nära ytan. Avgörande är att dessa S-molekyler inte längre pekar i slumpmässiga riktningar. Deras dipoler börjar rikta sig längs riktningen vinkelrätt mot ytan, drivet av interaktioner mellan intilliggande molekylära dipoler och av ett område med negativt tryck precis under ytan. När det händer börjar S-tillståndets vatten, som tidigare mildrade ytspänningen, nu att stärka den. Detta ordnade tillskott ger en förnyad, snabbare ökning — den ”reentranta” uppgången — i ytspänningen vid låga temperaturer.
Från ytmysterier till isbildning och vidare
Samma tetraedriska S-tillståndskluster som stelnar ytan vid låga temperaturer liknar också tidiga byggstenar för vissa former av is, och simuleringarna visar att de är förhöjda nära gränsytan. Det betyder att luft–vatten-gränsen kan fungera som en vagga för isbildning, vilket hjälper till att förklara varför frysning ofta börjar vid ytor. Mer allmänt ger arbetet en konkret, molekylnivåkoppling mellan hur vattenmolekyler ordnar och orienterar sig och hur starkt ytan drar inåt. Denna strukturellt-mekaniska bild löser inte bara den märkliga temperaturkurvan för vattnets ytspänning, utan erbjuder också en vägkarta för att förstå och kontrollera interfaciala fenomen i andra nätverksbildande vätskor, från överkylvt vatten i moln till material som används inom teknik och biologi.
Citering: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Nyckelord: vattnets ytspänning, vätebindning, överkylvt vatten, vätskestruktur, iskärnbildning