Clear Sky Science · sv
STING samverkar med TOX för att undertrycka HO-1-uttryck och utlösa ferroptos i tumörinfiltrerande CD8+-T‑celler och immunoterapiresistens
Varför denna forskning är viktig för cancerbehandling
Moderna cancerimmunoterapier fungerar genom att frigöra kroppens egna mördande T‑celler, men många tumörer hittar ändå sätt att slå av dessa celler. Denna studie avslöjar en dold självdestruktionsknapp inne i CD8+-"mördare" T‑celler som tumörer utnyttjar, och visar hur avstängning av den knappen kan göra immunoterapi mycket effektivare.
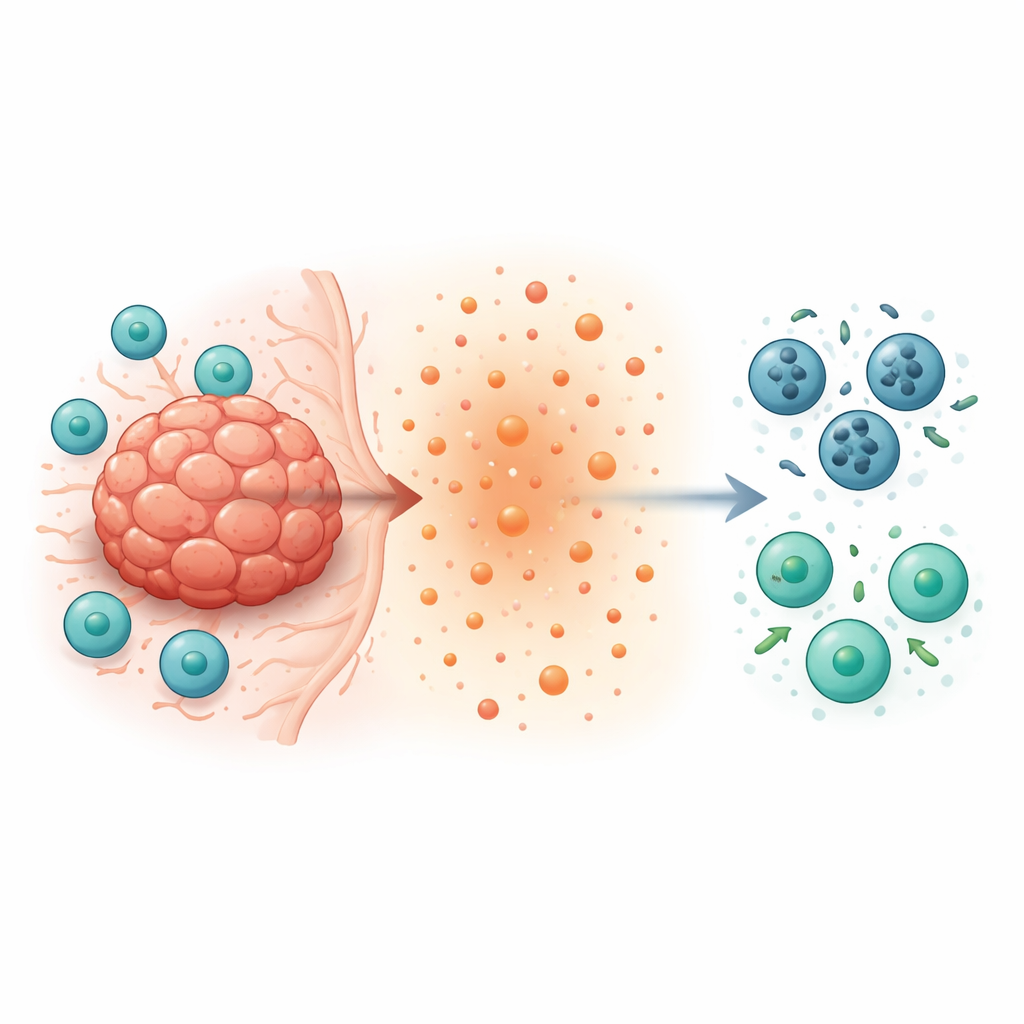
En dold dödsväg i tumörbekämpande T‑celler
Inne i en tumör ska CD8+-T‑celler jaga och förstöra cancerceller. Istället blir de ofta sällsynta, slöa och kortlivade. Författarna fokuserade på två molekyler inuti T‑celler—STING, en sensor av DNA‑skador, och TOX, ett protein kopplat till T‑cellsutmattning. De konstruerade möss där CD8+-T‑celler saknade STING, TOX eller båda, och satte sedan in flera typer av tumörer. Överraskande nog rensade möss vars T‑celler saknade antingen STING eller TOX tumörerna betydligt bättre. Deras tumörer växte långsammare, innehöll många fler CD8+-T‑celler, och dessa T‑celler producerade större mängder cancerdödande molekyler som interferon‑gamma och granzyme B. Detta pekade på ett internt program som tyst saboterade T‑celler inne i tumörer.
Hur järndriven celldöd försvagar immuniteten
Genom att granska genaktivitet i tumörinfiltrerande T‑celler fann forskarna att normala T‑celler inne i tumörer var primade för en speciell form av celldöd kallad ferroptos. Till skillnad från apoptos utlöses ferroptos av järnöverskott och ansamling av skadade fetter i cellmembran. I vanliga CD8+-T‑celler exponerade för tumörceller var gener som främjar järnackumulering och lipidskada påslagna, medan skyddande gener var nedreglerade. I kontrast visade STING‑ eller TOX‑defekta T‑celler motsatt mönster: de uttryckte mer av de skyddande enzymerna HO‑1 och GPX4, hade lägre järnnivåer, mindre lipidperoxidation, friskare mitokondrier och motstod ferroptotisk död. Laboratorietester bekräftade att kemisk blockad av ferroptos höll normala T‑celler vid liv, medan borttagning av STING eller TOX gjorde dem naturligt motståndskraftiga.
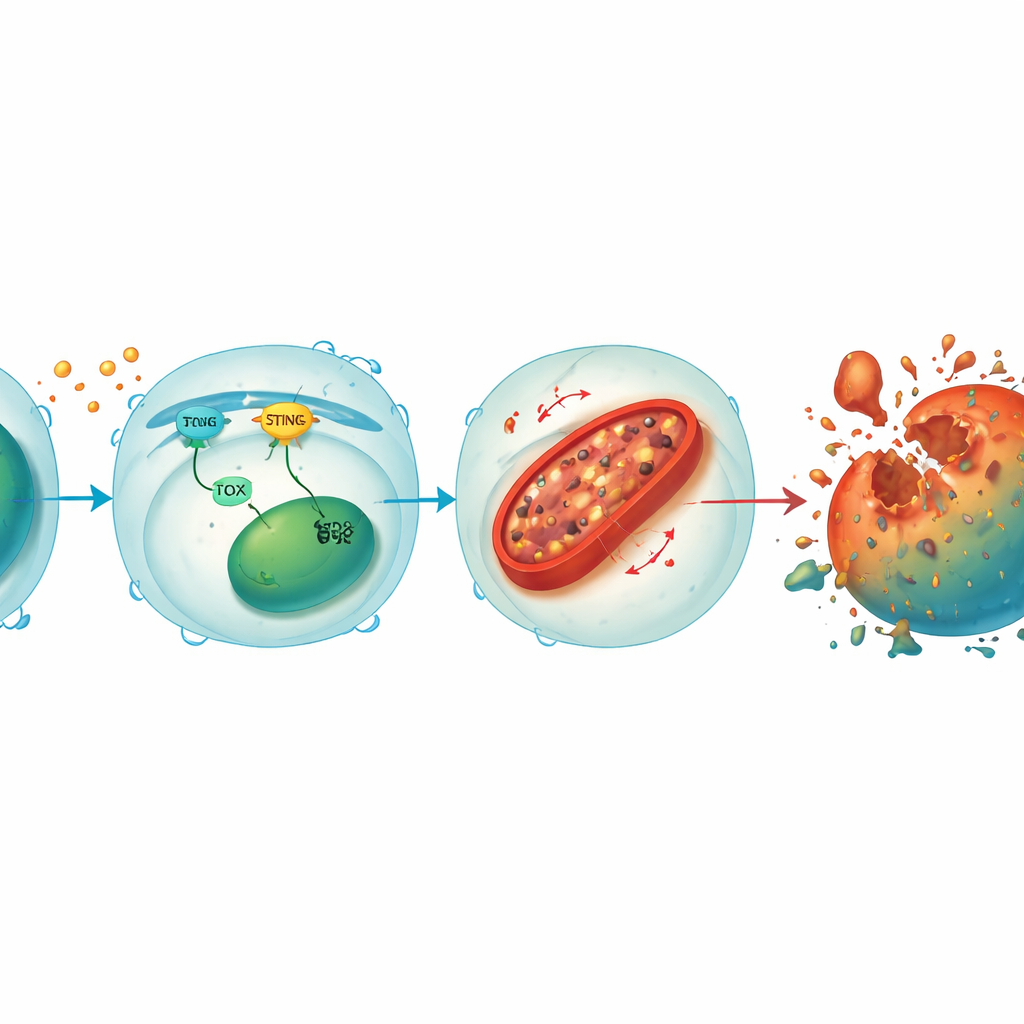
En loop som kopplar stressignaler till mitokondrieskada
Vid en djupare granskning upptäckte teamet att STING och TOX bildar en förstärkande loop inne i CD8+-T‑celler. När tumör‑ eller virussignaler aktiverar STING triggar det nedströmsfaktorer som ökar TOX, och TOX i sin tur hjälper till att upprätthålla STING‑aktivitet. Tillsammans undertrycker de HO‑1, ett enzym som normalt hjälper till att hålla cellulärt järn i schack. Med HO‑1 nedtryckt bygger järn upp i mitokondrierna—cellens kraftverk—vilket leder till höga nivåer av reaktiva syremolekyler och oxidation av membranfetter. Denna mitokondrieskada urholkar energiproduktionen och skjuter slutligen T‑cellen in i ferroptos. Återställande av STING eller TOX i knockout‑T‑celler återförde järnöverskottet och celldöd, medan ytterligare sänkning av HO‑1 gjorde även de skyddade T‑cellerna sårbara igen, vilket understryker HO‑1 som en central broms i denna destruktiva väg.
Hur tumörtillverkat laktat drar i avtryckaren
Tumörmikromiljön är rik på laktat, en restprodukt av cancercellernas förändrade metabolism. Studien visar att detta laktat inte bara är metabolt avfall—det hjälper aktivt till att slå på ferroptos‑brytaren i T‑celler. Jämfört med andra celler var CD8+-T‑celler särskilt känsliga för laktat. När laktat tog sig in i cellerna genom specifika transportörer orsakade det järnansamling, mitokondrieförminskning, DNA‑förlust i mitokondrier och mer oxidativ skada. Samtidigt ökade laktat STING‑ och TOX‑aktivitet och undertryckte ytterligare HO‑1. T‑celler som saknade STING eller TOX var mycket mer motståndskraftiga mot laktatinducerad skada. Blockad av en nyckeltransportör för laktat med ett läkemedel (AZD3965) skyddade CD8+-T‑celler från ferroptos i möss, ökade deras närvaro inne i tumörer och bromsade tumörtillväxten, vilket efterliknade fördelen av genetisk deletion av STING i T‑celler.
Att vända en sårbarhet till en terapeutisk fördel
Dessa mekanistiska insikter har praktiska implikationer. När forskarna använde adoptiv cellterapi—infusion av laboratorieaktiverade T‑celler—fann de att T‑celler konstruerade att sakna STING eller TOX gav mycket starkare tumörkontroll än normala T‑celler. Dessutom gav kombinationen av dessa "ferroptosresistenta" T‑celler med befintliga behandlingar såsom PD‑1‑ eller TIM‑3‑checkpointhämmare, cisplatin‑kemoterapi eller ett STING‑aktiverande läkemedel markant bättre tumörinvolution än någon enskild terapi ensam. Slutligen, i tumörprover från patienter med livmoderhalscancer kopplades högre TOX‑ och lägre HO‑1‑nivåer i tumörinfiltrerande lymfocyter till sämre överlevnad, vilket tyder på att denna väg också formar kliniska utfall hos människor.
Vad detta betyder för framtida cancervård
Enkelt uttryckt visar studien att tumörer kan få våra bästa cancerbekämpande T‑celler att rosta inifrån genom att driva en järndriven form av celldöd. En laktat–STING–TOX‑krets sänker det skydd som HO‑1 erbjuder, skadar mitokondrier och leder till ferroptos, vilket tunnar ut ledet av effektiva CD8+-T‑celler. Att störa denna krets—genom att konstruera T‑celler som saknar STING eller TOX, öka HO‑1 eller blockera laktatinträde—håller T‑cellerna vid liv, energiska och redo att attackera. Detta arbete pekar mot nästa generations immunoterapier som kombinerar metabolisk och genetisk finjustering av T‑celler med befintliga läkemedel för att övervinna resistens och ge mer hållbar cancerkontroll.
Citering: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Nyckelord: cancerimmunoterapi, CD8 T‑celler, ferroptos, tumörmikromiljö, STING TOX HO-1‑väg