Clear Sky Science · sv
Analys av det transkriptomiska och metabolomiska landskapet hos prostatacancer med olika anatomiska ursprung med snFLARE-seq och mxFRIZNGRND
Varför denna forskning är viktig för patienter och familjer
Prostatacancer är den vanligaste cancerformen hos män, men inte alla prostatatumörer beter sig likadant. Var en tumör uppstår i prostatan och hur den svarar på hormonbehandling kan starkt påverka om sjukdomen återkommer eller blir aggressiv. Denna studie använder två nya laboratorietekniker på rutinmässigt sparade sjukhusprover för att visa hur tumörer från olika regioner i prostatan skiljer sig i celltyper, immunceller runt tumören och metabolism. Dessa insikter kan hjälpa läkare att bättre förutsäga vilka som behöver intensiv behandling och avslöja nya sätt att förhindra att cancer utvecklas till svårbehandlade former.
Olika kvarter inne i samma körtel
Prostatan har distinkta regioner, främst perifera zonen och transitionszonen. Ungefär 70 % av prostatacancer uppstår i den perifera zonen, medan ungefär en fjärdedel börjar i transitionszonen. Genom att följa mer än 400 män som genomgick operation fann forskarna att tumörer begränsade till transitionszonen tenderade att återkomma senare och mer sällan än de i den perifera zonen. Cancer som spred sig över båda zonerna var mest oroande, återföll snabbare och visade starkare motstånd mot hormonsänkande behandling. Dessa kliniska mönster, bekräftade hos östasiatiska patienter, tyder på att tumörens ursprungliga ”kvarter” formar dess framtida beteende.
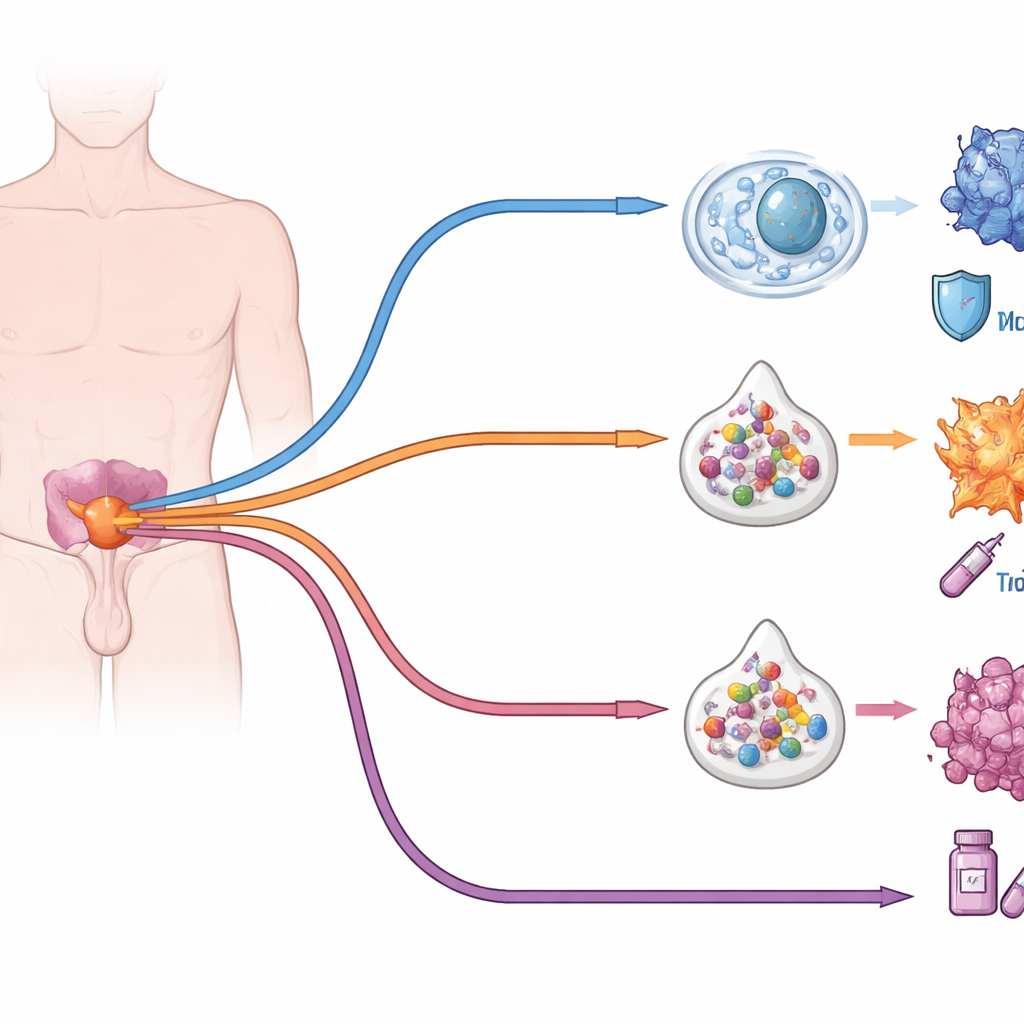
Läsa skadat vävnad på single-cell-nivå
De flesta patologiprov på sjukhus bevaras som formalinfixerade, paraffininslutna (FFPE) block, vilket är utmärkt för långtidsförvaring men svårt att analysera på molekylär nivå. Teamet utvecklade två kompletterande metoder anpassade för dessa prover. Den första, kallad snFLARE‑seq, extraherar försiktigt kärnor och fångar RNA från enskilda celler samtidigt som kemiska korsbindningar omvänds med omsorg. Detta tillåter forskare att mäta vilka gener varje cell använder, även år efter operation. Den andra metoden, mxFRIZNGRND, använder djupfrysning, malning och optimerade lösningsmedel för att återvinna både vattenlösliga molekyler och fetter utan att förstöra ömtåliga föreningar. Tillsammans avslöjar dessa verktyg både de ”budskap” som finns i cellerna och småmolekylerna som driver dem.
Hur tumörceller och deras omgivning skiljer sig åt
Genom att tillämpa snFLARE‑seq på över 100 000 celler från prostatatumörer och intilliggande normalvävnad kartlade forskarna 13 huvudsakliga celltyper, inklusive cancerösa epitelceller, immunceller och stödjande fibroblaster. Tumörer i den perifera zonen var berikade på särskilda epitelialsubtyper som tidigare kopplats till aggressiv sjukdom. En subtyp som kallas ”club”-celler visade stark aktivering av inflammationsrelaterade IL‑17‑signalvägar och ökad känslighet för manliga hormoner, och dess genprofil förutspådde sämre utfall i stora publika cancert databaser. Efter hormonbehandling såg tumörer som spände över båda zonerna inte bara ut som en blandning av perifera och transitionstumörer. Istället blev deras epitelceller ”polariserade”: aggressiva subtyper blev ännu mer dominerande medan andra nästan försvann, vilket tyder på att behandlingen kan omforma tumören snarare än bara krympa den.
Immunsvar vänd upp och ner
Studien undersökte också hur immunceller förändras mellan tumörtyper. I obehandlade tumörer var minnes‑T‑celler och cytotoxiska T‑celler vanliga, och det övergripande immunlandskapet såg liknande ut mellan perifer och transition. Efter hormonbehandling i tvärzonstumörer vände denna balans. Utnötta T‑celler och regulatoriska T‑celler—båda kända för att dämpa immunsvar—blev dominerande, medan kraftfulla effektorceller minskade. Makrofager och dendritiska celler skiftade också mot mer hämmande, ”M2‑lika” och sämre antigenpresenterande tillstånd. Många av dessa förändringar följdes av ökad aktivitet i androgenreceptorn och förändrad kolesterolmetabolism, vilket pekar på en hormonstyrd, metabolt justerad immunnedsättning som kan begränsa effekten av efterföljande immunterapier.
Den dolda sidan av tumörmetabolismen
Med hjälp av mxFRIZNGRND profilerade teamet över tusen lipidarter och hundratals andra metaboliter i matchade vävnadsskivor. Tumörer i den perifera zonen visade en överraskande enhetlig, lågaktiv lipidprofil, vilket tyder på ett metabolt ”vilande” tillstånd som kan hjälpa celler att överleva stressiga behandlingar. I kontrast visade tumörer som spände över båda zonerna efter hormonbehandling uppreglerade vägar som förser byggstenar för cellmembran, DNA och RNA samt energi. Viktiga förändringar inkluderade snabb omvandling av kolin till fosfatidylkolin för nya membran, ökad nedbrytning av socker och omkoppling av ceramid och andra fettbaserade signalmolekyler. När dessa metabola fynd kombinerades med genaktivitetsdata och stora cancerregister framträdde fyra centrala vägar—kolin‑ och fosfolipidmetabolism, central kolmetabolism, pyrimidinsyntes och ceramidmetabolism—som starkt kopplade till aggressiv sjukdom och dålig prognos.
Vad detta betyder för framtida vård
För icke‑specialister är huvudbudskapet att prostatacancer inte är en enda sjukdom utan många, formade av sin startplats och av de behandlingar som syftar till att kontrollera den. Hormonbehandling kan oavsiktligt selektera för cancerceller med särskilt starka hormon‑signalkretsar och omkonfigurera omgivande immunceller och stödjeceller på sätt som gynnar återfall. Genom att utvinna data från gamla FFPE‑prover med snFLARE‑seq och mxFRIZNGRND kan forskare nu följa dessa skiften på single‑cell‑ och metabol nivå i verkliga patienter, inte bara i modeller i laboratorium. På sikt kan detta arbete leda till mer personanpassad vård: att välja zon‑specifika läkemedel (till exempel rikta IL‑17 i perifera zon‑tumörer), addera agenter som blockerar nyckelmetabola vägar som kolin eller PI3K‑AKT‑signalering, och utforma smartare kombinationer av hormon- och immunterapier som undviker att väcka vilande cancerceller samtidigt som kroppens försvar bevaras.
Citering: He, D., Hu, H., Xiao, K. et al. Analysis of the transcriptomic and metabolomic landscape of prostate cancer with different anatomical origins using snFLARE-seq and mxFRIZNGRND. Nat Commun 17, 2461 (2026). https://doi.org/10.1038/s41467-026-69347-7
Nyckelord: heterogenitet i prostatacancer, single-cell-sekvensering, tumörmetabolism, resistens mot hormonbehandling, tumörmikromiljö