Clear Sky Science · sv
Seq-Scope-eXpanded: rumslig omik bortom optisk upplösning
Se celler i skarpare detalj
Våra kroppar är uppbyggda av otaliga små celler, var och en full av aktivitet som vi vanligtvis inte kan se, inte ens med kraftfulla mikroskop. Denna artikel presenterar Seq-Scope-X, en teknik som låter forskare zooma in på vävnaders inre funktioner med en hittills osedd klarhet, och kartlägga vilka gener och proteiner som är aktiva på precisa platser i och mellan celler. Den detaljnivån kan förändra hur vi studerar utveckling, immunsystemet och sjukdomar som cancer eller leverskador.
Varför kartlägga molekyler på plats?
Celler fungerar inte isolerat: de lever i grannskap, bildar skikt och specialiserar sig beroende på var de befinner sig. Traditionella gensekvenseringsmetoder sönderdelar vävnader och förlorar därmed detta rumsliga sammanhang. Nyare ”rumsliga omik”-verktyg bevarar molekylerna på plats, men det har funnits en kompromiss. Metoder baserade på bildtagning kan se mycket små detaljer men mäter vanligtvis bara en begränsad uppsättning gener. Sekvenseringsbaserade metoder kan läsa nästan alla gener samtidigt, men de suddar ut finkorniga strukturer och sprider ofta signaler över flera mikrometer — större än många subcellulära strukturer. Författarna gav sig i kast med att överbrygga detta gap: bevara sekvenseringens rika, opartiska läsning samtidigt som man når eller till och med överträffar skärpan hos moderna mikroskop.
Sträcka vävnad för att slå optiska gränser
Den grundläggande idén bakom Seq-Scope-X är till synes enkel: förstora själva vävnaden försiktigt så att varje ursprunglig nanometer av strukturen blir lättare att urskilja. Teamet fäster först RNA-molekyler — eller särskilda DNA-taggar knutna till antikroppar — i ett mjukt hydrogel som byggs runt vävnadsskivan. De digererar sedan bort den ursprungliga vävnaden och sväller gelen i en saltlösning, vilket fysiskt sträcker allt ungefär tre gånger samtidigt som relativa positioner i stort sett bevaras. Denna expanderade gel läggs ovanpå ett ultratätt sekvenseringschip täckt med fångstprober. Genom att försiktigt värma ihopställningen frigörs de fästa molekylerna från gelen och återfästs på chippet, vilket sedan kan sekvenseras för att avslöja vilka gener eller proteiner som fanns vid varje liten koordinat. 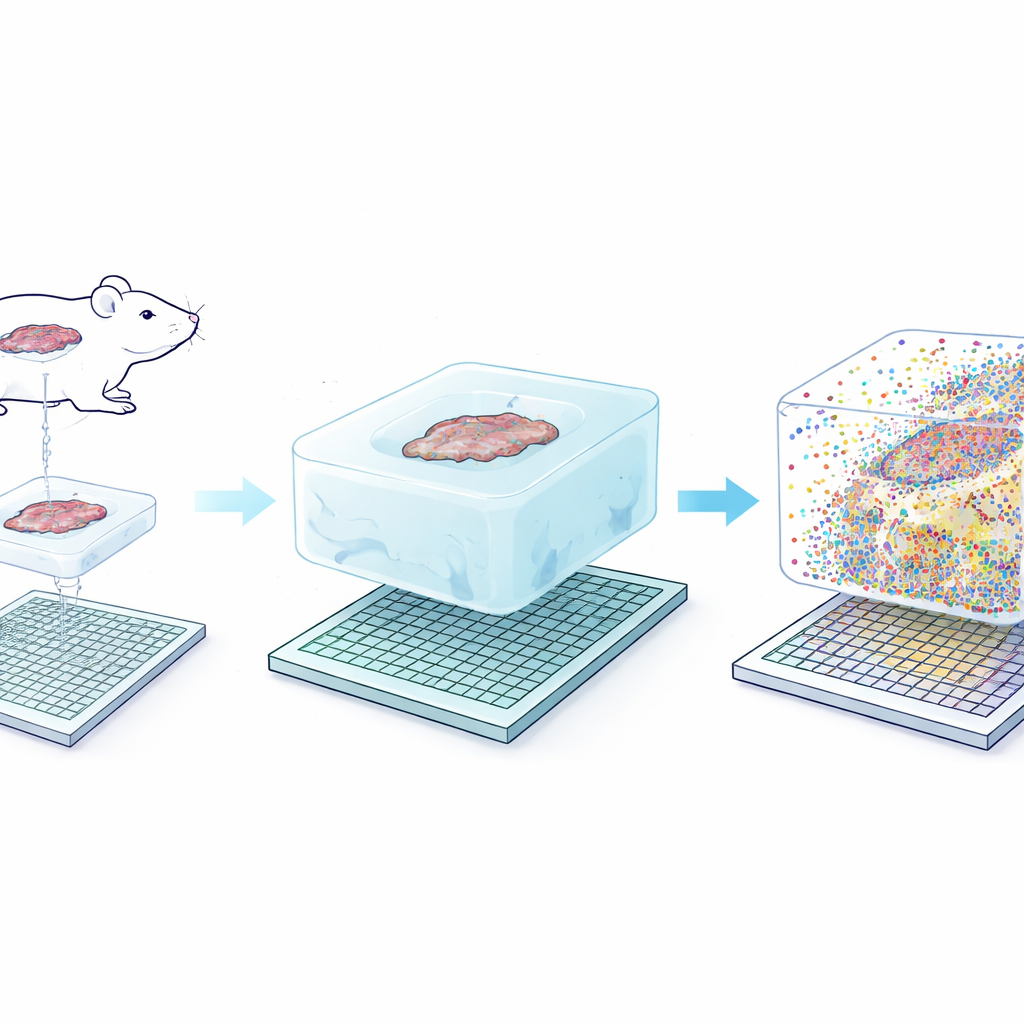
Från suddiga celler till subcellulära kartor
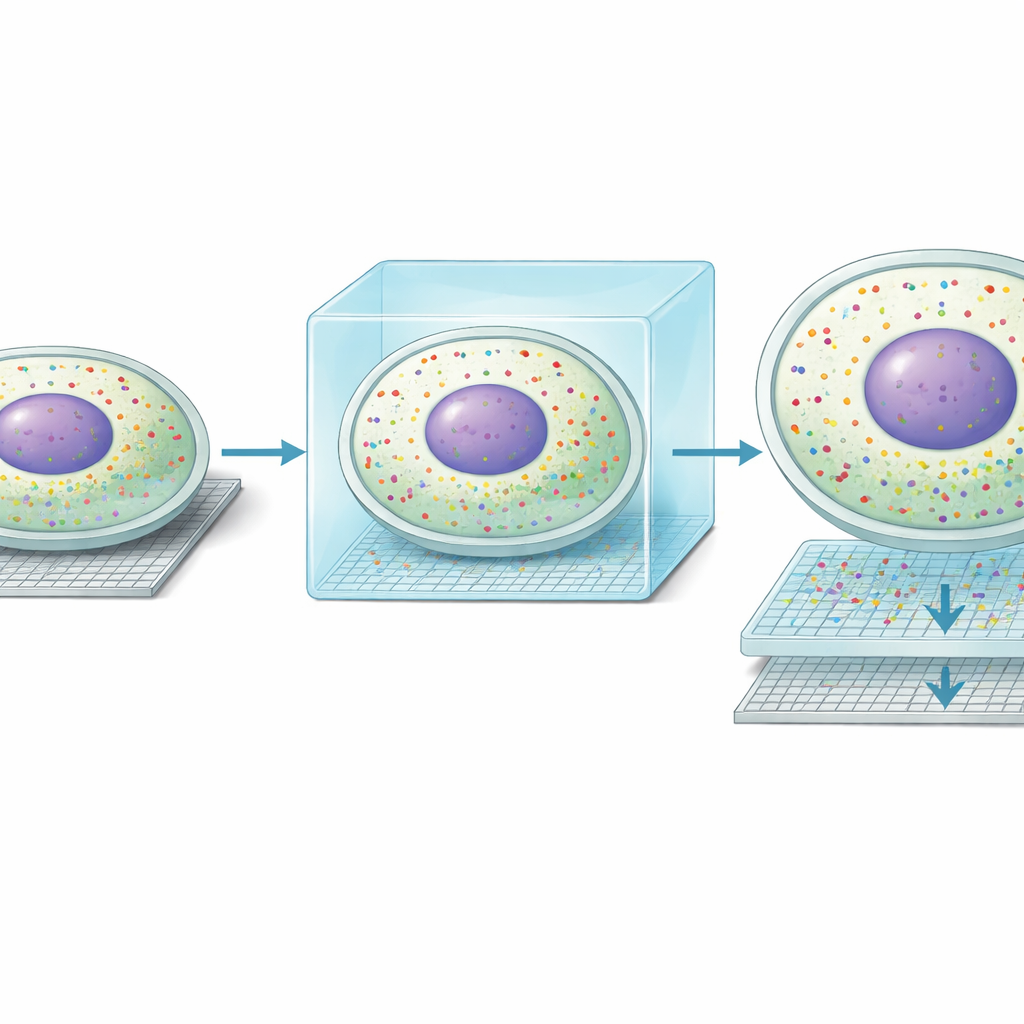
När forskarna tillämpade Seq-Scope-X på muslever fann de att metoden förbättrade den rumsliga upplösningen från ungefär 0,6 mikrometer till cirka 0,2 mikrometer och ökade antalet mätbara positioner per kvadratmillimeter med nästan en faktor tio. I praktiska termer kunde det som tidigare såg ut som suddiga klumpar av signaler nu avteckna skarpa konturer av enskilda celler. Ännu mer slående var att kluster av RNA som ännu inte fullständigt bearbetats (ointroniskt eller osplicerat) låg tätt kring kärnornas centra, medan moget RNA (splicerat) följde det omgivande cytoplasman. Detta gjorde det möjligt för författarna att rita cellgränser med hjälp av enbart RNA och att separera nukleära och cytoplasmatiska genavläsningar för nästan varje hepatocyt i vävnaden — något tidigare sekvenseringsbaserade metoder bara kunnat ana.
Cellers delade personligheter
Med denna nya klarhet upptäckte teamet en oväntad form av molekylärt ”dubbelliv” inne i levercellerna. Längs den välkända gradienten från blodkärl vid den portala sidan av leverlobulen till dem vid den centrala sidan specialiserar sig hepatocyter på olika metaboliska uppgifter. Seq-Scope-X visade att i många celler stämde inte mönstret av gener i kärnan överens med mönstret i den omgivande cytoplasman. Ungefär en tredjedel av hepatocyterna verkade ha en nukleär profil som låg i linje med en zon medan cytoplasmatiska profilen stämde med en intilliggande zon. Oberoende bildbaserade metoder, inklusive MERFISH och singelmolekylära RNA-fluorescensassays, bekräftade att individuella transkript kan vara koncentrerade antingen i kärnan eller i cytoplasman. Tillsammans tyder dessa observationer på att hepatocyter dynamiskt kan skifta sina metaboliska roller över tid, där kärnan förbereder för ett framtida tillstånd medan cytoplasman speglar det aktuella.
Bortom levern: hjärna, tarm och immunt vävnad
Författarna testade därefter om Seq-Scope-X fungerar i andra organ. I hjärnan separerade metoden tydligt olika neuron- och stödcellstyper och avslöjade subcellulära RNA-mönster runt kärnorna. I tjocktarmen löste den ut distinkta undergrupper av bägarceller och lager av kolonocyter längs krypta-till-yta-axeln, återigen med fångade nukleära signaturer. Kanske mest dramatiskt anpassade teamet metoden till proteiner genom att använda DNA-barcodade antikroppar i musens mjälte och mänskliga tonsiller. Seq-Scope-X kunde samtidigt kartlägga över ett hundra olika ytmolekylära markörer på single-cell-nivå och särskilja tätt packade T- och B-cellssubtyper samt myeloida celler. Genom att byta till en mer expanderbar gelkemi pressade de den effektiva upplösningen mot det verkliga nanoskalet, samtidigt som vävnadsarkitekturen bevarades tillräckligt för detaljerad kartläggning.
Vad detta betyder framöver
Seq-Scope-X visar att fysisk förstoring av vävnader före sekvensering kan övervinna långvariga upplösningsgränser och leverera nästan mikroskopisk detalj samtidigt som tusentals gener eller proteintaggar läses ut på en gång. För en allmän observatör innebär detta att forskare nu kan bygga ”molekylära atlaser” som inte bara visar var celler är, utan också vad som pågår i olika delar av varje cell. Sådana kartor kan hjälpa till att förklara hur vävnader svarar på skada, hur immunceller organiserar sig i lymfoida organ och tumörer, eller hur subtila skiftningar inne i celler förebådar sjukdom. Även om vidare förbättringar behövs för att skala upp täckningen och förbättra vissa färgningspaneler, öppnar Seq-Scope-X ett kraftfullt nytt fönster mot de mikroskopiska landskap som ligger till grund för hälsa och sjukdom.
Citering: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Nyckelord: rumslig transkriptomik, vävnadsexpansion, single-cell omik, rumslig proteomik, leverzonering