Clear Sky Science · sv
CD38 bryter ner MAVS genom mitofagi för att hämma frisättning av typ I-interferon i nasofarynxcancer‑celler och försämrar CD8+T‑cellsmedierad antitumörimmunitet
Varför detta är viktigt för cancerbehandling
Nasofarynxcancer är en tumör som uppstår bakom näsan och är särskilt vanlig i Öst‑ och Sydostasien. Immunbaserade läkemedel som frigör kroppens egna T‑celler har förändrat prognosen för vissa patienter, men de flesta får fortfarande ingen nytta. Denna studie avslöjar en dold broms inne i tumörcellerna själva: ett molekylärt protein kallat CD38 som tyst stänger av ett internt larmsystem och försvagar attacken från cancer‑dödande CD8‑T‑celler. Att förstå och inaktivera denna broms kan göra befintliga immunterapier effektiva för många fler människor.
En dold strömbrytare på tumörceller
Forskarna fokuserade på CD38, ett protein som finns på många immunceller men även uttrycks på nasofarynxcancerceller. Tidigare arbete hade kopplat CD38 till resistens mot populära checkpoint‑läkemedel som riktar sig mot PD‑1 och PD‑L1. Här undrade teamet om CD38 inne i tumörcellerna direkt förändrar hur väl CD8‑T‑celler kan känna igen och förstöra dessa celler. Genom att odla humana tumörceller med eller utan CD38 tillsammans med aktiverade humana CD8‑T‑celler fann de att borttag av CD38 från cancercellerna gjorde T‑cellerna mycket kraftfullare: de utsöndrade högre nivåer av viktiga attackmolekyler, överlevde bättre och dödade fler tumörceller. När CD38 sattes tillbaka sjönk T‑cellsfunktionen, vilket pekar på CD38 som en tumörintrinsisk hämmare av immunattacken.
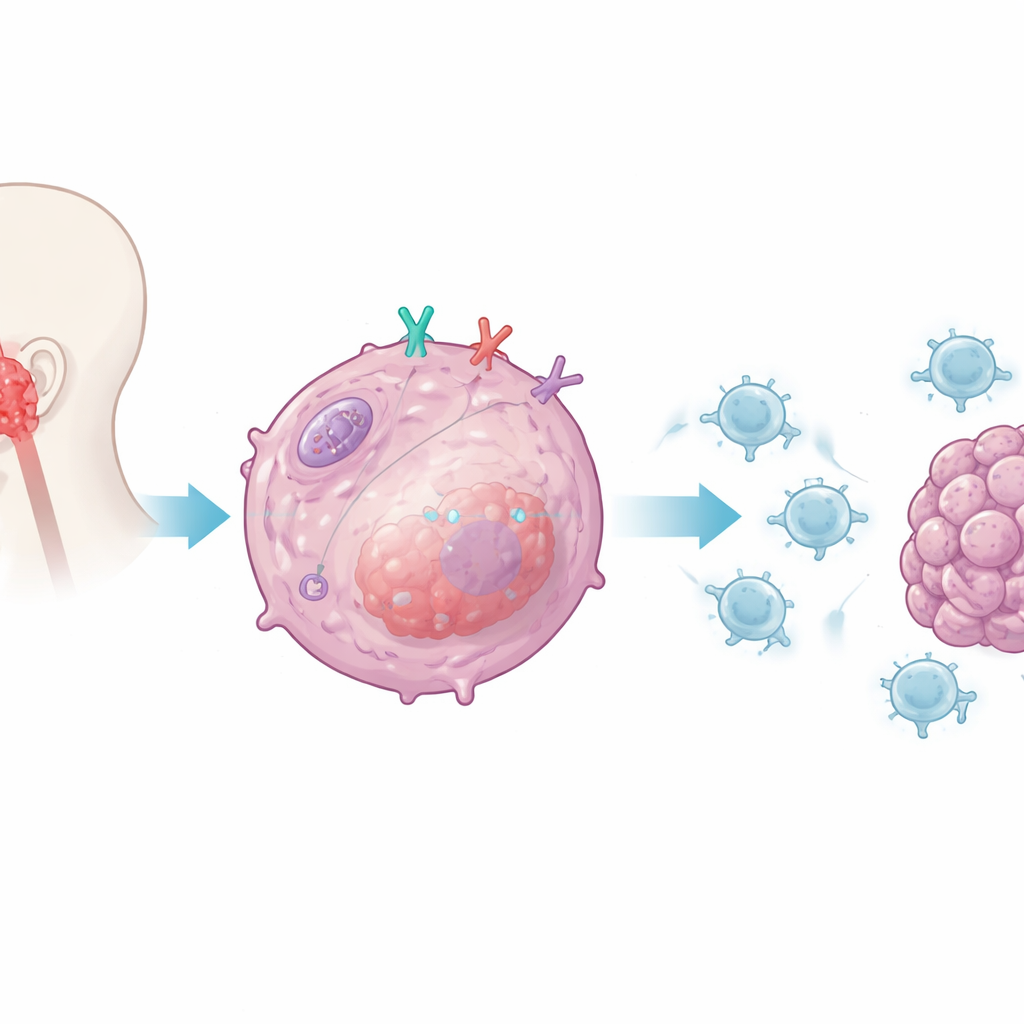
Att dämpa cellens interna alarm
Teamet undersökte sedan hur CD38 sänder denna hämmande signal. De koncentrerade sig på tumörcellens medfödda larmsystem, som normalt upptäcker virusliknande genetiskt material och utlöser typ I‑interferoner—potenta immunstimulerande budbärare. I tumörceller utan CD38 observerade forskarna en stark ökning av interferon‑beta och av kemokiner som lockar CD8‑T‑celler in i tumörer. De visade att CD38 selektivt dämpar den väg som kontrolleras av den interna sensorn RIG‑I och dess adapterprotein MAVS, som sitter på mitokondrierna, cellens energifabriker. När CD38 var närvarande försvagades aktiveringen av denna väg och dess nedströmssignalering; när CD38 togs bort ökade signaleringen och interferonproduktionen kraftigt, vilket ökade tumörens synlighet för immunsystemet.
Hur CD38 förstör en viktig signalhub
Vid en närmare granskning fann forskarna att CD38 fysiskt associerar med MAVS på mitokondrier och stör MAVS:s samarbete med RIG‑I, vilket försvagar signalöverföringen. Än mer anmärkningsvärt var att högre nivåer av CD38 ledde till en minskning av MAVS‑protein utan att ändra dess genetiska mall, vilket tyder på aktiv nedbrytning. Tester med olika hämmare visade att denna förlust var beroende av cellens återvinningsmaskineri, känt som autophagi, och specifikt av en form som riktar sig mot mitokondrier. CD38 ökade markörer för mitokondriell "självätning", minskade flera mitokondriella proteiner och främjade paketering av MAVS i autophagosomstrukturer som senare bryts ner. Blockering av mitokondriell autophagi bevarade MAVS och återställde interferonsignaleringen, vilket indikerar att CD38 tystar alarmet genom att föra MAVS in i cellens avfallsström.
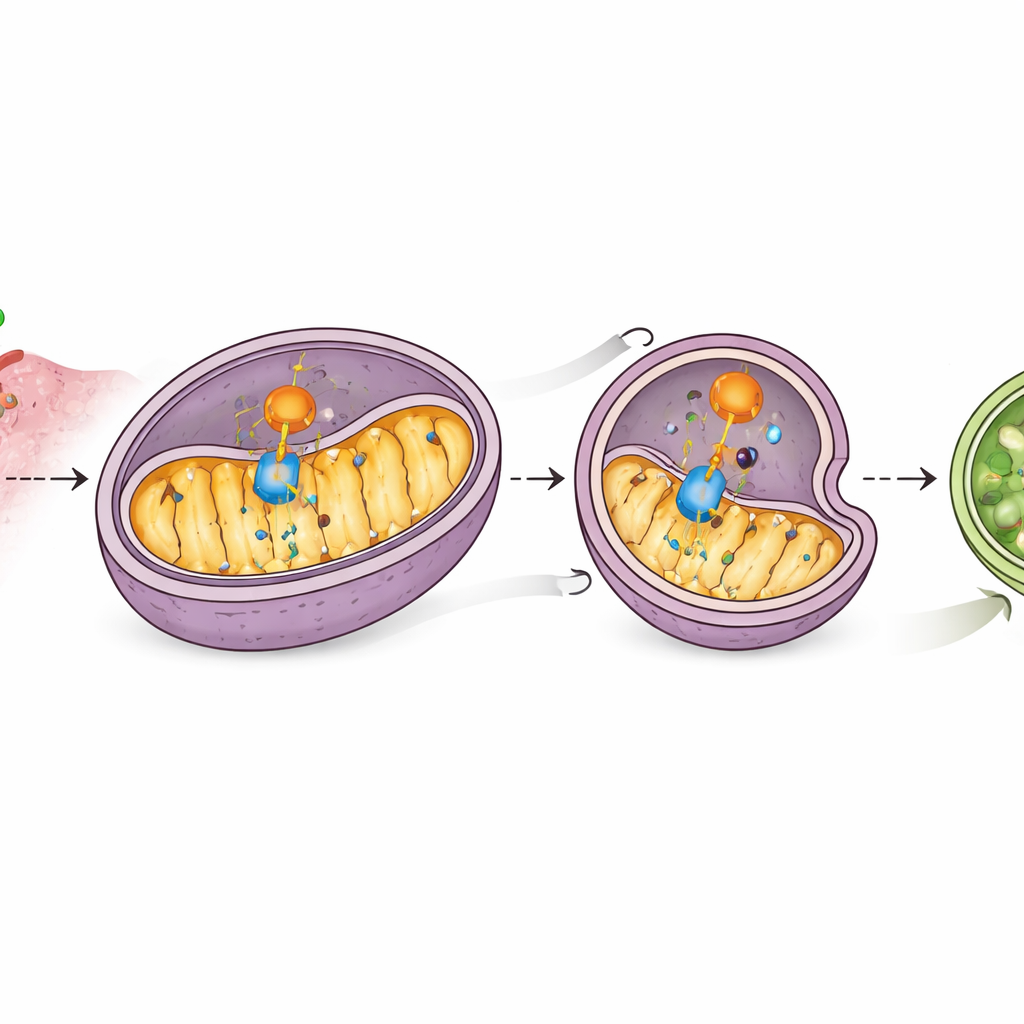
En hjälpare som styr mitokondrier till självförstörelse
Studien identifierade en annan aktör, PHB2, ett protein inne i mitokondrier som fungerar som en receptor för målinriktad mitokondriell borttagning. Masspektrometri och bindningsexperiment visade att CD38 interagerar med PHB2 och ökar PHB2:s närvaro i mitokondrier, där PHB2 i sin tur rekryterar den centrala autophagimaskineriet. PHB2 binder också MAVS, och CD38 fördjupar denna kontakt. När PHB2 reducerades kunde CD38 inte längre effektivt utlösa mitokondriell autophagi, MAVS‑nivåerna återhämtade sig och interferonrelaterade gener reaktiverades. Detta avslöjar en händelsekedja: CD38 engagerar PHB2, PHB2 engagerar MAVS, och tillsammans för de MAVS till mitokondrier avsedda för nedbrytning, vilket tystar interferon‑alarmet.
Bevis från djurmodeller
För att testa effekten i levande organismer använde forskarna muse‑tumörer konstruerade att sakna CD38. I immunkompetenta möss växte dessa tumörer långsammare, innehöll fler CD8‑T‑celler och hade en högre andel celler som producerade interferon‑gamma, ett kännetecken för aktiva antitumörsvar. Blockering av receptorn för typ I‑interferoner avlägsnade denna fördel och bekräftade att interferonsignalering är avgörande för den förbättrade immuniteten. I humaniserade möss med nasofarynxtumörer saktade minskad CD38 också tillväxten och ökade CD8‑T‑cellsinfiltrationen, men denna fördel försvann när även MAVS reducerades i tumörcellerna. Dessa in vivo‑fynd stärker idén att CD38–PHB2–MAVS‑axeln inne i tumörceller formar styrkan i kroppens T‑cellssvar.
Vad detta betyder för framtida terapier
Sammanfattningsvis visar arbetet att CD38 i nasofarynxcancerceller fungerar som en intern sabotör av antitumörimmunitet. Genom att driva en selektiv form av mitokondriell återvinning tömmer CD38 MAVS, försvagar produktionen av typ I‑interferon, sänker antigenpresentationen och dämpar slutligen CD8‑T‑cellsattacken. Nuvarande CD38‑blockerande föreningar riktar sig mest mot dess enzymaktiviteter och tar inte bort proteinet eller återställer MAVS. Författarna argumenterar för att nya strategier som syftar till att minska CD38‑nivåer eller störa dess samarbete med PHB2 eller MAVS skulle kunna återväcka interferon‑alarmet inne i tumörer. I kombination med befintliga checkpoint‑hämmare kan sådana angreppssätt göra fler nasofarynxcancer—och potentiellt andra—tumörer från immun‑kalla till immun‑responsiva.
Citering: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
Nyckelord: nasofarynxcancer, tumörimmunoterapi, typ I‑interferon, CD8 T‑celler, mitofagi