Clear Sky Science · sv
Benchmarking av EGF-signalvägen med fosfoproteomik och kinas-substratinteraktioner
Varför detta spelar roll bortom laboratoriet
Våra celler lyssnar ständigt och reagerar på signaler från sin omgivning. En av de viktigaste av dessa signaler är epidermal tillväxtfaktor (EGF), som hjälper till att kontrollera hur celler växer, delar sig och överlever. När detta kommunikationssystem fungerar fel kan det driva fram cancer och andra sjukdomar. Denna studie ställer en bedrägligt enkel fråga med stora konsekvenser: om vi använder dagens kraftfulla mättekniker och datorbaserade modeller, hur mycket bättre kan vi egentligen förstå EGF-signalvägen jämfört med vad som visas i läroboksdiagram?
Från raka linjer till verkliga kopplingsscheman
Traditionella ”signalvägar” ritas ofta som prydliga, nästan linjära kedjor av proteiner som för ett meddelande från cellens yta till kärnan. De kartorna byggdes upp under årtionden med långsamma, riktade experiment som bara kunde studera ett fåtal proteiner åt gången. Författarna hävdar att detta lämnat oss med en snäv, gatlykteliknande bild: vi vet mycket om de få proteiner som var lätta att studera, men betydligt mindre om det bredare nätverk av kopplingar som sannolikt finns i verkliga celler.
Lyssna på tusentals molekylära switchar samtidigt
För att gå bortom den begränsade bilden använde teamet fosfoproteomik, en masspektrometriteknik som kan spåra tiotusentals små kemiska märken kallade fosfatgrupper på proteiner i ett enda experiment. Dessa märken sätts dit av enzymer kallade kinaser och fungerar som snabba på/av-strömbrytare för signalering. Forskarna satte först ihop de mest omfattande ”vem-kan-fosforylera-vem”-kartorna hittills genom att slå samman tre typer av information: kuraterade fynd från litteraturen, prediktioner från en artificiell intelligens-modell som läser proteinsekvenser, och stora experimentella skärmar av kinaspreferenser. Detta utökade täckningen av kända eller misstänkta kinas–substrat-relationer från ungefär 5 % av mätbara platser till så mycket som 70–80 %.
Stresstesta EGF-signalering över många experiment
Nästa steg var att fokusera på EGF-responsen, en klassisk väg som är en huvudaktör i cancer i lungor, bröst, hud och hjärna. Gruppen kombinerade tre publicerade toppmoderna dataset med tre nya, mycket djupa tidsupplösta mätserier i njuravledda celler, plus två kontrollstudier där andra stimuli användes. Tillsammans mätte dessa experiment över 40 000 fosforyleringsplatser per dataset och följde hur de steg eller föll under minuterna efter EGF-stimulering. Även om de övergripande mönstren skiljde sig något mellan celltyper och tekniker, aktiverades nyckel-fosforyleringsplatser i EGF-vägen upprepade gånger, vilket bekräftar att kärnsignalen är robust även över olika experiment.
Återskapa den dolda konversationen mellan kinaser
Efter att ha härlett vilka kinaser som blev mer eller mindre aktiva försökte författarna sedan återskapa den underliggande ”konversationen” mellan dem: vilka kinaser som sannolikt aktiverar eller påverkar andra. De omvandlade sina kinas–substrat-kartor till kinas–kinas-nätverk och tillämpade tre beräkningsstrategier, från enkla rankningsscheman till en mer komplex metod som tvingar fram ett resultat som liknar ett riktat träd rotat i EGF-receptorn. De jämförde de härledda vägarna med flera typer av ”sanningsunderlag”: en noggrant kuraterad EGF-karta från en databas, storskaliga experiment där enskilda kinaser överuttrycktes, och par av kinasplatser vars beteende var starkt korrelerat över tid.
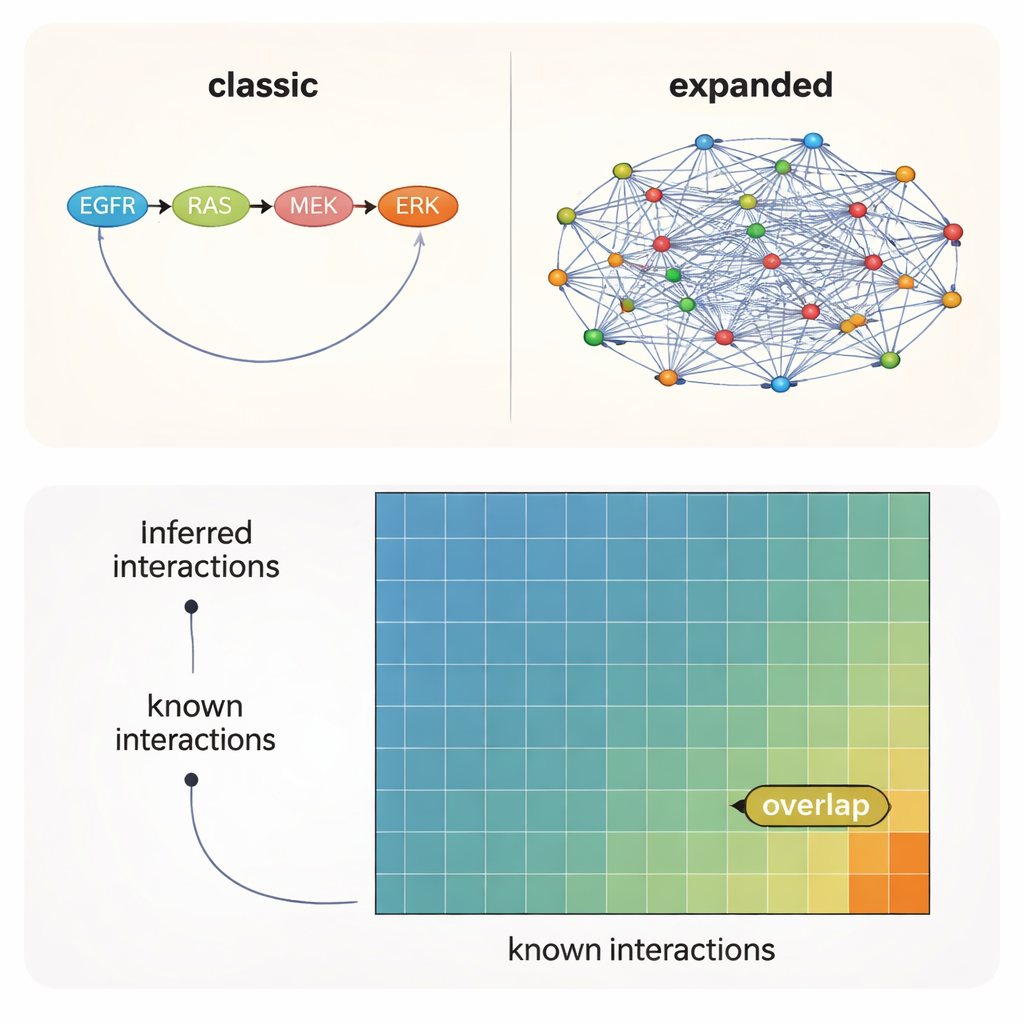
De mest plausibla länkarna ligger fortfarande utanför officiella kartor
Över alla tester var ett budskap tydligt: valet av förkunskap—vilket startnätverk du matar in i algoritmen—spelade större roll än den specifika metoden eller till och med det experimentella sammanhanget. Nätverk byggda från litteraturen återfann det största antalet kända interaktioner, medan bredare prediktiva resurser pekade på många ytterligare, plausibla kopplingar som ännu inte formellt dokumenterats. Även under de bästa förhållanden fanns dock endast cirka 10–12 % av interaktionerna som föreslogs av data och modeller med i någon av referenssatserna. Med andra ord ligger ungefär 90 % av de stödjade kinas–kinas-länkarna i okänt territorium.
Vad detta betyder för framtida behandlingar
För icke-specialister är slutsatsen att det välkända EGF-diagrammet i läroböcker sannolikt bara är toppen av isberget. Modern fosfoproteomik i kombination med avancerade beräkningsmetoder avslöjar ett mycket rikare och mer intrikat signalnätverk. Många av dessa nyföreslagna kopplingar kan representera förbisedda sätt som cancerceller omdirigerar signaler för att undkomma läkemedel, eller nya möjligheter att utforma smartare läkemedelskombinationer. Studien bevisar inte att varje ny länk är verklig, men den ger en färdplan och öppna verktyg för forskare att testa dessa idéer, med målet att slutligen nå mer precisa och effektiva behandlingar i sjukdomar där EGF-signalering spelar en central roll.
Citering: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Nyckelord: EGF-signalering, fosfoproteomik, proteinkinaser, cellsignalnätverk, cancerbiologi