Clear Sky Science · sv
Mycobacterium tuberculosis modulerar fosforylering av värdens ATP6V1E1 för att främja intracellulär överlevnad
Varför detta är viktigt för att bekämpa tuberkulos
Tuberkulos är fortfarande en av världens dödligaste infektionssjukdomar och dödar mer än en miljon människor varje år. Våra immunceller är utrustade med kraftfulla ”sura återvinningskärl” som normalt smälter ner invaderande mikrober. Denna artikel avslöjar hur tuberkelbakterien, Mycobacterium tuberculosis (Mtb), saboterar det surhetsreglerande systemet inne i våra celler, och visar att ett läkemedel riktat mot detta knep kan hjälpa infekterade djur att rensa infektionen mer effektivt.
Cellens syrabad för mikrober
När tuberkelbakterier inhaleras till lungorna tas de snabbt upp av immunceller som kallas makrofager. Bakterierna hamnar i membranblåsor som normalt ska fusionera med lysosomer — små säckar fyllda med matsmältningsenzymer som fungerar bäst i en starkt sur miljö. Denna surhet skapas av en molekylär pump, vakuolär ATPas (V-ATPase), som använder cellens energi för att pressa protoner in i lysosomerna och sänka det inre pH-värdet. Korrekt acidifiering är avgörande för att bryta ner Mtb, men decennier av forskning har visat att denna patogen på något sätt håller sina compartment mindre sura och överlever.
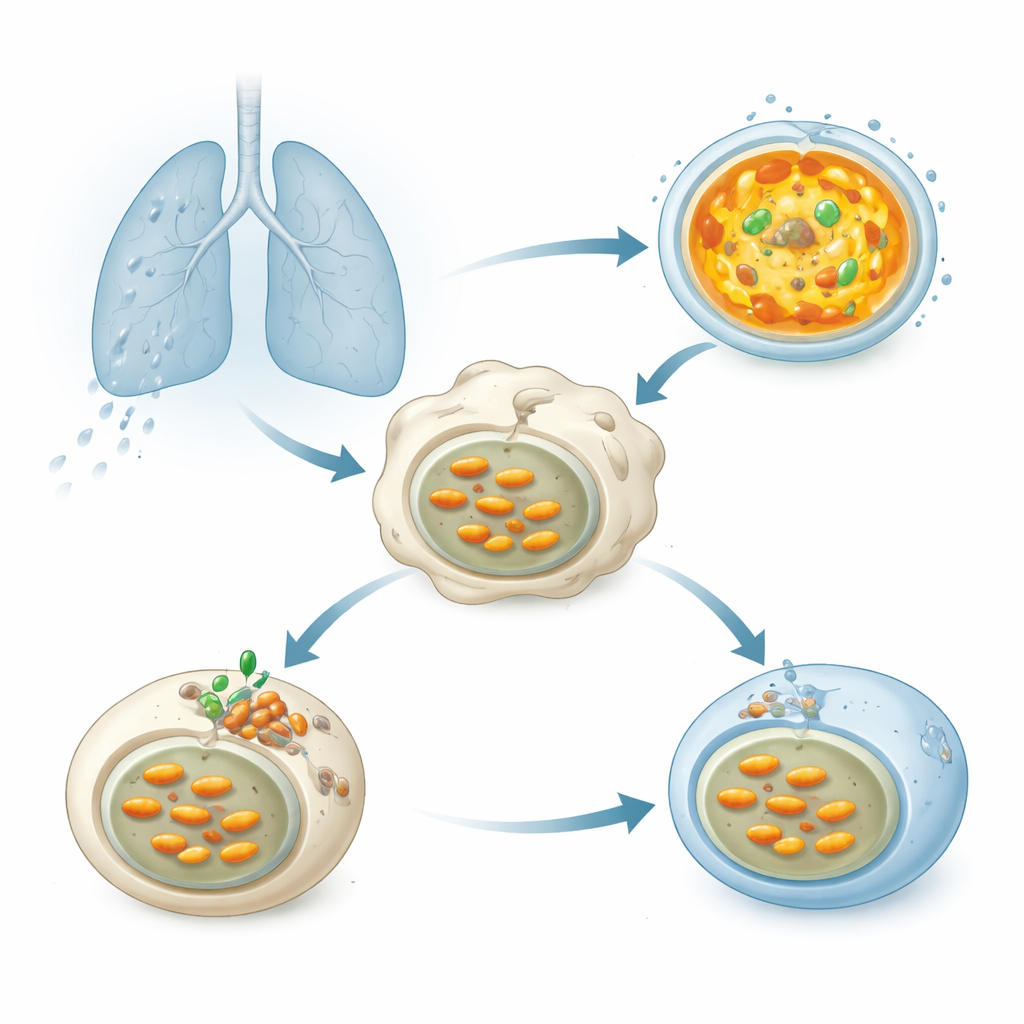
En hemlig bakteriell hjälpare som blockerar försurningen
Forskarna screenade mer än 200 proteiner som Mtb kan frisätta för att se vilka som försvagar lysosomal försurning i humana celler. Ett protein stack ut: ett enzym kallat Chp2 (även känt som Rv1184). När celler producerade Chp2 gav deras lysosomer svagare signal med syrakänsliga färgämnen, vilket indikerar ett högre, mindre fientligt pH. Mtb-stammar som förändrats så att de saknar Chp2 undertryckte inte längre försurningen; i infekterade makrofager och i möss rensades dessa mutanta bakterier bort mer effektivt och orsakade mindre allvarliga lungsjukdomar. Återinförande av Chp2 i den mutanta stammen återställde både blockaden av försurning och den högre bakteriebördan, vilket identifierar Chp2 som en virulensfaktor som hjälper Mtb att bestå inne i värdceller.
Värdpumpens subenhet som fungerar som en brytare
För att förstå hur Chp2 stör försurningen sökte teamet efter värdkomponenter som den kan binda till. De fann att Chp2 direkt fäster vid en specifik del av V-ATPasen, en subenhet kallad ATP6V1E1 (förkortat E1), som hjälper till att stabilisera pumpens struktur. Ökad mängd E1 i celler stärkte lysosomal försurning och gjorde det svårare för Mtb att överleva, medan minskad E1 gav motsatt effekt. Möss som bara bar en fungerande kopia av E1-genen hade mindre sura lysosomer, högre bakterieladdningar i sina lungor och mer omfattande vävnadsskador efter infektion, vilket visar att E1 är en viktig värdförsvarare mot tuberkulos.
En kinas-tagg på pumpen som sänker syran
Författarna undersökte sedan om kemiska ”taggar” på E1 kan reglera pumpens aktivitet. De upptäckte att tillsättning av fosfatgrupper till två specifika tyrosiner (Tyr56 och Tyr57) på E1 fungerar som en broms: att efterlikna fosforylering minskade försurningen och hindrade fullständig sammansättning av V-ATPasen, medan att förhindra fosforylering gav motsatt effekt. Genom att screena en panel av enzymer identifierade de en kinas kallad BMX som värdproteinet som sätter denna tagg. När BMX blockerades genetiskt eller med en litenmolekylär inhibitor sjönk E1-fosforyleringen, pumpen monterades mer effektivt på lysosomala membran, lysosomerna blev surare och Mtb-överlevnaden i makrofager minskade.
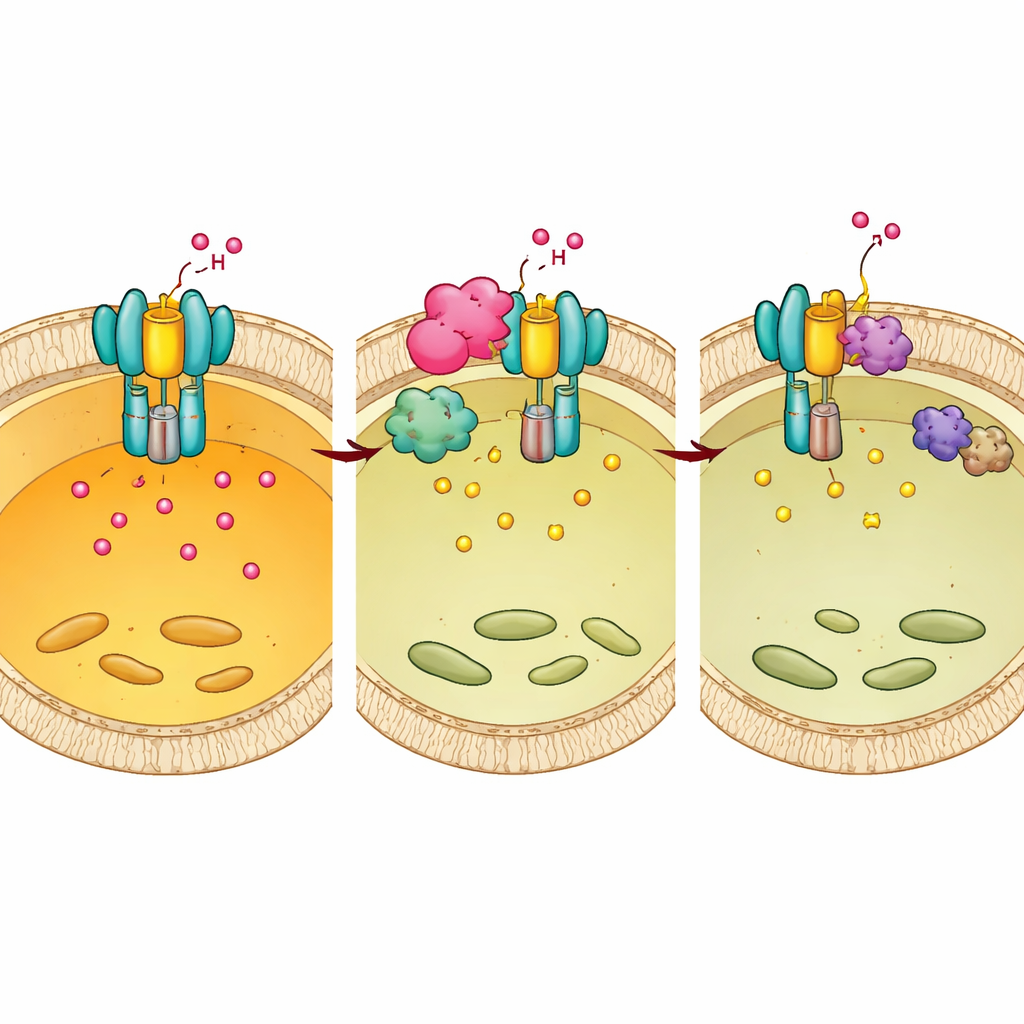
Hur Mtb kopplar om värdens brytare till sin fördel
Chp2 och BMX visade sig samarbeta. Strukturella och biokemiska experiment visade att Chp2 fungerar som ett skelett som för E1 och BMX i nära kontakt på lysosomal yta, vilket förstärker E1-fosforylering vid Tyr56/57. Denna extra märkning stör fullständig pumpmontering, höjer lysosomal pH och skapar en mildare miljö där Mtb kan bestå. När BMX hämmas försvann den överlevnadsfördel som Chp2 gav, både i odlade celler och i infekterade möss. Viktigt är att behandling av möss med BMX-inhibitorn efter infektion minskade bakterieladdningar och lungpatologi hos normala djur, men inte hos möss med försvagat E1, vilket indikerar att läkemedlet verkar genom att återställa effektiv E1-driven försurning.
Att omvandla patogenens trick till en behandlingsidé
Enkelt uttryckt visar denna studie att tuberkelbakterier smugglar in ett hjälpprotein i våra celler som stör ”syrapumpen” i avfallshanteringen och dämpar den så att mikroberna kan överleva. Genom att identifiera pumpens subenhet som fungerar som huvudreglage (E1) och värdens enzym som vrider på den (BMX) avslöjar författarna en exakt punkt där ett läkemedel kan ingripa. Inhibering av BMX hos möss återaktiverar effektivt cellens interna syrabad och förbättrar bakterierens rensning. Dessa fynd öppnar för värdriktade terapier som gör våra egna celler mer fientliga mot Mtb, potentiellt i kombination med antibiotika och till hjälp mot läkemedelsresistent tuberkulos.
Citering: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Nyckelord: tuberkulos, lysosomer, värdriktad terapi, Mycobacterium tuberculosis, V-ATPase