Clear Sky Science · sv
En 3D tarm-hjärna-kärl-plattform för tvåvägskommunikation i tarm-neuropatogenes
Varför din tarm kan vara viktig för din hjärna
Idén att "du är vad du äter" har fått en ny nyans: växande bevis tyder på att vad som händer i din tarm kan påverka din hjärnas hälsa. Denna artikel presenterar en avancerad laboratoriemodell som kopplar ihop miniatyrversioner av mänsklig tarm, blodkärl och hjärnvävnad på ett enda chip. Genom att följa hur signaler rör sig längs denna lilla motorväg undersöker forskarna hur problem i tarmen kan utlösa hjärnsjukdomar som Alzheimers och Parkinsons — och hur hjärnproblem i sin tur kan sända varningssignaler tillbaka mot tarmen.
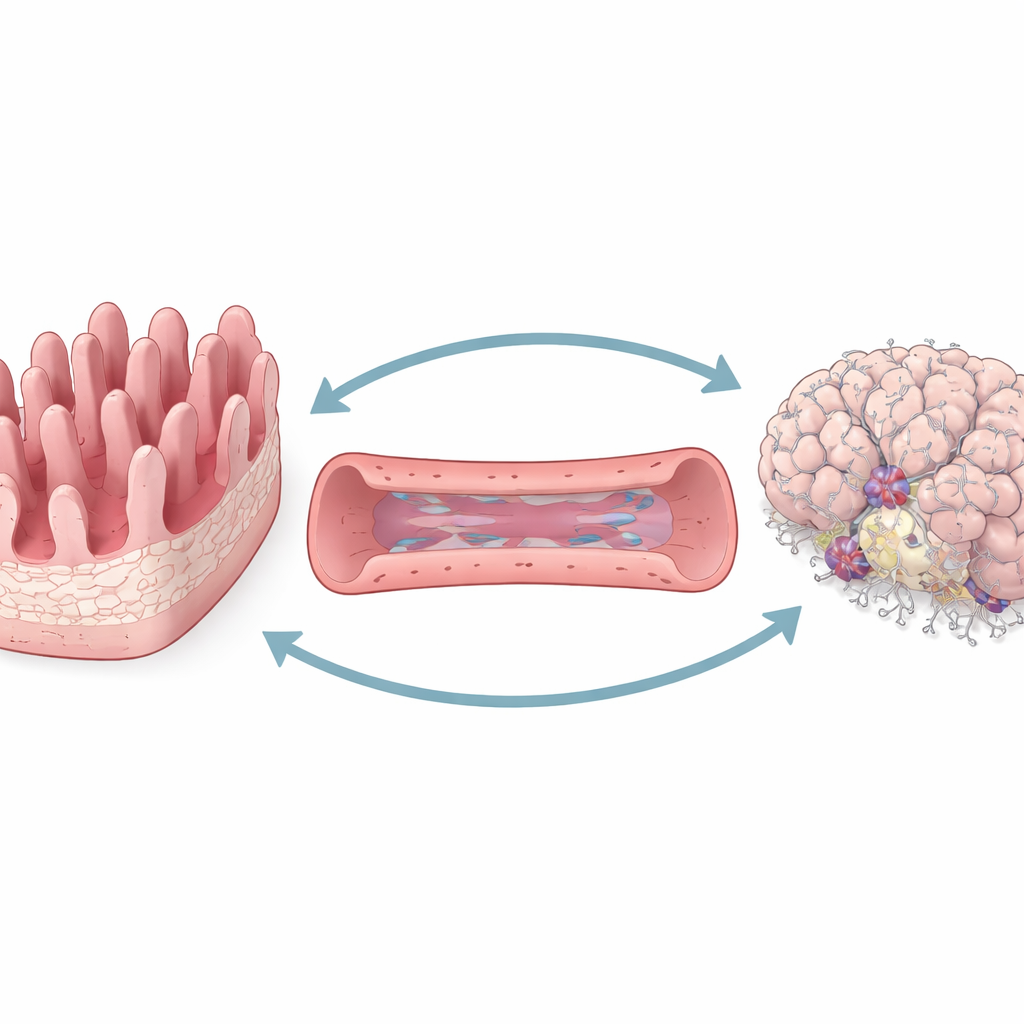
Att bygga en minikropp på ett chip
För att studera tarm–hjärnkommunikation på ett kontrollerat sätt konstruerade teamet en trefaldig "organ-on-a-chip"-plattform. Ett fack efterliknar tarmens inre yta, komplett med fingerlika utskott som bildar en barriär mellan tarminnehållet och resten av kroppen. Ett andra fack representerar blodkärl beklädda med kärlceller som liknar dem i hjärnan. Det tredje rymmer levande mänskliga neuroner och stödjeceller arrangerade för att likna en liten bit hjärnvävnad. Vätska kan flöda mellan dessa fack, vilket tillåter molekyler att färdas ungefär som de skulle göra genom cirkulationen i kroppen.
Att få modellen att uppföra sig som verklig vävnad
Chippet är utformat så att cellerna utsätts för ett milt, gungande flöde i stället för att stå still i en statisk skål. Denna rörelse uppmuntrar tarmlagret att utveckla tjockare, mer realistiska veck och tätare förbindelser mellan cellerna, vilket gör det mindre läckande. Kärllagret svarar genom att töja ut sig i flödets riktning, ett kännetecken för friska blodkärl, och visar stark barriärfunktion mot stora molekyler. I hjärnafacket bildar neuroner aktiva nätverk som sänder rytmiska kalciumsignaler, ett tecken på elektrisk aktivitet, medan stödjeceller omsluter närliggande kärl precis som i verklig hjärnvävnad. Tillsammans visar dessa egenskaper att de tre regionerna beter sig mer som de gör inne i kroppen än i traditionella platta cellkulturer.
När tarmirritanter utlöser problem i hjärnan
För att modellera tarmdrivna sjukdomar tillsatte forskarna bakteriella produkter — antingen material insamlat från E. coli-kulturer eller ett renat toxin kallat LPS — på tarmsidan av chippet. Dessa stimuli försvagade tarmbarriären, vilket tillät fler stora molekyler och bakteriella spår att slinka igenom till kärlfacket och sedan vidare till hjärnafacket. När läckaget ökade blev kärlväggen mindre tät, och stjärnformade stödjeceller i hjärnan gick över i ett reaktivt, alarmt tillstånd. I den hjärnliknande vävnaden ackumulerades skadliga proteinedelar kopplade till Alzheimers och Parkinsons, skyddande förbindelser mellan neuroner minskade och inflammatoriska signaler sköt i höjden. Denna sekvens, som börjar med en störd tarm och slutar med stressade hjärnceller, speglar mönster som ses i djurstudier och hos patienter.
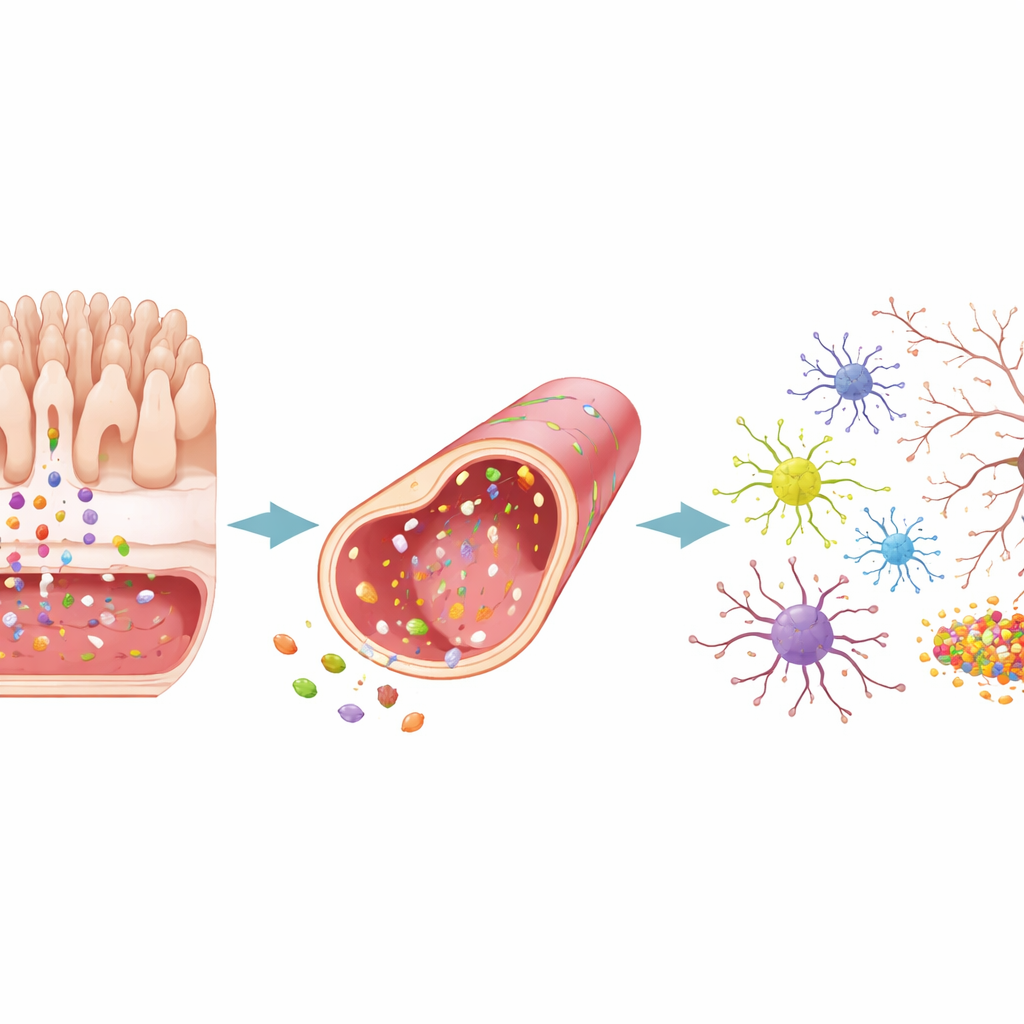
När hjärnsjukdom skickar signaler tillbaka
Teamet vände sedan experimentets riktning. De skapade Alzheimerliknande förhållanden genom att konstruera hjärnceller på chippet som överproducerar klibbiga amyloidfragment, och Parkinsonliknande förhållanden genom att exponera dem för klumpar av proteinet α-synuklein. I båda scenarierna byggdes giftiga proteiner upp först i hjärnafacket och dök sedan upp i kärl- och tarmregionerna. Hjärnvävnaden släppte ut vågor av inflammatoriska molekyler, förlorade synaptiska kopplingar och visade andra kännetecken på degeneration. Dessa hjärnrelaterade farosignaler störde kraftigt kärllagret, lösgjorde dess barriär och aktiverade närliggande stödjeceller. Tarmlagret visade däremot endast måttliga strukturella förändringar: dess yta blev något förändrad och mer "aktiverad", men dess täta förbindelser höll till stora delar, och läckaget ökade bara marginellt.
Vad detta betyder för framtida behandlingar
I vardagstermer tyder detta chip på att en sjuk tarm kan driva hjärninflammation och skada mer direkt än en sjuk hjärna stör tarmen. Tarmbetingade bakteriella produkter och inflammation verkar kunna försvaga både kärl och hjärnvävnad, medan hjärnorsakad inflammation främst riktar sig mot blodkärlen och endast subtilt omformar tarmen. Eftersom hela systemet är byggt av mänskliga celler erbjuder det en lovande testbädd för terapier som syftar till att lugna tarminflammation, täta barriärer eller blockera spridning av skadliga proteiner. I slutändan kan plattformar som denna hjälpa läkare att avgöra vilka patienter som skulle ha mest nytta av tarmfokuserade strategier för att bromsa eller förebygga neurodegenerativa sjukdomar.
Citering: Tran, M., Jeong, H.W., An, M. et al. A 3D gut-brain-vascular platform for bidirectional crosstalk in gut-neuropathogenesis. Nat Commun 17, 2504 (2026). https://doi.org/10.1038/s41467-026-69318-y
Nyckelord: tarm-hjärnaxel, organ-på-en-chip, neuroinflammation, Alzheimers sjukdom, Parkinsons sjukdom