Clear Sky Science · sv
Preoptiskt kisspeptin-nNOS-GnRH (KiNG) neuronalt nätverk reglerar LH-rytmicitet genom aktivering–inhibering hos möss
Varför den här hjärnhistorien spelar roll för fertilitet
Ägglossning och fertilitet beror på en liten grupp hjärnceller som frisätter ett mästarhormon i pulser och ibland i stora toppar. När tidpunkten rubbas kan fortplantningen misslyckas. Denna studie visar hur två typer av signalsubstanser i musens hjärna — en som sätter igång aktivitet och en annan som tystare släcker av den igen — samarbetar för att forma dessa hormonrytmer. Att förstå denna dolda tidshållarkrets kan så småningom hjälpa till att förklara vissa former av infertilitet och föreslå nya sätt att behandla reproduktiva störningar.
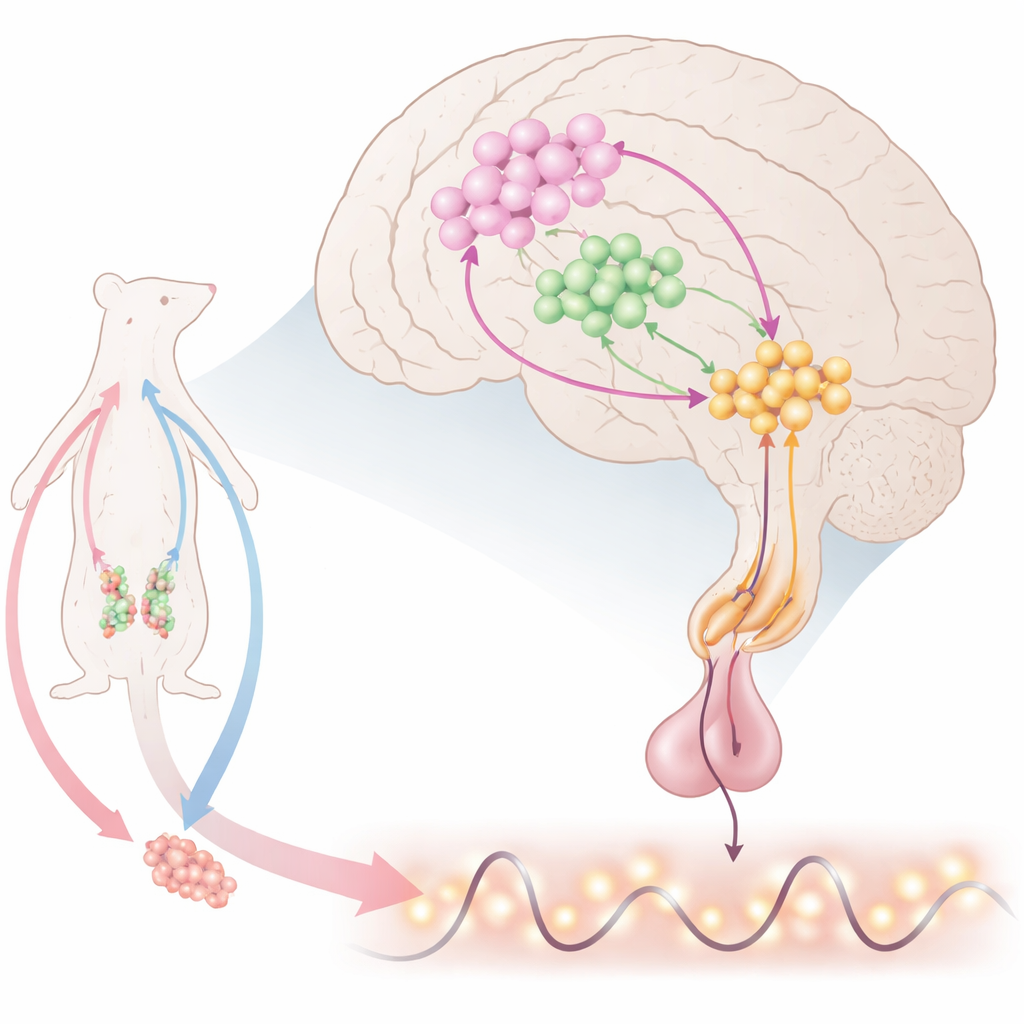
Hjärnans tidhållare för reproduktion
Djup inne i hjärnan släpper specialiserade nervceller ut gonadotropinfrisättande hormon (GnRH), som får hypofysen att frigöra luteiniserande hormon (LH) och follikelstimulerande hormon. Dessa styr i sin tur äggstockar och testiklar. GnRH flödar inte jämnt; istället uppträder det som regelbundna pulser och, hos honor, en stor för-ägglossningsvåg. Forskare vet att många signaler påverkar GnRH-celler, men den exakta kombinationen som ger både pulser och toppar har varit oklar. Detta arbete fokuserar på en liten region i fronten av hypothalamus, där GnRH-celler möter två andra viktiga aktörer: kisspeptinproducerande neuroner som exciterar GnRH, och neuroner som bildar kväveoxid (NO), en gasformig signal som kan diffundera korta sträckor.
Ett på/av-partnerskap mellan två signaler
Forskarna föreslår ett tredelat „KiNG”-nätverk, bestående av kisspeptin-, NO-producerande (nNOS)-neuroner och GnRH-celler. Kisspeptin är en stark aktivator som kan driva GnRH- och LH-frisättning, men konstant stimulering släcker faktiskt ner systemet, vilket antyder att en intern broms behövs. Genom att använda mycket känsliga molekylära prober, genetiska verktyg och hjärnskivinspelningar i möss visar teamet att kisspeptin gör mer än att direkt excitera GnRH-neuroner. Det aktiverar också närliggande nNOS-neuroner i preoptiska området, särskilt i en region kallad OV/MePO. När kisspeptinnivåerna stiger producerar dessa nNOS-celler pulser av NO, vilket triggar produktion av en sekundär budbärare, cGMP, i omgivande celler, inklusive GnRH-cellerna själva. Denna NO–cGMP-signal dämpar GnRH-avfyrning och utgör en inbyggd avstängningsknapp för kisspeptin-driven aktivitet.
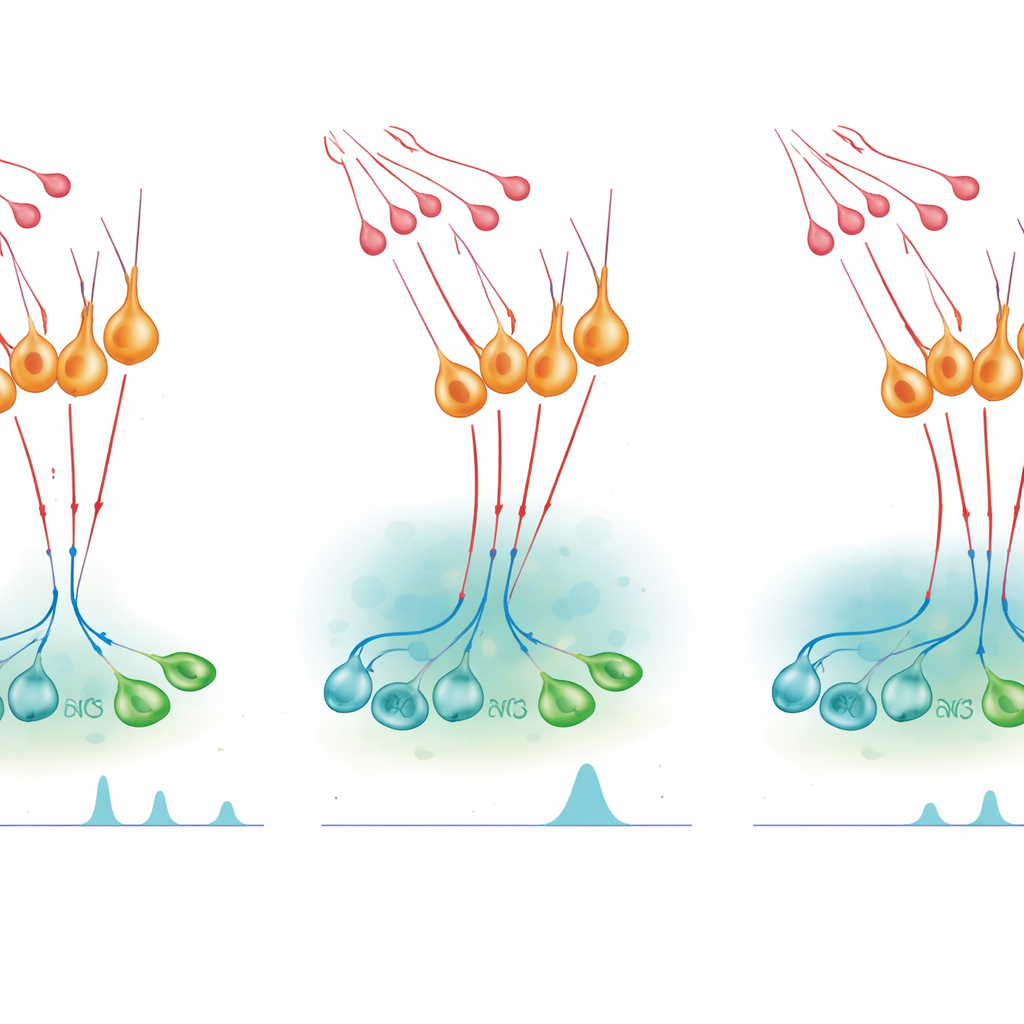
Att slå på hormontoppar och dämpa dem
För att testa hur denna mikrokrets påverkar hormonfrisättning använde teamet kemogenetiska strömbrytare — konstruerade receptorer som aktiveras av ett i övrigt inaktivt läkemedel — för att sätta på eller stänga av nNOS-neuroner i levande möss. Att konstgjort aktivera nNOS-celler under en normalt lugn fas i honans cykel räckte för att framkalla en toppliknande ökning av LH i blodet, och samma gällde hos hanar. Att blockera NO-produktion utsuddade denna effekt, vilket visar att NO från dessa neuroner är nödvändigt för toppen. Ändå, när forskarna hämmande nNOS-neuroner eller minskade deras känslighet för kisspeptin, gav en dos kisspeptin en överdriven och långvarig LH-ökning. Farmakologiska substanser som blockerar NO-syntes hade en liknande förstärkande effekt, medan ett läkemedel som förlänger cGMP-signaler kortade ner kisspeptinresponsen och minskade senare LH-frisättning. Tillsammans visar dessa experiment att NO både hjälper till att synkronisera GnRH-neuroner för att skapa toppar och begränsar hur länge kisspeptin kan hålla dem aktiva.
En flexibel rytm över ägglossningscykeln
Studien visar också att denna på/av-balans förändras över honans cykel. Med en känslig RNA-detekteringsmetod fann författarna att fler nNOS-neuroner uttrycker kisspeptinreceptorn dagen före ägglossning, när östrogennivåerna är höga och LH-toppen inträffar. Under de lugnare stadierna svarar färre nNOS-neuroner på kisspeptin och producerar endast små, lokala mängder NO som försiktigt hejdar GnRH-pulser utan att stoppa dem. På toppdagen ger starkare kisspeptininput och ökat receptoruttryck en massiv ökning av NO-produktion, vilket tillåter NO att sprida sig längre och tillfälligt tysta många GnRH-neuroner samtidigt. När NO-signalen avtar återhämtar sig dessa celler tillsammans och genererar den stora, samordnade LH-toppen som behövs för ägglossning.
Vad detta betyder för människors hälsa
Enkelt uttryckt visar detta arbete att samma signal som startar GnRH-neuroner — kisspeptin — också rekryterar ett fördröjt bromssystem via NO, vilket säkerställer att hormonutbrott blir starka men inte okontrollerade. KiNG-nätverket fungerar alltså både som gas och som broms för reproduktionens timing, finjusterar GnRH-pulser under större delen av cykeln och formar den topp som utlöser ägglossning. Eftersom genetiska förändringar i kisspeptin- och NO-vägar har upptäckts hos människor med reproduktionsproblem kan förståelsen av denna fint avvägda krets ge upphov till nya sätt att diagnosticera och behandla infertilitet och närliggande tillstånd.
Citering: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Nyckelord: reproduktionshormoner, hypothalamus, kisspeptin, kväveoxid, ägglossningstiming