Clear Sky Science · sv
Histonlactylering ökar CXCL1‑uttryck för neutrofilinfiltration och immunflykt vid bukspottkörtelcancer
Varför denna cancerstudie är viktig
Bukspottkörtelcancer är en av de dödligaste cancerformerna, delvis eftersom den ofta är motståndskraftig mot moderna immunterapier som fungerar i andra tumörer. Denna studie avslöjar hur bukspottkörteltumörer omprogrammerar sin egen socker‑metabolism för att tyst avväpna immunsystemet, och hur blockering av den processen kan återöppna en väg för kroppens försvar — och befintliga läkemedel — att slå tillbaka.
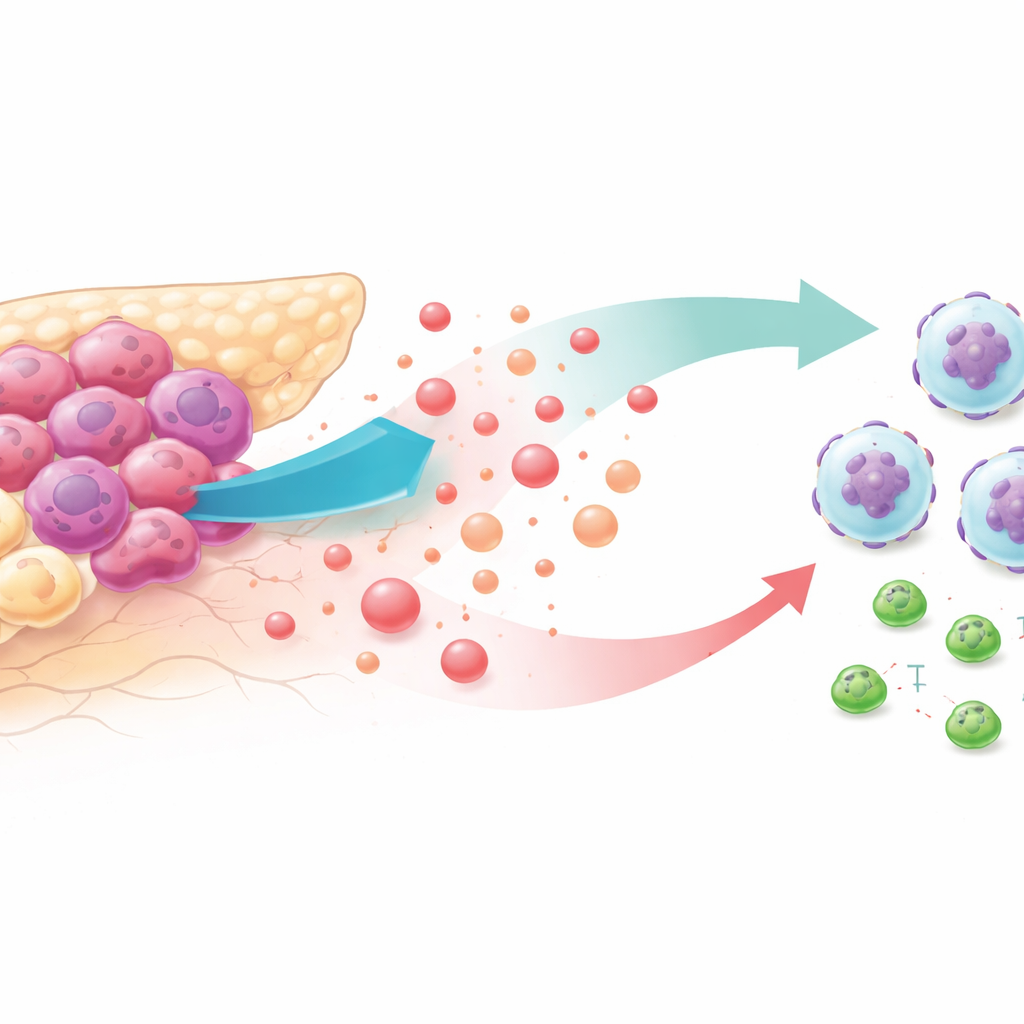
Sockerälskande tumörer och en fientlig omgivning
Cancerceller är ökända för att förbränna glukos i rasande takt, även när syre finns tillgängligt. Denna "högglykolytiska" livsstil översvämmar tumörens omgivning med laktat, en biprodukt som tidigare avfärdats som metabolt avfall. Genom att analysera patienttumördatabaser och musemodeller fann forskarna att bukspottkörtelcancer med intensiv glykolys var fyllda med neutrofiler — vita blodkroppar som i detta sammanhang hjälper tumörer att växa — och hade färre CD8‑T‑celler som dödar cancer. Patienter vars tumörer visade denna profil tenderade att leva kortare tid, vilket tyder på att förändrad metabolism och immunflykt hänger nära samman.
Hur tumörer använder laktat för att kalla in fel hjälp
För att förstå hur glykolys lockar till sig neutrofiler sänkte teamet tumörernas glykolys med läkemedel eller genetiska knep i bukspottkörtelcancercellinjer och möss. När sockernedbrytningen blockerades släppte tumörcellerna ut mycket mindre av en kemisk signal kallad CXCL1, och cirkulerande nivåer av denna signal sjönk i möss och i patientprover. I laboratoriemigreringsprov rörde sig neutrofiler villigt mot odlingsmedium från mycket glykolytiska cancerceller men inte mot medium från celler med hämmad glykolys — om inte forskarna tillsatte renat CXCL1. I levande möss återställde man neutrofilantalet och försvagade den antitumoreffekt som glykolyshämning gav genom att återinföra CXCL1 i tumörer med nedsatt glykolys.
En ny epigenetisk strömbrytare driven av laktat
Studien zoomade sedan in på nivån för DNA‑packning. Våra gener är lindade kring spolliknande proteiner kallade histoner, vars kemiska markeringar fungerar som på/av‑brytare för genaktivitet. Författarna visar att i bukspottkörtelcancer tillsätter laktat från glykolys en specifik "laktyl"‑markering på en histonposition, känd som H3K18. Denna modifiering, kallad histon H3K18‑lactylering, var märkbar högre i tumörvävnad än i normal pankreas. När glykolys blockerades föll lactyleringen vid H3K18, särskilt nära CXCL1‑genens kontrollregion, och CXCL1‑produktionen minskade. Återläggning av laktat återställde både histonmarkeringen och CXCL1‑uttrycket. I patientprover visade tumörer med mer H3K18‑lactylering också högre CXCL1, vilket kopplar detta molekylära märke till ett pro‑tumört immunlandskap.
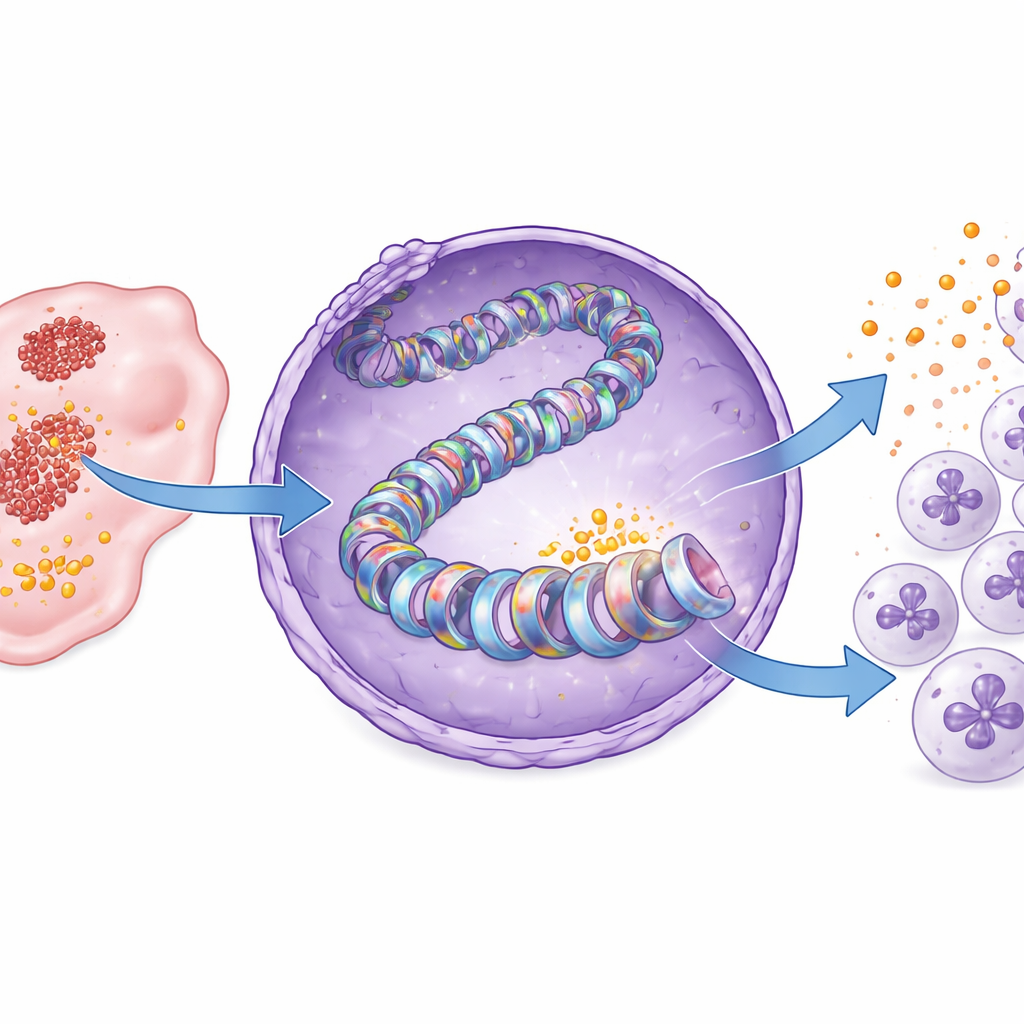
Identifiering av enzymet och en farmakologiskt angripbar svag punkt
Histonmarkeringar skrivs av specialiserade enzymer. Genom att screena inhibitorer mot kända histonmodifierande proteiner identifierade forskarna ett enzym kallat PCAF som en nyckelskrivare av H3K18‑lactyleringsmärket i bukspottkörtelcancer. Strukturell modellering föreslog att PCAF kan binda lactyl‑CoA, den aktiva formen av laktat som används för märkningen, och biokemiska tester bekräftade att renat PCAF direkt kan tillföra lactylgrupper till histon H3. Blockering av PCAF med en småmolekyl, bromosporin, sänkte H3K18‑lactylering och CXCL1‑produktion i cancerceller och i musstumörer. Som resultat trängdes färre neutrofiler in i tumörerna, fler CD8‑T‑celler ansamlades, och tumörtillväxten bromsade — allt utan synlig viktminskning eller toxicitet hos mössen.
Att göra en kall tumör het med kombinationsbehandling
Eftersom standardimmunkontrollläkemedel som anti‑PD‑1‑antikroppar har visat begränsad framgång vid bukspottkörtelcancer, testade teamet om upplösning av laktat–PCAF–CXCL1‑vägen kunde göra dessa tumörer mer mottagliga. I både subkutana och pankreatiska ortotopa musemodeller krympte tumörer mer av kombinationen bromosporin och anti‑PD‑1 än av någon behandling ensam, neutrofilinfiltrationen minskade, aktiva CD8‑T‑celler ökade, och överlevnaden förlängdes signifikant. Detta tyder på att det att stänga av tumörens metabola "sirén" för neutrofiler hjälper till att göra en immunologiskt "kall" tumör "hetare" så att checkpoint‑terapin kan engageras bättre.
Vad detta betyder för framtida behandling
Kort sagt visar studien en kedjereaktion: bukspottkörteltumörer förbränner socker, släpper ut laktat, använder det för att slå om en epigenetisk brytare på sina DNA‑packande proteiner, ökar CXCL1 och rekryterar därigenom neutrofiler som hjälper dem att gömma sig från mördande T‑celler. Att avbryta denna kedja vid PCAF‑steget med ett läkemedel bromsar inte bara tumörer utan gör också befintlig immunterapi mer effektiv i möss. Mer arbete krävs för att säkerställa säkerhet och hitta bästa sättet att rikta denna väg hos människor, men fynden lyfter fram en lovande strategi: omprogrammera tumörens metabolism och genreglering för att ge immunsystemet en rättvis chans.
Citering: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Nyckelord: bukspottkörtelcancer, tumörmetabolism, histonlactylering, tumörmikromiljö, cancerimmunterapi