Clear Sky Science · sv
Upptäckt av antimikrobiella peptider som riktar sig mot Acinetobacter baumannii via en förtränad och finjusterad few‑shot‑inlärningsbaserad pipeline
Varför detta är viktigt för vardagshälsan
Läkemedelsresistenta infektioner ökar så snabbt att de i mitten av detta sekel kan döda fler människor per år än cancer. En av de mest oroande bovarna är Acinetobacter baumannii, en svår sjukhusbakterie som står emot många antibiotika och ofta infekterar personer på respirator. Denna studie visar hur forskare kombinerade artificiell intelligens med laboratorieexperiment för att snabbt upptäcka nya, små läkemedelskandidater som kan döda denna bakterie samtidigt som de orsakar betydligt mindre skada på kroppen än vårt nuvarande sista utvägsmedel.
En sjukhussuperbugg som är svår att döda
Acinetobacter baumannii är en gramnegativ bakterie som trivs på intensivvårdsavdelningar, särskilt hos patienter beroende av respiratorer. Dess robusta yttre skal och snabbt utvecklande genom gör den resistent mot många standardantibiotika. Idag är ett av de få återstående alternativen ett läkemedel som kallas polymyxin B, men det kan orsaka allvarlig njurskada och bakterien kan ändå utveckla resistens. Samtidigt har en lovande klass av små proteinkedjor, kallade antimikrobiella peptider, utforskats mot andra mikrober, men mycket få har visat sig fungera särskilt bra mot A. baumannii. Traditionell trial‑and‑error‑screening är helt enkelt för långsam och kostsam för att sålla i det astronomiskt stora antalet möjliga korta peptidsekvenser.
Användning av smarta algoritmer för att söka i ett gigantiskt utrymme
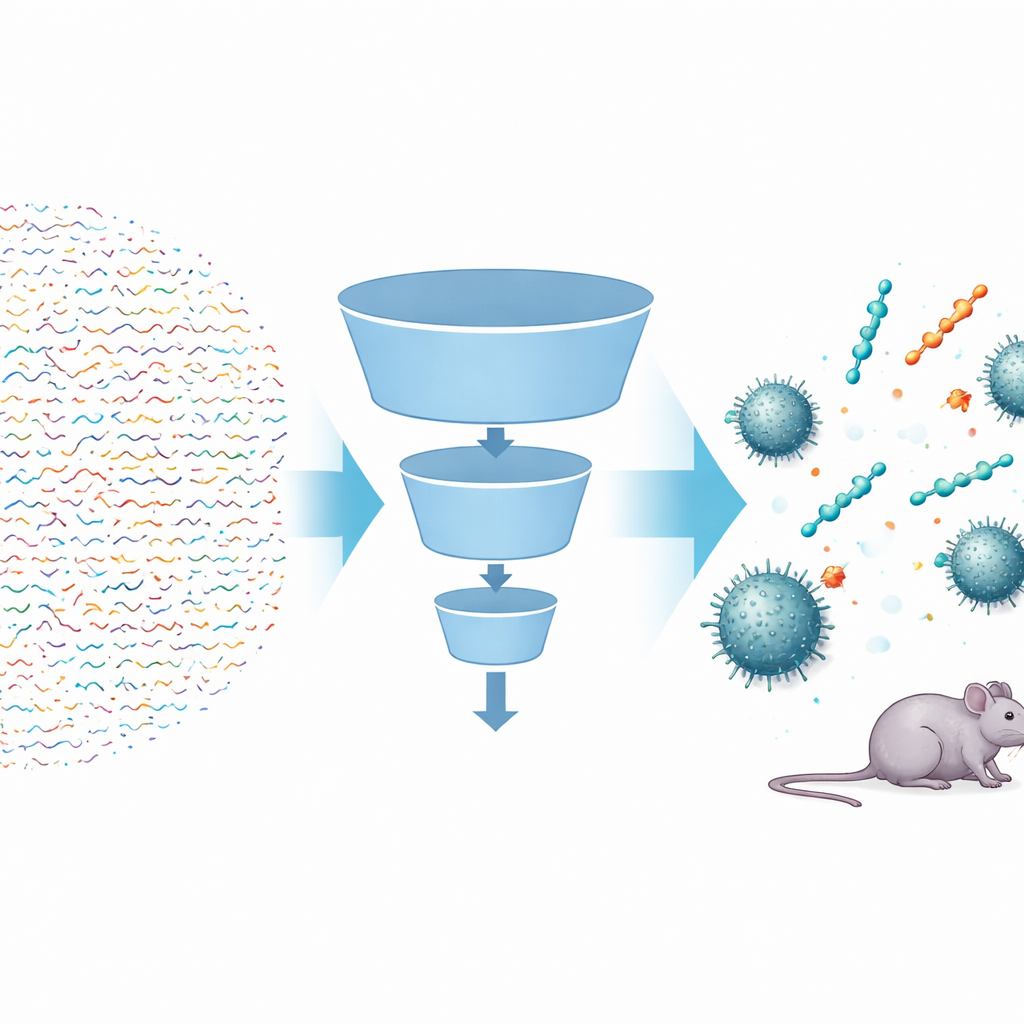
Forskarna byggde en flerstegs AI‑pipeline, kallad FSLSMEP, för att skanna hela bibliotek av korta peptider—de med sex, sju eller åtta byggstenar—motsvarande tiotals miljarder kandidater. Utmaningen var att de endast hade 148 kända peptider som fungerar mot A. baumannii, alldeles för få för standardmetoder inom maskininlärning. För att komma runt detta började de med en kraftfull förtränad modell som redan hade ”läst” hundratals miljoner naturliga proteinsekvenser och lärt sig generella regler om hur sådana molekyler beter sig. De finjusterade sedan denna modell i två steg: först på en större uppsättning peptider aktiva mot en närbesläktad bakterie, Pseudomonas aeruginosa, och slutligen på det sparsamma A. baumannii‑materialet. Längs vägen fungerade tre sammankopplade moduler—en för att skilja troliga från otroliga peptider, en för att rangordna dem och en för att uppskatta hur stark var och en kan vara—som successiva filter i en tratt.
Från datorförutsägelser till provrörsframgångar
Efter att först ha kasserat de minst lovande peptiderna med enkla kemiska regler matade teamet nästan fyra miljoner kandidater in i sin pipeline. Klassificeraren gallrade bort de flesta sekvenser som inte såg antimikrobiella ut; rankningsmodellen favoriserade dem vars egenskaper antydde stark aktivitet; och regressionsmodellen förutsade den minimala läkemedelskoncentrationen som krävdes för att stoppa bakterietillväxt. Från sextiofyra miljoner sexenhetspeptider föreslog systemet bara tio toppkandidater. När dessa syntetiserades och testades i laboratoriet visade nio verklig antibakteriell aktivitet — en imponerande träffprocent inom läkemedelsupptäckt. Samma tränade modeller användes sedan, utan omträning, på mycket större sju‑ och åttaenhetspeptidrymder, varifrån forskarna valde ytterligare topprankade sekvenser för testning. Återigen visade sig de flesta vara aktiva, inklusive heptapeptider lika potenta som polymyxin B mot vissa stammar.
Potenta dödare med en mildare beröring
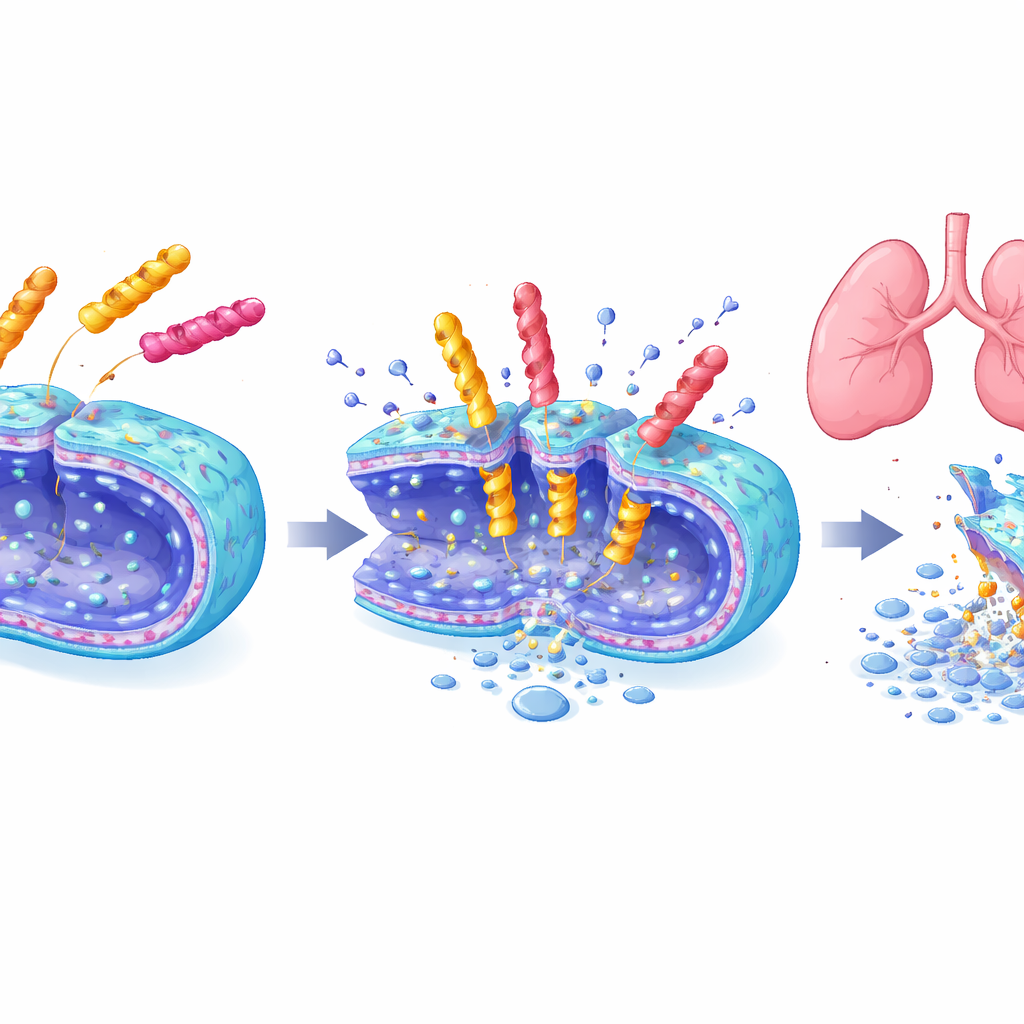
Tre ledande peptider—en från vardera sex‑, sju‑ och åttaenhetsbiblioteken—undersöktes i detalj. De utplånade snabbt A. baumannii‑populationer inom minuter till timmar, skadade bakteriella membran som syns i elektronmikroskop och fungerade även mot flera andra farliga mikrober. Samtidigt orsakade de liten skada på odlade däggdjursceller eller röda blodkroppar, till skillnad från vissa befintliga antimikrobiella peptider. I långtidsexponeringstester utvecklade bakterierna inte lätt resistens mot dessa nya molekyler, medan resistens mot polymyxin B ökade snabbt. Mest anmärkningsvärt var att i en musemodell för pneumoni rensade en inhalerad dos av heptapeptiden EME7(7) lunginfektioner lika effektivt som polymyxin B men skadade inte njurarna, medan polymyxin B gav tydlig njurskada och ökningar i blodmarkörer för njurstress.
Vad detta betyder för framtida läkemedel
Dessa resultat visar att en noggrant utformad AI‑pipeline kan omvandla en liten, ofullständig datamängd till en kraftfull motor för att upptäcka nya antimikrobiella peptider. Genom att kombinera bred förträning, stegvis finjustering och flera filtreringslager utforskade forskarna effektivt hela bibliotek av korta peptider och hittade kandidater som både bekämpar en farlig sjukhussuperbugg och tycks vara säkrare för viktiga organ. Samma strategi lyckades också hitta peptider aktiva mot den svampaktiga patogenen Candida albicans, vilket tyder på att den kan återanvändas för att söka efter många andra typer av terapeutiska peptider. För patienter kan denna metod så småningom översättas till nya läkemedel som behandlar svåra infektioner utan de svåra bieffekter och den snabba resistensutveckling som plågar dagens sista linjens antibiotika.
Citering: Huang, J., Zhang, W., Wang, A. et al. Discovery of antimicrobial peptides targeting Acinetobacter baumannii via a pre-trained and fine-tuned few-shot learning-based pipeline. Nat Commun 17, 2475 (2026). https://doi.org/10.1038/s41467-026-69306-2
Nyckelord: antimikrobiella peptider, antibiotikaresistens, Acinetobacter baumannii, maskininlärning för läkemedelsupptäckt, few‑shot‑inlärning