Clear Sky Science · sv
Utnyttja DNA-PAINT:s förutsägbara bindningskinetik för att avbrusa superupplösta bilder
Skarpare inblickar i den mikroskopiska världen
Moderna mikroskop kan numera ”se” enskilda molekyler inne i celler, men dessa bilder är ofta prickiga av vilseledande bakgrundspunkter. Denna studie introducerar ett sätt att rensa upp sådana bilder genom att utnyttja hur DNA-bitar naturligt fäster vid och släpper varandra över tid. Resultatet är klarare bilder av cellernas molekylära maskineri, vilket är viktigt för allt från grundläggande biologi till läkemedelsforskning.
Hur ett blinkande trick avslöjar dolda detaljer
En kraftfull avbildningsmetod, kallad DNA-PAINT, omvandlar den slumpmässiga bindningen av korta DNA-strängar till ett superupplöst mikroskop. En DNA-sträng är fäst vid det protein som forskaren vill se; en matchande sträng märkt med ett fluorescerande färgämne flyter i lösningen. När den flytande strängen kortvarigt binder till sin partner ger det ett litet ljusblixt. Genom att spela in många sådana blinkningar och fastställa deras positioner kan forskare återskapa proteinernas lägen med nanometerprecision—mycket skarpare än konventionella ljusmikroskop.
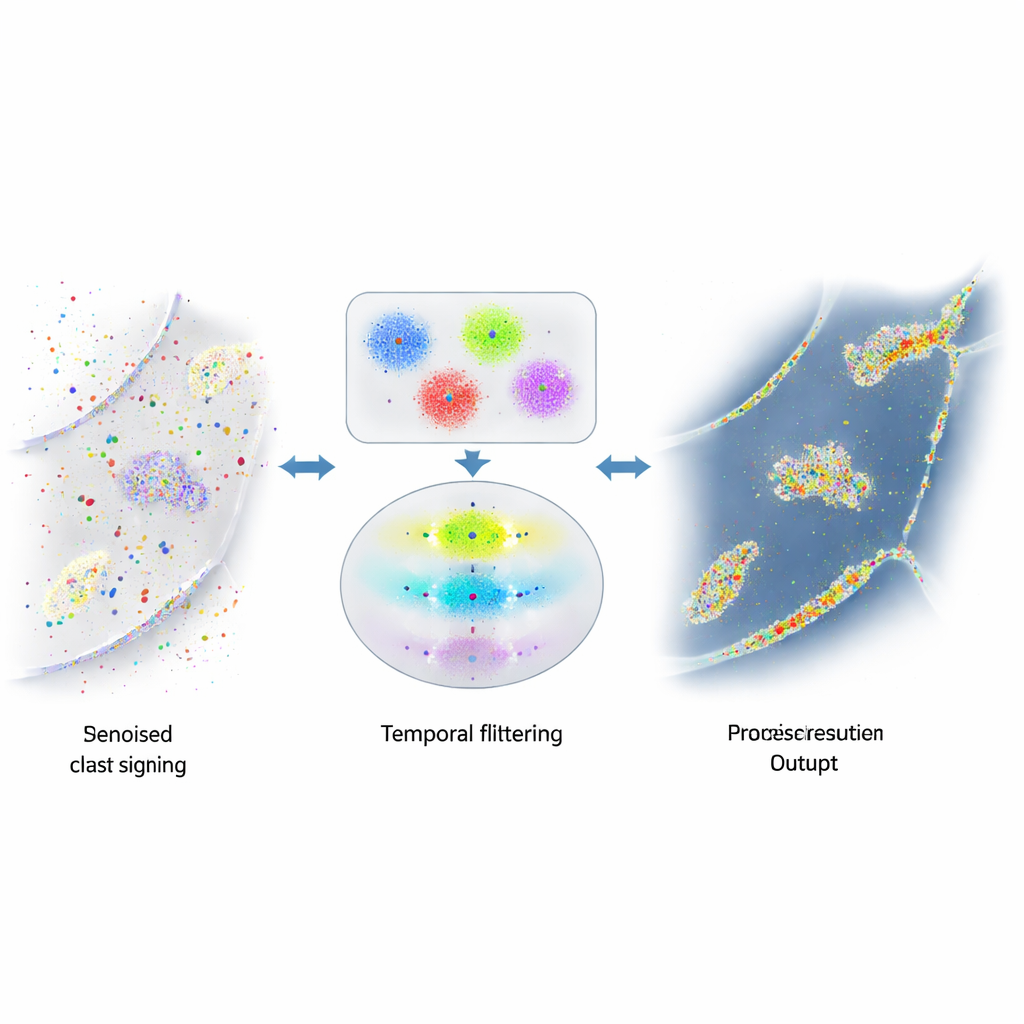
När hjälpsamma signaler grävs ner i brus
DNA-PAINT:s styrka—många fritt rörliga fluorescerande strängar—skapar också ett problem. Dessa strängar fastnar ibland där de inte borde, till exempel på slumpmässiga cellulära ytor eller på det rikliga DNA:t inne i cellkärnan. Dessa oavsiktliga blixtar är omöjliga att skilja visuellt från de verkliga och rör till den slutliga bilden med falska punkter och kluster. Tidigare försök att minska detta brus fokuserade på att ändra kemin för att göra oönskad bindning mindre vanlig, eller på grova regler för att upptäcka uppenbara avvikare. Ändå återstod en betydande mängd vilseledande signal, vilket begränsade hur tillförlitligt forskare kunde mäta proteinmängder eller rumsliga relationer.
Att använda tiden för att skilja sanning från trick
Författarna insåg att verkliga DNA-par i DNA-PAINT följer en enkel tidsregel: pauserna mellan äkta bindningstillfällen följer ett förutsägbart, exponentiellt mönster. Slumpmässiga bindningar gör inte det. De byggde en flerstegsalgoritm som först grupperar närliggande blinkningar i små kluster baserat på var de uppträder, med en kombination av densitetsbaserad klustring och k-means för att dela upp komplexa former i lokaliseringsstora enheter. För varje kluster konstruerar de sedan en ”tidskurva” av bindningstillfällen, och slår noggrant ihop snabba på/av-blinkningar från samma bindning till enstaka händelser. Slutligen tillämpar de ett statistiskt test för att undersöka om luckorna mellan händelser i varje kluster matchar det förväntade exponentiella beteendet. Kluster som klarar testet betraktas som verkliga; de som misslyckas kasseras som brus.
Metoden testad i riktiga celler
För att testa sin metod avbildade teamet celladhesionsproteinet E-cadherin i fruktflugans äggkammare, där vissa celler producerade det märkta proteinet och närliggande celler inte gjorde det. Detta skapade sid-vid-sid-områden rika på äkta signal och områden som bara borde innehålla bakgrund. Genom att justera hur många bindningstillfällen ett kluster måste uppvisa innan det testas fann de inställningar som tog bort över 90 % av de falska klustren samtidigt som mer än 98 % av de verkliga vid cellgränserna behölls. I avbrusade bilder blev fina strukturer, såsom tunna rörformiga strukturer och vesiklar, mycket tydligare. Samma strategi fungerade i andra system, inklusive mitokondrier och mikrotubuli, och till och med för proteiner med mer diffusa, amorfa fördelningar där rumsliga mönster ensamma inte ger någon ledtråd om vad som är verkligt.
Klarare molekylära kartor för framtida studier
Genom att lyssna på DNA-bindningens ”rytm” istället för enbart titta på var blinkningar inträffar, renar denna metod pålitligt bort vilseledande bakgrund från DNA-PAINT-data. För icke-specialister är huvudresultatet enkelt: skarpare, mer pålitliga molekylära kartor inne i celler. Det gör det säkrare att räkna hur många proteinmolekyler som finns, att bedöma hur nära olika proteiner sitter intill varandra och att bygga mer exakta bilder av cellernas inre liv. Allteftersom DNA-baserad avbildning växer kommer denna typ av smart avbrusning vara avgörande för att omvandla råa prickiga bilder till solida biologiska insikter.
Citering: Sirinakis, G., Allgeyer, E.S., Richens, J.H. et al. Utilizing the predictable binding kinetics of DNA-PAINT to denoise super-resolution images. Nat Commun 17, 2397 (2026). https://doi.org/10.1038/s41467-026-69304-4
Nyckelord: DNA-PAINT, superupplöst mikroskopi, bildavbrusning, enstaka-molekylavbildning, proteinkartläggning