Clear Sky Science · sv
STING-aktivering framkallar cytotoxiska och immunsvar i meningiom via inflammatoriska celldöds‑vägar
Att vända kroppens larm mot hjärntumörer
Meningiom hör till de vanligaste hjärntumörerna, och även om operation och strålning ofta hjälper återkommer vissa tumörer. Dessa envisa tillväxter kan orsaka kramper, huvudvärk och funktionsnedsättning, men det finns få etablerade läkemedelsbehandlingar. Denna studie undersöker ett sätt att få tumörcellerna och de närliggande immuncellerna att sända ett kraftfullt internt larm, med hjälp av en molekyl som aktiverar ett medfött farosystem kallat STING. Genom detta vill forskarna inte bara döda tumörceller direkt, utan också väcka immunsystemet och luckra upp tumörens tuffa stomme.
En tumör gömd i ett tyst immunkvarter
Författarna kartlade först den cellulära ”grannskapet” i mänskliga meningiom med hjälp av enkelcellssekvensering och spatial avbildning. De fann att dessa tumörer är fyllda med medfödda immunceller, särskilt makrofager, medan klassiska tumörbekämpande T‑celler och natural killer‑celler (NK) är få och ofta utmattade. Omgivande tumörcellerna finns ett tätt skal av kollagen och andra matrixproteiner som bildar en pansarlik, lager på lager‑struktur. Många makrofager i dessa regioner bär inhibitoriska receptorer som aktiveras av kollagen, vilket skapar en kraftigt undertryckt miljö där immunceller är närvarande men hålls tillbaka istället för att frigöras mot cancern.
Att hitta en strömbrytare som tumörcellerna fortfarande har
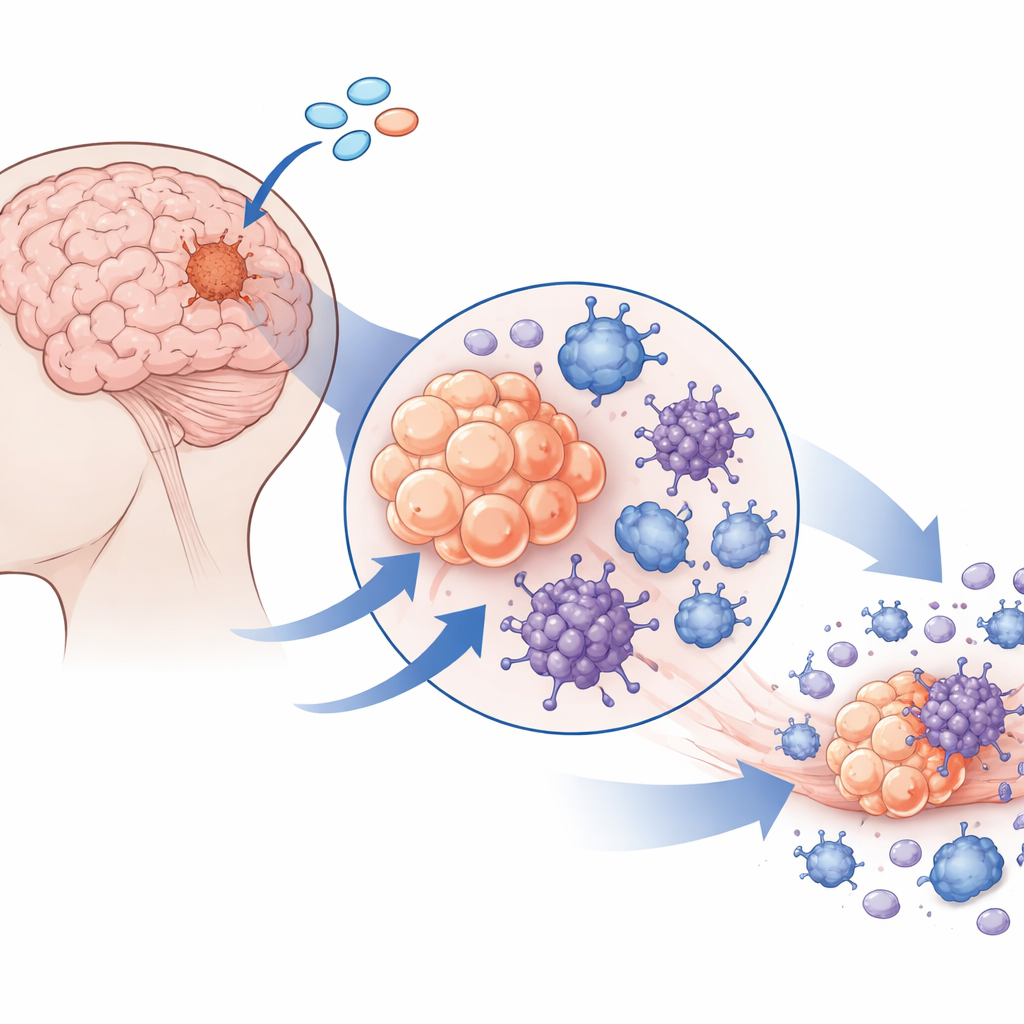
Sedan sökte teamet efter vägar som kunde vända denna suppressiva miljö till en inflammerad, tumörfientlig sådan. De fokuserade på STING, en sensor som normalt svarar på felplacerat DNA inne i celler och utlöser antivirala och inflammatoriska svar. Till skillnad från många andra hjärntumörer visade sig meningiomceller ha ovanligt höga STING‑nivåer. Detta spårades till öppet kromatin och låg DNA‑metylering vid STING‑genen, vilket betyder att genen är epigenetiskt förberedd för aktivitet. STING fanns inte bara rikligt i tumörceller utan även i närliggande blodkärlsceller och makrofager, vilket tyder på att ett enda läkemedel potentiellt kan påverka flera nyckelspelare i tumörmikromiljön samtidigt.
Tvång att leda tumörceller till brännande självförstörelse
FORSKARNA behandlade nyupptagna patientmeningiomprover med en potent STING‑agonist kallad 8803. Även när immunceller avlägsnats dog tumörcellerna, vilket bevisade en direkt effekt. Genom att tillsätta läkemedel som selektivt blockerar olika celldöds‑vägar, och genom att avläsa genaktivitet, visade de att 8803 inte enbart orsakade tyst apoptos. Istället drev det meningiomceller in i flera inflammatoriska former av celldöd—pyroptos, nekroptos och ferroptos—vilka får celler att sprängas öppna snarare än att prydligt demonteras. Ett nyckelsteg var aktivering och klyvning av ett protein kallat gasdermin D, som bildar porer i cellmembranet. Elektronmikroskopi visade tumörceller fyllda av membranhål och skadade mitokondrier, och blockering av reaktiva syreföreningar minskade dödligheten, vilket kopplar mitokondriell stress till denna brännande undergång.
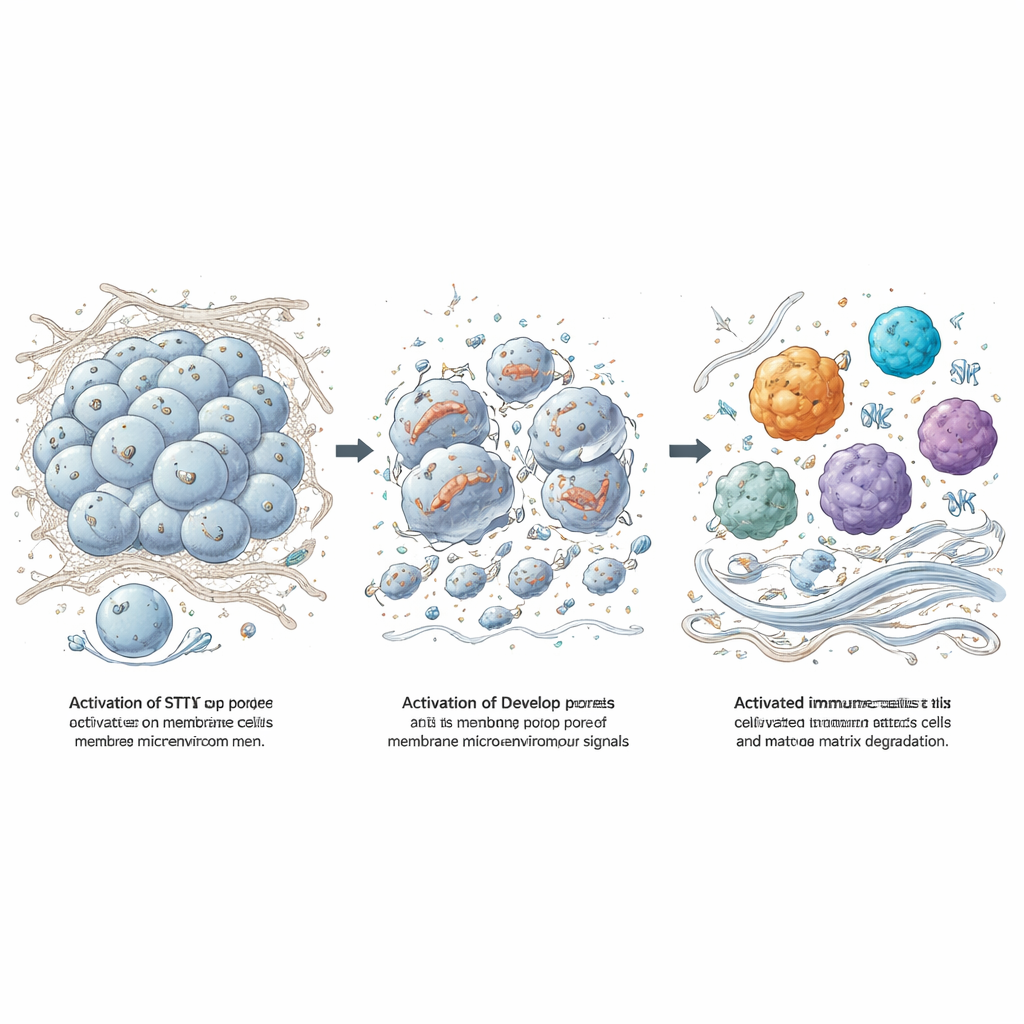
Från tumörskräp till immunvaknande och matrixnedbrytning
När tumörceller dör på detta dramatiska sätt spiller de ut ”faromolekyler” som kan väcka immunceller. Teamet exponerade musmakrofager för lyserade meningiomceller och såg en våg av inflammatoriska faktorer och enzymer som bryter ned kollagen, särskilt matrixmetalloproteinas‑3 (MMP‑3). Genom att arbeta med möss som saknar specifika signaladaptorer visade de att toll‑liknande receptorer, ett annat farosystem, är avgörande för detta svar, samtidigt som STING‑aktivering av 8803 tillför en egen nivå av immunstimulans. I musmodeller av meningiom ledde direkt injektion av 8803 i tumörer till krympning eller stabilisering av tillväxten, förlängd överlevnad och omvandling av tumörområdet från en tyst, kollagenrik massa till en plats fylld av aktiva makrofager, NK‑celler, T‑celler och markant minskad kollagenfärgning.
Varför denna strategi kan förändra behandling för patienter
Sammanfattningsvis visar studien att meningiom bär på en inbyggd sårbarhet: deras tumörceller behåller en tillgänglig STING‑strömbrytare som, när den slås på av 8803, driver dem in i explosivt, inflammatoriskt celldöd. Denna process både dödar cancerceller och översvämmar området med larm‑signaler som rekryterar och energiserar immunceller, samtidigt som den hjälper till att bryta ned kollagenstommen som bidrar till massverkan. Eftersom meningiom vanligtvis är lokaliserade snarare än brett metastaserande, och eftersom standardalternativen är begränsade vid recidiv, kan en lokalt administrerad STING‑agonist som 8803 erbjuda ett nytt, målinriktat sätt att både minska tumörbördan och omprogrammera dess immummiljö för varaktig kontroll.
Citering: Youngblood, M.W., Tripathi, S., Najem, H. et al. STING activation induces cytotoxic and immune responses in meningiomas via inflammatory cell death pathways. Nat Commun 17, 2685 (2026). https://doi.org/10.1038/s41467-026-69296-1
Nyckelord: meningiom, STING‑väg, immunterapi mot hjärntumörer, inflammatoriskt celldöd, tumörmikromiljö