Clear Sky Science · sv
Den genetiska drivaren bakom akut nekrotiserande encefalopati, RANBP2, reglerar den inflammatoriska responsen vid influensa A‑virusinfektion
När influensan skadar hjärnan
De flesta förknippar influensa med en vecka av feber, hosta och sängläge. I sällsynta fall, särskilt hos barn, kan en vanlig influensainfektion dock plötsligt utvecklas till en livshotande hjärnsjukdom kallad akut nekrotiserande encefalopati (ANE). Familjer och läkare har länge misstänkt att gener bidrar till vem som drabbas av denna katastrofala komplikation. Denna studie visar hur ett enda cellulärt grindvaktprotein, RANBP2, normalt håller influensaviruset i schack och hindrar kroppens egen inflammatoriska respons från att skena iväg.
En sällsynt men förödande influensakomplikation
ANE uppträder abrupt efter en febersjukdom, ofta influensa, och kan snabbt orsaka kramper, koma och bestående neurologisk skada. Ungefär hälften av kända ANE‑fall globalt kopplas till influensa A‑virus, särskilt H1N1‑stammen. Barn som ärver vissa förändringar i RANBP2‑genen har en mycket högre risk, i en sjukdomsform som kallas ANE1. Fram tills nu har forskare dock inte förstått vad detta protein faktiskt gör under influensainfektion, eller varför dess förändring leder till så svår inflammation i hjärnan.
Cellulära portar och virala genom
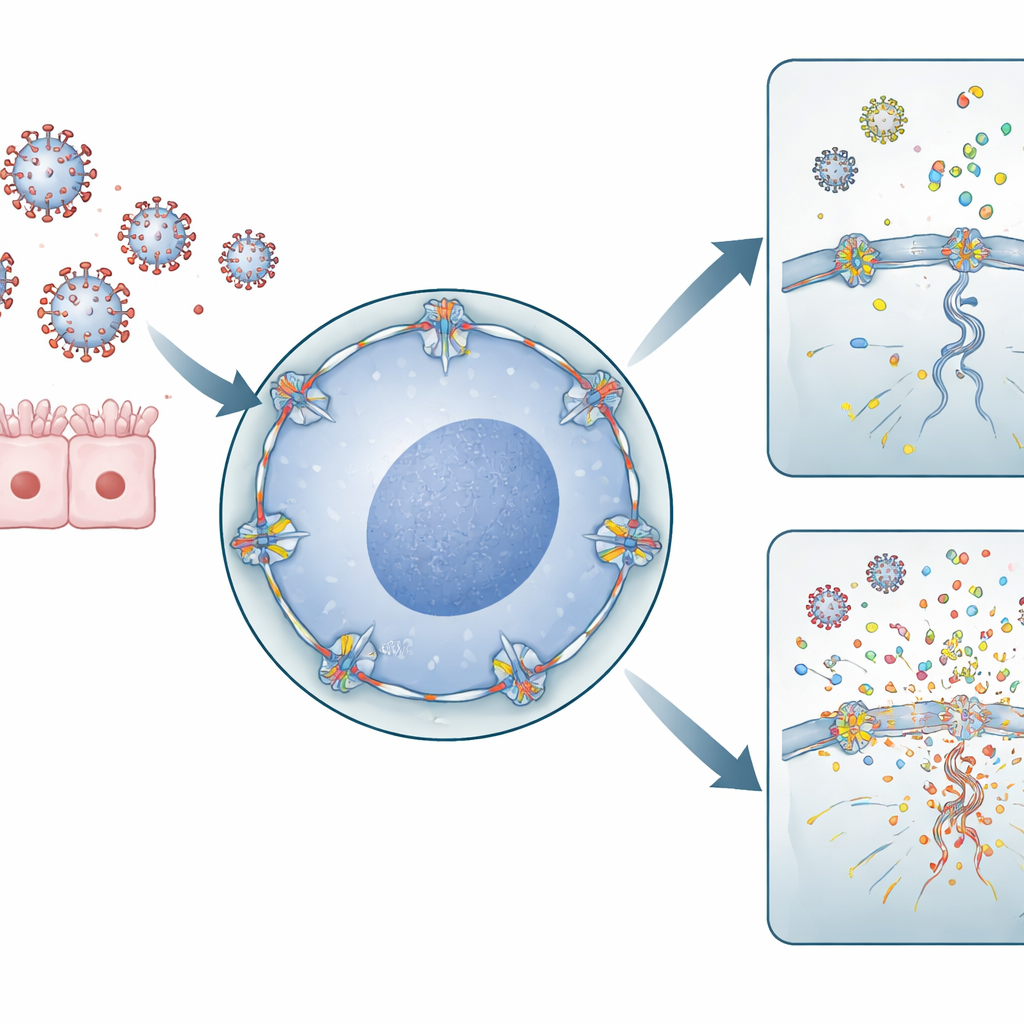
Influensa A‑virus har ett ovanligt levnadssätt för ett RNA‑virus: det måste ta sig in i cellens cellkärna för att kopiera sitt genetiska material. För att göra det passerar det genom kärnporer—stora portar i kärnmembranet som kontrollerar trafiken mellan kärnan och det omgivande cytoplasman. RANBP2 är en huvudkomponent på utsidan av dessa porer. Författarna använde humana lungderiverade celler och immunceller för att sänka RANBP2‑nivåer eller införa den ANE‑kopplade mutationen. De fann att när RANBP2 saknades eller var felplacerat, replikerades influensagenom mer omfattande i kärnan, och virala genetiska segment exporterades till cytoplasman på ett obalanserat sätt. Överraskande nog gav detta överskott av viralt RNA inte fler infektiva partiklar, men det förändrade var och hur viralt material samlades inuti cellen.
När virala fragment matar larmsystemet
Immunförsvaret förlitar sig på molekylära sensorer som upptäcker lösa bitar av viralt RNA i cytoplasman som farosignaler. Teamet visade att i celler utan normalt RANBP2 samlades extra virala RNA‑segment upp i cytoplasman och skapade precis de mönster som dessa sensorer känner igen. I lungderiverade celler utlöste detta högre nivåer av inflammatoriska molekyler såsom IL‑6 och IL‑1β. I primära humana makrofager—första försvarslinjen‑immunceller från blodgivare—ledde förlust av RANBP2 till en påfallande ökning av proinflammatoriska kemokiner, inklusive CXCL8, CXCL10, CCL2, CCL3 och CCL4. Dessa kemiska budbärare rekryterar och aktiverar ytterligare immunceller och förstärker den övergripande reaktionen mot infektionen.
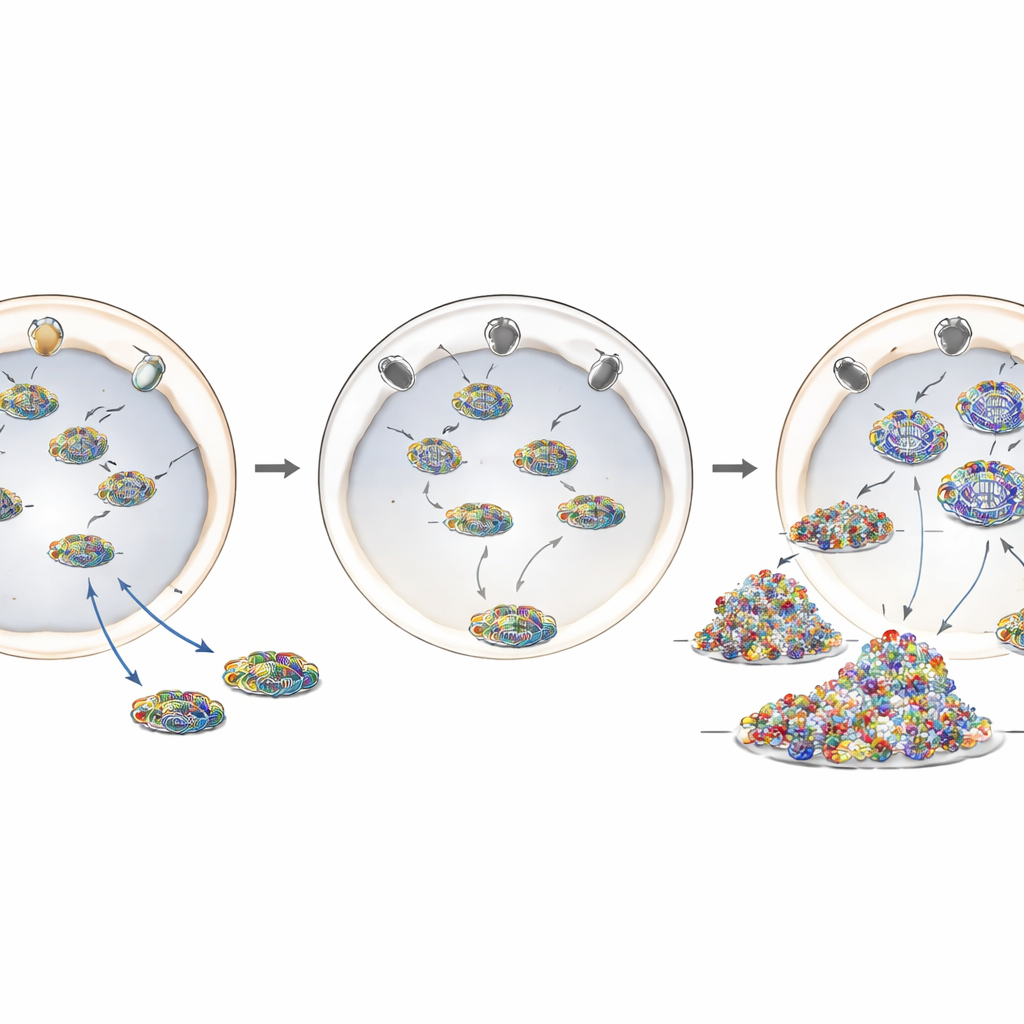
En sjukdomsmutation som förflyttar en väktare
För att modellera ANE1 närmare använde forskarna CRISPR‑Cas9‑genredigering för att införa den vanligaste sjukdomsassocierade förändringen, T585M, i den humana RANBP2‑genen. I dessa redigerade celler var RANBP2‑proteinets nivåer till stor del normala, men dess placering var det inte: istället för att bilda en tydlig kant runt kärnmembranet var mycket av proteinet förflyttat in i cellens inre. Celler med denna mutation, oavsett om den fanns i en eller båda genkopiorna, uppvisade liknande beteende som RANBP2‑utarmade celler. De visade ökad influensagenomreplikation, mer viralt material i cytoplasman och en starkare inflammatorisk respons efter infektion. Detta tyder på att korrekt positionering av RANBP2 vid kärnporerna—snarare än dess totala mängd—är avgörande för dess skyddande roll.
Varför detta är viktigt för barn i riskzonen
Tillsammans målar resultaten upp RANBP2 som en cellulär väktare som finjusterar hur influensas genetiska material rör sig in i och ut ur kärnan. När RANBP2 saknas eller är felplacerat överreplikerar och exporteras viralt RNA på ett kaotiskt sätt, vilket fyller cytoplasman med molekylärt skräp som kraftigt intensifierar immunsignalerna. För de flesta vävnader kan detta innebära en hårdare men överlevbar influensasjukdom. Hos sårbara barn med ANE1 kan dock sådan okontrollerad inflammation—särskilt om den når hjärnan—bidra till att förklara den plötsliga, svåra neurologiska skada som ses efter annars vanliga infektioner. Att förstå denna väg kan vägleda framtida strategier för att tidigt identifiera riskpatienter och anpassa antiinflammatoriska behandlingar innan immunsvaret går från skyddande till destruktivt.
Citering: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Nyckelord: influensa, akut nekrotiserande encefalopati, RANBP2, hyperinflammation, kärnpor