Clear Sky Science · sv
En roll för interaktionen mellan condensin och mediator i mitotisk kromosomorganisation
Hur delande celler håller sitt genetiska hus i ordning
Varje gång en cell delar sig måste den noggrant packa och skilja åt meter med DNA så att varje dottercell får en komplett uppsättning kromosomer. När denna process misslyckas kan resultatet bli celldöd, utvecklingsstörningar eller cancer. Denna studie avslöjar hur två stora molekylära maskiner—en som styr genaktivitet och en annan som kompakterar DNA—samarbetar för att vika kromosomer under celldelning, och blottlägger en dold koppling mellan vilka gener som slås på i mitos och om kromosomer delas korrekt.
Nyckelaktörer: packaren och samordnaren
I kärnan fungerar ett proteinkomplex som kallas condensin som en molekylär packare och loopar och drar ihop DNA till de tjocka kromosomer som syns under mitos. Ett annat stort komplex, kallat mediator, hjälper till att kontrollera vilka gener som är påslagna eller av genom att samverka med RNA-polymeras, enzymet som kopierar DNA till RNA. Författarna studerade dessa komplex i klyvningjäst, en väletablerad modellorganism vars kromosombiologi liknar människocellernas. De upptäckte att en subenhet i condensin, Cnd1, binds fysiskt till en mediator-subenhet kallad Pmc4. Denna interaktion sker vid mycket aktiva gener och vid en speciell uppsättning gener som slås på endast under mitos. Dessa ”mitotiska gener” ligger i kanterna av stora kromosomala områden, eller domäner, och verkar fungera som gränsmarkörer.
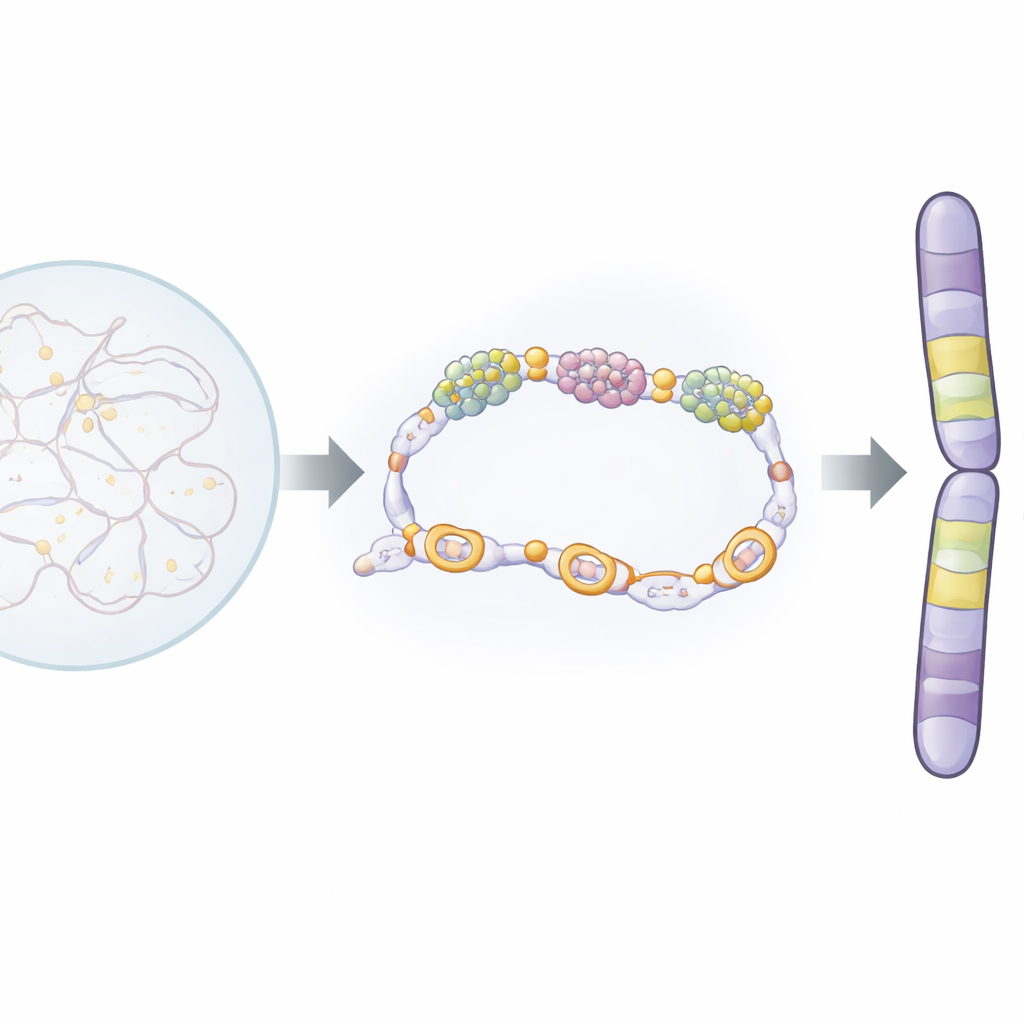
En enda molekylär handskakning med stora följder
För att testa hur viktig denna handskakning är, konstruerade forskarna en mycket precis mutation i Cnd1 och ändrade bara en aminosyra (K658E) så att Cnd1 inte längre kan binda Pmc4 samtidigt som en normal condensin-komplex fortfarande bildas. Jästceller som bar denna mutation var livsdugliga, men deras kromosomer delades fel oftare och lämnade efter sig släpande DNA-bitar under mitos. Med hjälp av 3D-genomkartläggning (Hi-C) och mikroskopiska avståndsmätningar mellan utvalda DNA-platser visade teamet att de mutanta cellerna hade svagare condensindrivna kontakter och mindre kompakta kromosomdomäner. Med andra ord, utan en fungerande Cnd1–Pmc4-interaktion kunde condensin inte effektivt vika kromosomer till robusta, domänbaserade strukturer under celldelning.
Genaktivitet som gränsbyggare
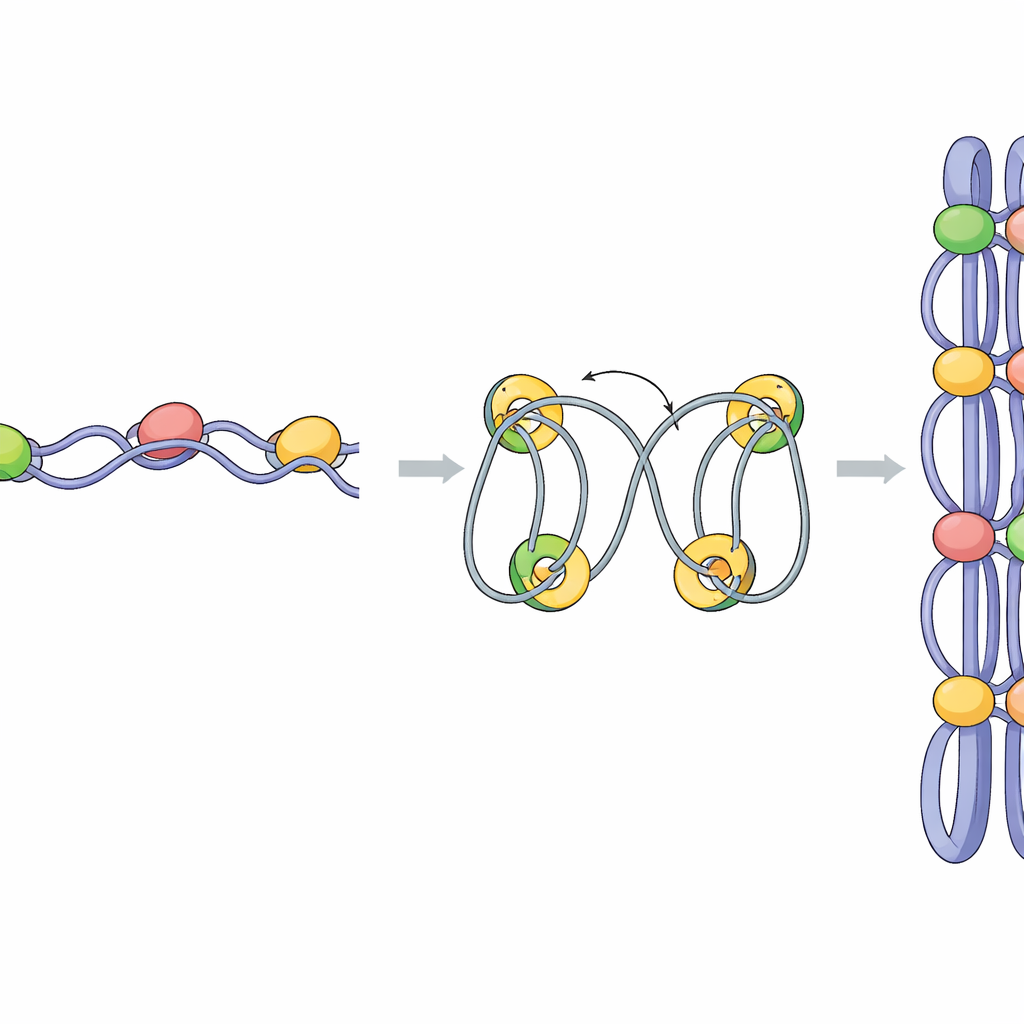
Studien undersökte därefter hur mediator bidrar till denna vikning. När Pmc4 utarmades minskade condensinbindningen vid många gener och styrkan i condensin-skapade domäner sjönk. Slående nog blev gränserna mellan närliggande domäner suddiga och DNA-interaktioner började flöda över vad som tidigare var skarpa gränser. Detaljerade RNA-mätningar visade att förlust av Pmc4 kraftigt reducerade uttrycket av en delmängd mitotiskt aktiverade gener som styrs av transkriptionsfaktorn Ace2. Dessa gränsgeners promotorer uppvisade normalt mycket hög beläggning av mediator, condensin och en basal transkriptionsfaktor kallad TBP. Data stöder en modell där mediator och TBP först rekryterar condensin till promotorer för mycket aktiva och mitotiska gener; när transkription fortgår skjuts condensin längs genkropparna och hjälper till att binda närliggande DNA i loopar, där Ace2-målgenerna sätter kanterna för varje kondenserad domän.
En möjlig roll för vätskeliknande droppar
Det är känt att mediator i humana celler kan bilda vätskeliknande droppar genom en process som kallas fasseparation, vilket kan koncentrera transkriptionsmaskineri i små nukleära nav. Författarna fann att mediator i klyvningjäst beter sig likartat: Pmc4-subenheten kan bilda droppar i provrör, och behandling av celler med 1,6-hexandiol, en kemikalie som stör sådana kondensat, spred snabbt mediatorfokuser i kärnan. Mild hexandiol-behandling försvagade mediator- och condensinbindning vid nyckelgener och suddade specifikt ut gränserna mellan kromosomdomäner, även om den övergripande kompakteringen av kromosomer fortfarande fortgick. Detta tyder på att mediatorrika droppar vid mitotiska gränsgen kan hjälpa att forma var domäner börjar och slutar genom att fokusera transkription och condensin-pålastning på dessa platser.
Från jästlektioner till människors hälsa
Slutligen undersökte teamet om ett liknande samarbete finns i humana celler. Med ett interaktionsprov fann de att MED4, den humana motsvarigheten till Pmc4, binder specifikt till CAP-D3, en condensin II-subenhet som är nära besläktad med jästens Cnd1. En mutation i mänskligt CAP-D3 motsvarande jästens K658E-störning bröt denna interaktion och orsakade mitotiska fel, såsom felställda kromosomer och mikronuklei. Utarmning av MED4 gav också segregeringsdefekter. Dessa paralleller tyder på att kopplingen mellan mediator och condensin är en bevarad strategi som celler använder för att samordna genaktivitet med kromosomvikning och därigenom säkerställa att DNA packas och delas jämnt under celldelning.
Varför detta är viktigt för att förstå sjukdom
Detta arbete visar att hur kromosomer viks under mitos inte bara handlar om rå kompaktering. Istället beror det på var och när särskilda gener slås på, där mediatorstyrd transkription vid gränsgen rekryterar condensin för att forma storskaliga domäner. Genom att visa hur en enda interaktion mellan två komplex kan få genomgripande effekter på helkromosomarkitektur och segregeringsnoggrannhet erbjuder studien en ram för att förstå hur subtila förändringar i genregleringsmaskineriet eller i condensinfunktionen kan leda till kromosominstabilitet, ett kännetecken för många cancerformer och genetiska sjukdomar.
Citering: Iwasaki, O., Tashiro, S., Chung, C.YL. et al. A role for condensin-mediator interaction in mitotic chromosome organization. Nat Commun 17, 2509 (2026). https://doi.org/10.1038/s41467-026-69270-x
Nyckelord: kromosomarkitektur, condensin, mediatorkomplexet, mitos, 3D-genomorganisation