Clear Sky Science · sv
Heterogen multicopy av blaCTX-M-varianter på samma plasmid ökar evolutionär anpassningsförmåga hos klinisk Klebsiella pneumoniae
Varför detta är viktigt för modern medicin
Antibiotikaresistenta infektioner är ett växande hot på sjukhus världen över, och läkare förlitar sig i allt större utsträckning på sista-hands-läkemedel för att rädda patienter. Denna studie förklarar hur en vanlig sjukhusbakterie, Klebsiella pneumoniae, kan använda en subtil genetisk strategi för att stå emot kraftfulla antibiotikakombinationer som är utformade för att övervinna resistens. Genom att avslöja denna strategi hjälper forskningen att förklara varför vissa infektioner återkommer trots aggressiv behandling — och ger ledtrådar för hur kliniker kan ligga steget före.
En sjukhusmikrob under tryck
Berättelsen börjar på en intensivvårdsavdelning, där två patienter blev infekterade av nästan identiska stammar av K. pneumoniae. Den ena stammen behandlades lätt med den moderna läkemedelsparet ceftazidim/avibactam, medan den andra var starkt resistent. Genetiska jämförelser visade att båda stammar bar samma breda familj av resistensenzym, kallade β-laktamaser, på en gemensam plasmid — en liten, rörlig DNA-cirkel inne i bakterien. Men i den resistenta stammen hade en av dessa enzymer förändrats subtilt, och den varianten, kallad CTX-M-249, tillät bakterien att stå emot läkemedelskombinationen som borde ha dödat den.
En liten förändring med stora konsekvenser
Närmare biokemiska tester visade att CTX-M-249 byter en typ av skydd mot en annan. Den vanliga versionen, CTX-M-65, är utmärkt på att bryta ner vissa antibiotika som cefotaxim, men förblir sårbar för hämmaren avibactam. CTX-M-249, förändrad på bara två positioner i proteinet, blir bättre på att hantera ceftazidim plus avibactam men förlorar mycket av sin styrka mot cefotaxim. På papperet ser detta ut som en klassisk evolutionär avvägning: vinna ett försvar samtidigt som ett annat försvagas. Ändå undvek den kliniska stammen denna nackdel genom att bära flera nära besläktade kopior av genen samtidigt, så att olika versioner av enzymet kunde samexistera i samma bakterielinje.
Många kopior, många möjligheter
Med hjälp av long-read DNA-sekvensering och precisa kvantifieringsmetoder fann forskarna att plasmiden i den resistenta stammen innehöll två separata blaCTX-M-platser, och att en av dem kunde förekomma i flera något olika varianter. Utan antibiotikapåverkan bar ungefär hälften av populationen den äldre CTX-M-65-versionen och nästan hälften bar CTX-M-249, med en liten andel som bar mellanliggande former. När bakterierna utsattes för ökande doser ceftazidim/avibactam steg både antalet genkopior och andelen CTX-M-249 kraftigt. Ibland skedde detta genom att antalet plasmider per cell ökade; vid högre läkemedelsnivåer växte plasmiden själv fram korta tandemupprepningar av resistensgenen. I praktiken använde bakterierna DNA-duplication som en ratt de kunde vrida upp eller ner för att matcha de omgivande antibiotika.
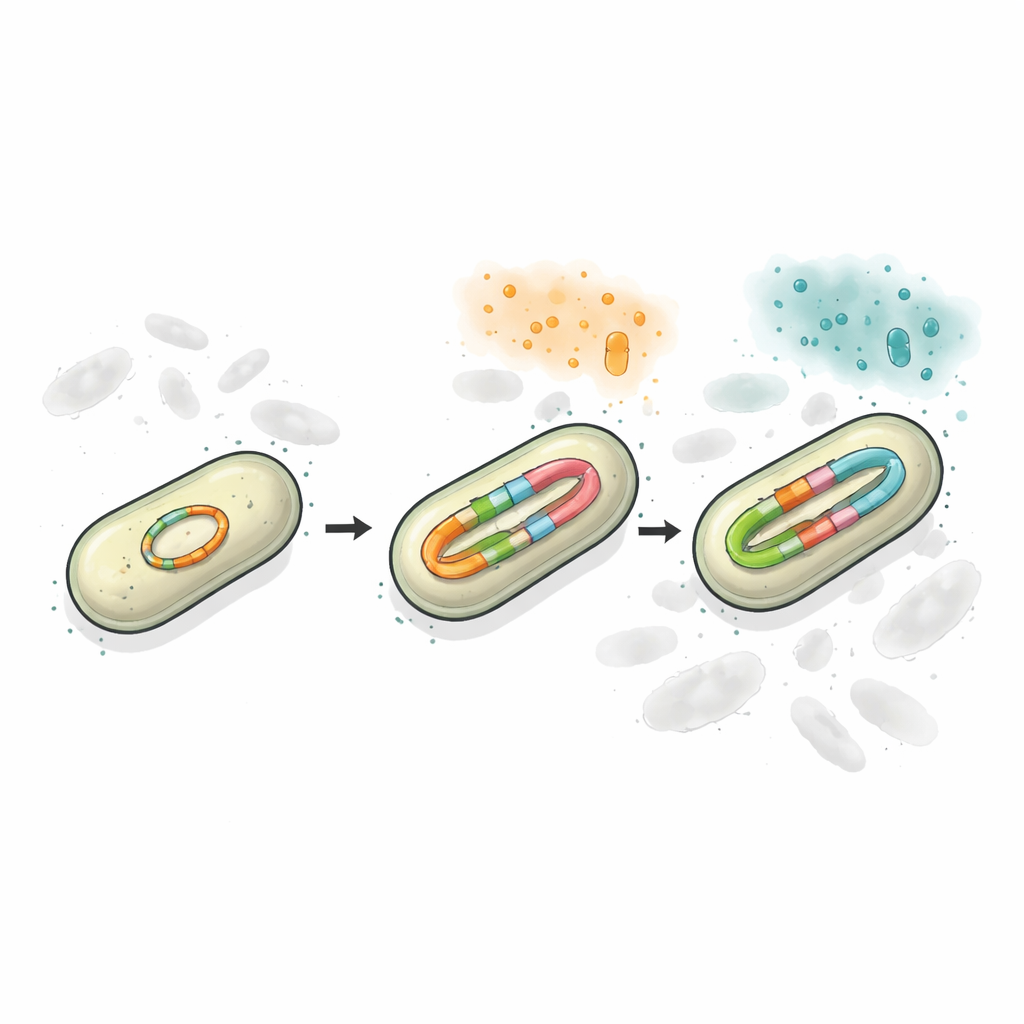
Behålla mångfald på en DNA-cirkel
För att testa hur denna ordning påverkar överlevnad byggde teamet förenklade laboratoriemodeller där bakterier bar antingen en resistensversion, två versioner på separata plasmider eller båda versionerna kodade tillsammans på en enda plasmid. När de utsattes för två olika cefalosporin-läkemedel presterade de blandade systemen bättre än enkelgenstammar, eftersom åtminstone en enzymversion kunde hantera varje läkemedel. Konfigurationen där båda genvarianterna satt på samma plasmid visade sig dock vara mest stabil. När antibiotika applicerades under flera dagar eller byttes från ett läkemedel till ett annat förlorade celler med två separata plasmider ofta en av dem och offrade en del av sitt skydd. Däremot ärvdes "två-i-ett"-plasmiden som ett paket, vilket bevarade båda resistensalternativen även när den medförde en kortsiktig tillväxthämning.
En bredare strategi i farliga bakterier
Matematiska modeller reproducerade dessa experiment och visade att, över vissa antibiotikanivåer, dominerar bakterier med en enda plasmid som bär flera resistensvarianter slutligen blandade populationer. Forskarna sökte sedan igenom tusentals K. pneumoniae-genomer från sjukhus, gårdar, livsmedel och miljö. De fann ofta flera något olika kopior av viktiga resistensgener — särskilt i mänskliga kliniska isolat som utsätts för stark läkemedelsexponering. Detta tyder på att att bygga in "multicopy-heterogenitet" i plasmider inte är en sällsynt kuriositet utan en utbredd taktik som bakterier använder för att satsa på flera kort mot föränderliga behandlingar.
Vad detta betyder för patienter och behandling
För en icke-specialist är kärnbudskapet att vissa bakterier inte bara bär en enda resistensgen; de bär familjer av besläktade varianter samlade på samma rörliga DNA-element, vilket ger dem ett flexibelt verktyg mot olika läkemedel. Denna ordning gör att de kan behålla resistens under långa perioder, även när läkare byter behandlingar, och hjälper till att förklara varför vissa infektioner är så svåra att utrota. Samtidigt visar studien att noggrant valda läkemedelskombinationer — såsom att para ceftazidim/avibactam med cefotaxim — kan utnyttja svagheter i detta system och undertrycka även dessa välbeväpnade stammar. Att förstå hur bakterier konstruerar och använder dessa multicopy-plasmider är därför avgörande för att utforma smartare antibiotikastrategier och bromsa resistensens framfart.
Citering: Weng, R., Zhu, J., Wu, X. et al. Heterogeneous multicopy of blaCTX-M variants on the same plasmid enhances evolutionary adaptability in clinical Klebsiella pneumoniae. Nat Commun 17, 2460 (2026). https://doi.org/10.1038/s41467-026-69266-7
Nyckelord: antibiotikaresistens, Klebsiella pneumoniae, plasmider, beta-laktamaser, multiläkemedelsbehandling