Clear Sky Science · sv
Trifunktionellt flavoprotein‑katalyserad asymmetrisk montering av 4‑alkylbutenolid i avenolidbiosyntes
Varför små ringar hos bakterier är viktiga för oss
Många livräddande läkemedel, från antiparasitära medel till växtskyddsprodukter, bygger på en liten kemisk motivgrupp som kallas butenolid. Idag tillverkas dessa ringar oftast från olje‑baserade utgångsmaterial i flerstegsindustrier som förbrukar energi och skapar avfall. Denna studie visar hur jordbakterier bygger en sådan ring — ett hormon kallat avenolid som slår på produktionen av den storsäljande antiparasitära läkemedelsgruppen avermectiner. Att förstå denna naturliga väg pekar mot renare, billigare sätt att framställa användbara kemikalier och kan hjälpa till att hitta nya antibiotika.
Den speciella ringen i många läkemedel
Butenolider är kompakta femledade ringar som kemister uppskattar eftersom de reagerar på mångsidiga sätt och förekommer i många naturprodukter och moderna läkemedel. De hjälper till att forma molekyler med anticancer-, antifungala, antiinflammatoriska och insekticida aktiviteter som används i medicin och jordbruk. Traditionella syntesvägar till dessa ringar kräver ofta flera noggrant kontrollerade steg, dyra katalysatorer och petroleum‑råvaror. Den kombinationen ökar kostnader och miljöpåverkan, och driver forskare att söka efter biologiska genvägar som naturen redan har förfinat.
Ett bakteriellt hormon som aktiverar ett blockbuster‑läkemedel
I jordbakterien Streptomyces avermitilis fungerar den butenolid‑innehållande molekylen avenolid som ett litet hormon. Vid mycket låga koncentrationer binder den till ett reglerande protein och lyfter en molekylär broms på de gener som producerar avermectiner, potenta medel som förlamar parasitiska maskar och vissa insekter. Tidigare genetiska studier hade antytt att två enzymer, kallade SavA och SavB, bygger avenolid, men de faktiska stegen var okända. Gruppen flyttade först de relevanta generna till en mer samarbetsvillig släkting, Streptomyces albidoflavus, och optimerade odlingsförhållandena tills den modifierade stammen producerade milligramkvantiteter ren avenolid — tillräckligt för att dissekera vägen i detalj. 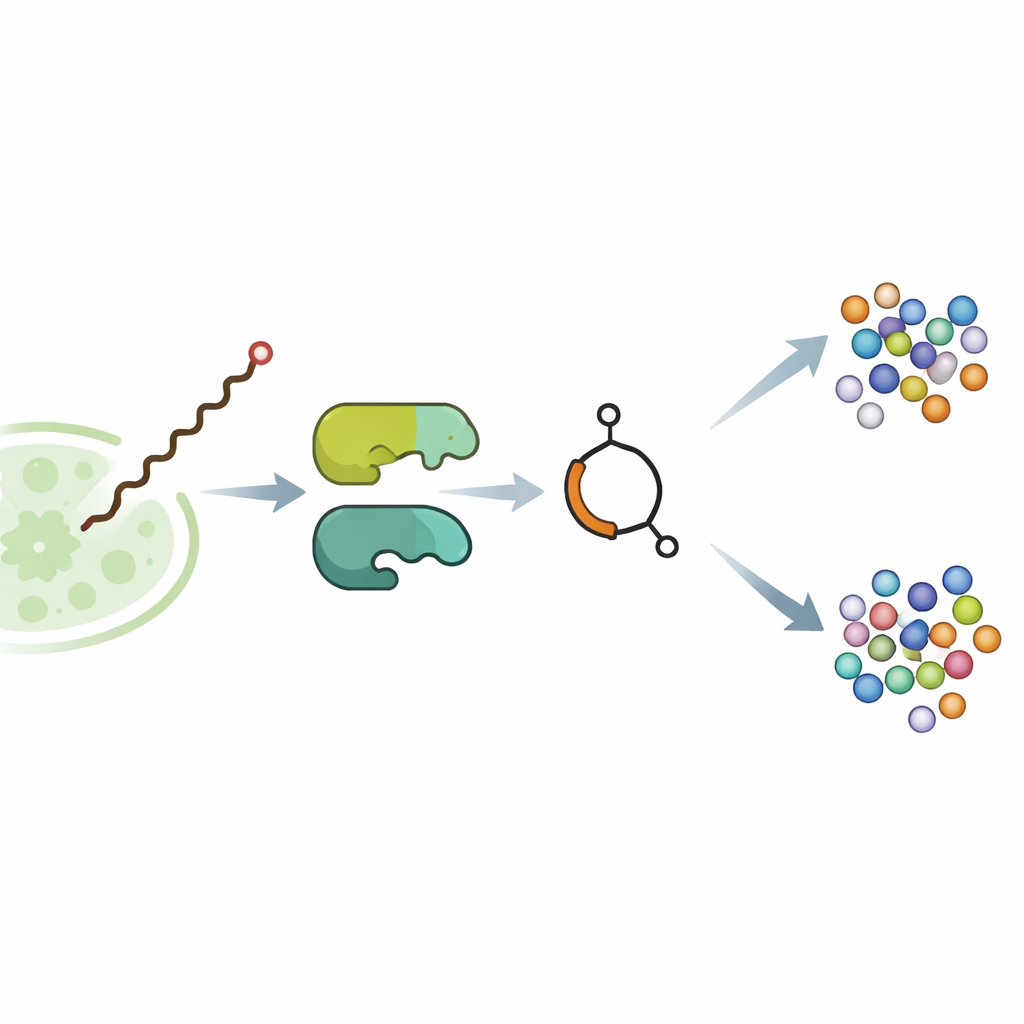
Ett enda enzym som gör tre jobb i följd
Studien överraskande kärna är SavA, ett flavin‑innehållande enzym som utför tre olika kemiska omvandlingar på en fettsyra‑liknande startbit hämtad från normal cellmetabolism. I provrörsreaktioner med noggrant syntetiserade mimetiska substrat visade forskarna att SavA först avlägsnar väteatomer för att införa en dubbelbindning, därefter tillför en syrehaltig grupp på en specifik position, och slutligen främjar kedjeavslutning till butenolidringen. Isotopexperiment med syre berikat i en tyngre form bekräftade att ringsyran kommer direkt från luften. Strukturell modellering och riktade mutationer pekade ut en enstaka aminosyra som basen som startar reaktionen, och visade hur den bundna flavin‑cofaktorn cyklar mellan oxiderad och reducerad form utan att förbrukas.
Ett avslutande enzym som finslipar sidokedjan
När SavA har byggt det kirala butenolid‑skelettet tar SavB — ett cytokrom P450‑enzym — över för att dekorera den bifogade kolkedjan. I närvaro av sina redoxpartners och en vanlig cellfaktor utför SavB en precis serie oxidationer vid två intilliggande kolatomer. Tidsupplöst analys avslöjade två intermediära molekyler: först en enkelhydroxylerad produkt, därefter en ketonform, innan den fullt funktionella avenoliden framträder. Kärnmagnetisk resonansmätning bekräftade positionerna och de tredimensionella arrangemangen av dessa nya grupper. Arbetet visar att SavB inför dessa syreatomer i en bestämd ordning och med strikt kontroll över orienteringen — en viktig egenskap för hormonets biologiska aktivitet. 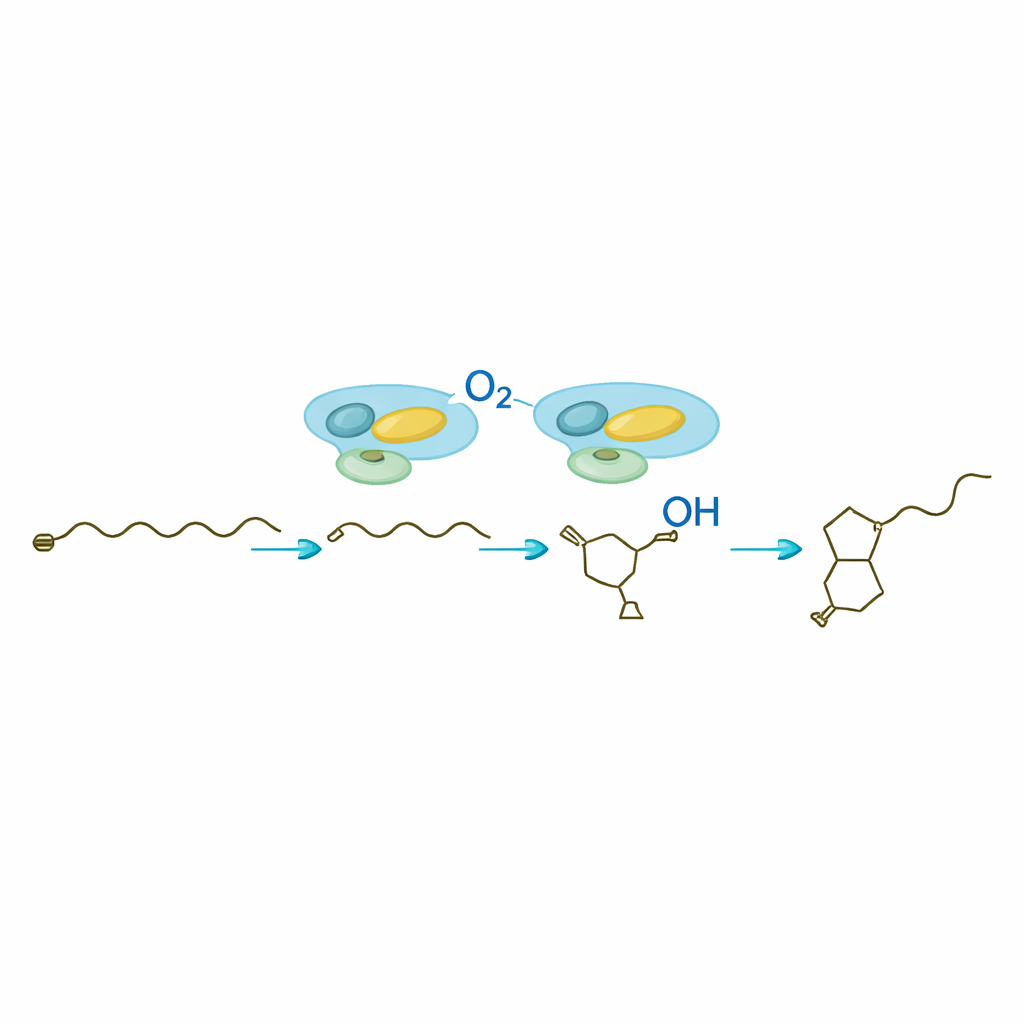
Gröna kemilektioner från bakteriella enzymer
Tillsammans omvandlar SavA och SavB ett vanligt byggblock härlett från fettsyror till en fint avvägd signalmolekyl med enbart syre från luften och vanliga cellulära hjälpämnen. Till skillnad från många industriella processer kräver SavA inga extra reducerande medel eller offerämnen; dess flavin‑cofaktor förflyttar endast elektroner medan substratet självt tillhandahåller drivkraften. Författarna lyfter fram SavA som en ny typ av mångbegåvat flavoprotein med stor potential som biokatalysator för hållbar tillverkning av butenolider och närliggande motiv. I praktiska termer skulle utnyttjande eller konstruktion av sådana enzymer en dag kunna göra det möjligt för fabriker — eller ingenjörsmodifierade mikrober — att framställa viktiga läkemedelsfragment och jordbruksprodukter från förnybara råvaror under milda förhållanden, vilket minskar både kostnader och miljöavtryck.
Citering: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Nyckelord: butenolidbiosyntes, flavoproteinet SavA, avenolid‑hormon, biokatalys, Streptomyces‑signalering