Clear Sky Science · sv
Degraderas av denguevirusets kapsidprotein uppvisar differentierad farmakologi jämfört med kapsid‑hämmare
Göra virusets skal till dess eget vapen
Denguefeber smittar hundratals miljoner människor varje år, men läkare saknar fortfarande tillförlitliga antivirala läkemedel för behandling. Denna studie undersöker ett nytt sätt att oskadliggöra denguevirus genom att förstöra ett av dess viktigaste byggstenar inne i infekterade celler, i stället för att bara försöka blockera dess funktion. Arbetet visar att noggrant utformade molekyler kan märka ett centralt virusprotein för avlägsnande av cellens eget avfallshanteringssystem, vilket minskar virusproduktionen och försvårar dess förmåga att undvika vårt immunsystem.
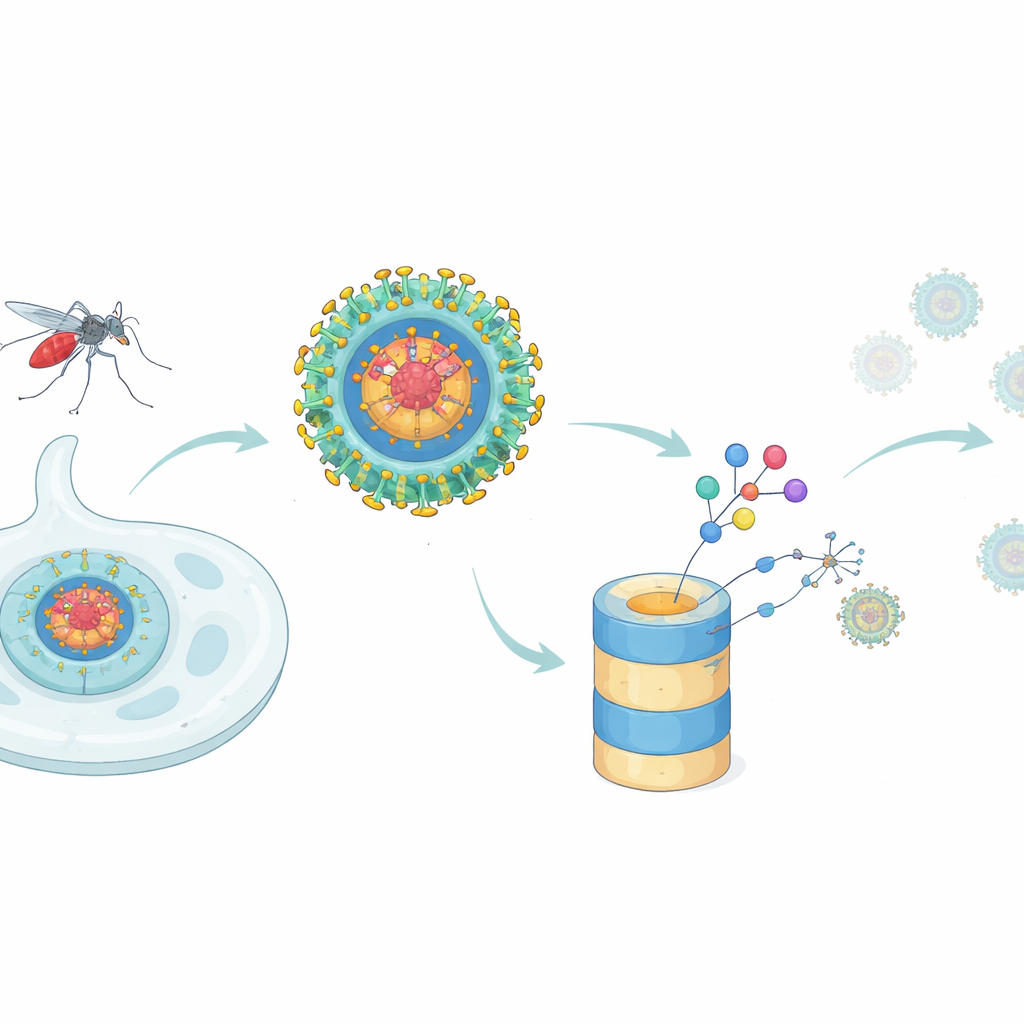
En ny taktik för att stoppa dengue
De flesta antivirala läkemedel fungerar som proppar i en maskin: de fäster på en funktionell plats på ett virusprotein och försöker blockera den. Detta tillvägagångssätt har problem när ett enskilt virusprotein utför många olika uppgifter eller när små mutationer försvagar läkemedlets grepp. Dengues kapsidprotein är ett tydligt exempel. Det bildar det inre skalet som paketerar virusets genetiska material i nya partiklar, men det påverkar också värdcellen genom att interagera med många mänskliga proteiner och genom att dämpa kroppens interferon‑svar, ett första försvar mot virus. Författarna frågade sig om ett nyare läkemedelskoncept — riktad proteinnedbrytning — skulle kunna gå längre än klassiska hämmare genom att faktiskt avlägsna kapsidproteinet från infekterade celler.
Designa en molekylär "prisjägare"
För att bygga en sådan degrader började forskarna från ST148, en känd liten molekyl som binder dengues kapsid och stör sammansättningen av nya viruspartiklar. De kopplade kemiskt ST148 till en andra modul som rekryterar ett mänskligt enzymkomplex ansvarigt för att märka proteiner för nedbrytning. De resulterande kimeriska molekylerna, kallade PROTACs, är formade för att greppa kapsiden i ena änden och ett E3‑ligascomplex i den andra, och föra dem samman så att kapsiden kan märkast med ubiquitin‑taggar och matas in i cellens proteasom, den huvudsakliga proteinmalaren. Genom att testa många länkarlängder och ligas‑rekryterande grupper identifierade de en särskild förening, döpt RPG‑01‑132, som pålitligt minskade kapsidnivåer i infekterade celler på ett sätt som var beroende av CRBN‑formen av ligaset och av normal proteasomfunktion.
Stoppa virusproduktion och immunneutrering
När de hade en fungerande degrader undersökte teamet vad den faktiskt gjorde mot dengueinfektion. I lever‑härledda celler infekterade med denguevirus orsakade RPG‑01‑132 en kraftig minskning av antalet infektiösa virus som släpptes ut, vid koncentrationer där den bara delvis sänkte den totala kapsidnivån. Viktigt var att andra virusproteiner och virus‑RNA förblev oförändrade, vilket visar att föreningen inte bara förgiftade den övergripande replikationen utan specifikt verkade genom förlust av kapsid. Elektronmikroskopi gav en visuell bekräftelse: celler behandlade med den ursprungliga hämmaren ST148 ackumulerade staplar av delvis bildade viruspartiklar i det endoplasmatiska retiklet, förenligt med ett hinder i montering, medan celler behandlade med degradaren visade nästan inga synliga virioner alls. Degradaren återställde också kapsidens förmåga att tysta interferon‑β‑signalering i ett rapportorsystem, vilket antyder att kapsidens icke‑strukturella roll i att oskadliggöra medfödd immunitet kan vändas genom att degraderas.
Besegra viral mångfald och läkemedelsresistens
Denguevirus finns i fyra huvudsakliga serotyper som skiljer sig i hur väl de svarar på kapsid‑riktade hämmare, och resistens kan uppstå genom enstaka mutationer. Författarna jämförde degradaren med ST148 över representativa stammar av alla fyra serotyperna och mot ett virus som bär en mutation (S34L i kapsiden) tidigare visad göra ST148 ineffektiv. Som förväntat fungerade ST148 bäst på en serotyp och förlorade aktivitet mot den resistenta mutanten. RPG‑01‑132, däremot, visade liknande antiviral potens över alla serotyper och behöll aktivitet mot S34L‑mutanten, samtidigt som den fortfarande verkade genom samma CRBN‑beroende degraderingsväg. Detta illustrerar en viktig fördel med "händelsestyrd" farmakologi: degradaren behöver inte sitta tätt på varje kapsidmolekyl hela tiden, så länge den kan utlösa tillräckligt många degraderingshändelser för att rubba balansen.
Vad detta innebär för framtida denguebehandlingar
Studien visar att dengues kapsidprotein kan angripas inte bara som en strukturell komponent i viruset utan som en avtagbar nav som stöder flera steg av infektion och immunneutrering. Genom att omvandla en traditionell hämmare till en degrader skapade forskarna en förening som blockerar virusproduktion, lyfter en del av virusets undertryckande av den medfödda immuniteten och förblir effektiv över olika virusstammar och en känd resistensmutation. RPG‑01‑132 i sig kommer behöva optimering — bättre cellinträde, starkare aktivitet i djurmodeller och noggranna säkerhetskontroller — men det ger ett övertygande bevis på konceptet. Mer i allmänhet tyder arbetet på att kapning av cellens egen avfallsmekanism kan öppna nya vägar för antivirala läkemedel som är svårare för virus att undvika och som kan neutralisera proteiner med många olika roller i infekterade celler.
Citering: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
Nyckelord: denguevirus, kapsidprotein, riktad proteinnedbrytning, antiviral läkemedelsdesign, PROTACs