Clear Sky Science · sv
Kooperativ aktivering av anjon vid en koboltcentrum genom jonparning och liganddesign
Varför små partner runt metaller spelar roll
Kemister fokuserar ofta på huvud"skådespelaren" i en reaktion — en metallatom som hjälper till att bryta och bilda bindningar. Men denna artikel visar att de tysta medspelarna som svävar i närheten, osynliga för blotta ögat, kan förändra vad metallen gör helt. Genom att noggrant forma omgivningen runt en koboltatom visar författarna hur två nästan utbytbara anjoner, ofta betraktade som passiva åskådare i kemi och batterier, kan leda till skarpt olika utfall. 
Bygga en skräddarsydd ficka runt kobolt
Forskarna konstruerade ett burliknande organiskt ramverk kallat Py4Im som omsluter en koboltjon tätt. Detta ramverk är uppbyggt av flera sammanlänkade pyridinkringar och en imidazolidinenhet, som tillsammans skapar en styv, skålformad kavitet med en enskild N–H‑grupp. Den lilla kaviteten är "protonisk", vilket innebär att den kan bilda vätebindningar, och den pekar i en bestämd riktning, som en liten dokningsficka för inkommande anjoner. När kobolt monteras med denna ligand bildas en familj av positivt laddade komplex vars övergripande form och inre ficka förblir densamma medan motjonen — den negativt laddade partnern — kan bytas ut. Detta gör systemet till en idealisk testbädd för att se hur olika anjoner beter sig i samma kontrollerade miljö.
Två lika anjoner, två mycket olika beteenden
Teamet jämförde två arbetsamma anjoner, tetrafluoroborat (BF4−) och hexafluorofosfat (PF6−), som är vida använda som så kallade svagt koordinerande anjoner. De är populära eftersom de vanligtvis håller avstånd till metalls centra, vilket hjälper till att stabilisera starkt laddade arter utan att involveras direkt. Överraskande nog beter de sig inte likadant inne i Py4Im‑kavitten. Under milda förhållanden donerar PF6− en fluoridjon till kobolt, bryter en stark P–F‑bindning och bildar ett väl definierat kobolt–fluoridkomplex. I kontrast vägrar BF4−, som vanligtvis anses vara den mer "spröda" av de två, att lämna ifrån sig fluorid i samma miljö. Istället intar den en stabil arrangemang bunden till koboltcentret utan att fullfölja bindningsbrytningen.
Att iaktta hur joner parar sig och rör sig
För att förstå dessa kontrasterande beteenden använde författarna en kombination av högupplöst NMR‑teknik och kvantkemiska beräkningar. Diffusions‑NMR‑experiment mätte hur snabbt de positiva och negativa arterna rör sig i lösning, vilket avslöjar hur tätt de är parade. Dessa mätningar visade att BF4− bildar ett närmare, mer bestående jonpar med koboltkomplexet än vad PF6− gör. Py4Im‑kaviteten positionerar anjonen direkt under imidazolidinringen, där vätebindningar från N–H och närliggande C–H‑grupper håller den på plats. Datorberäkningar bekräftade att denna starkare, riktade parning med BF4− stabiliserar starttillståndet så mycket att brytning av B–F‑bindningen blir något ofördelaktig, även om den bindningen i sig är svagare än P–F‑bindningen i PF6−. PF6−, som parar mer löst, kan närma sig, överföra fluorid till kobolt och avvika som PF5, vilket leder till ett fluoridbärande koboltkomplex som är termodynamiskt tillgängligt. 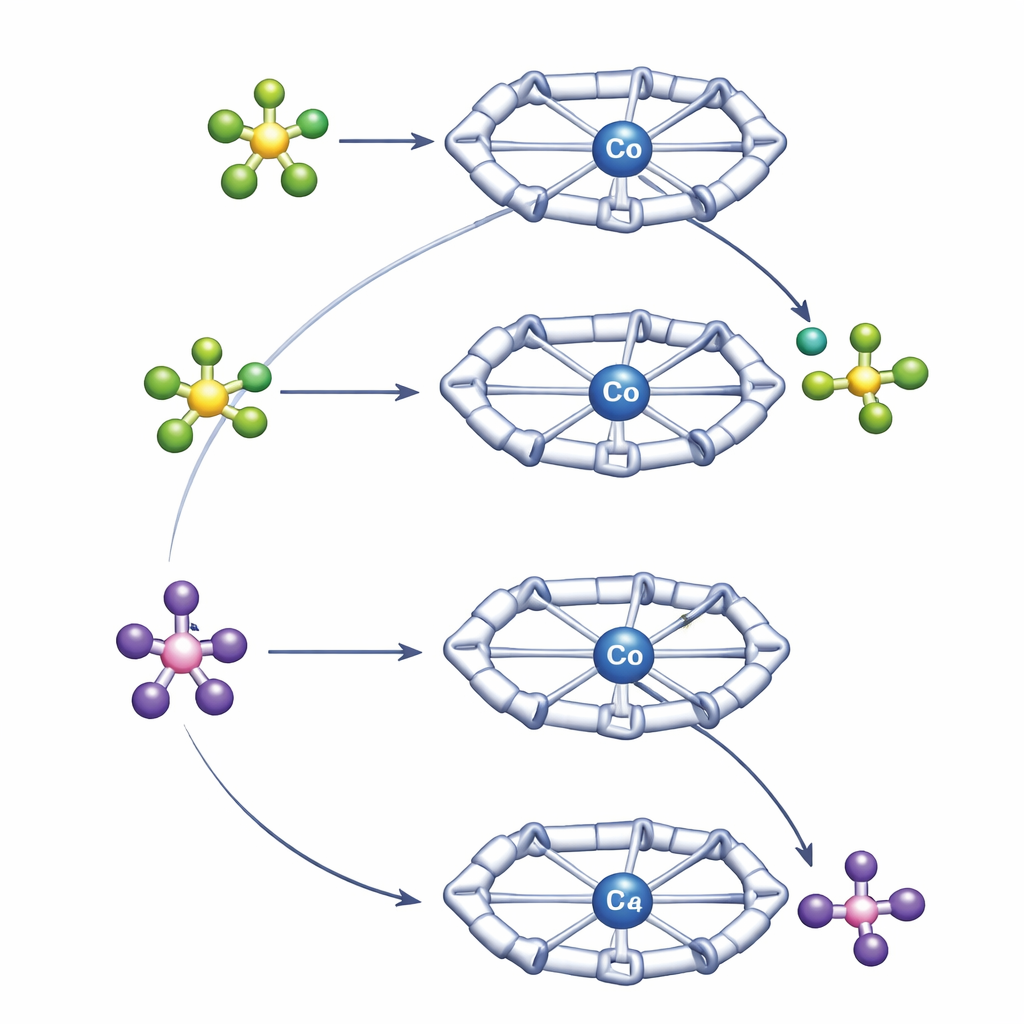
Att göra en bunden fluorid till ett användbart verktyg
När kobolt–fluoridkomplexet väl bildats är det inte ett dött slut. Författarna visar att det fungerar som en nukleofil fluoridkälla — enklare uttryckt kan det leverera fluorid till positivt laddade eller elektronfattiga partner. I lösning överför denna kobolt–fluoridart rent fluorid till reaktiva kolcentra, till kiselatomer i klorosilaner och till acylklorider, vilket genererar organiska fluorider medan koboltkomplexet växlar tillbaka till sin kloridform eller binder den nya partnern. I en smart vändning demonstrerar teamet också att BF4− kan övertalas att avge fluorid om en separat bas finns närvarande för att "fånga" den återstående BF3‑fragmentet. Detta omvandlar den annars motvilliga BF4−‑vägen till en som också ger samma kobolt–fluoridprodukt.
Vad detta betyder för att designa smartare katalysatorer
För en icke‑specialist är huvudbudskapet att joner som tidigare behandlats som tröga bakgrundssalter faktiskt kan styra kemiska reaktioner på kraftfulla sätt. Genom att skulptera en precis ficka runt ett metallcentrum och kontrollera hur tätt anjoner parar med det, vände författarna den förväntade reaktiviteten hos två nästan identiska arter. PF6−, normalt betraktad som mycket robust, blir den lättare källan till fluorid, medan BF4− låses fast av starkare parning om inte systemet får hjälp. Detta arbete ger en ritning för att använda liganddesign och motjonsval tillsammans för att finjustera hur reaktivt ett metallkomplex är — en idé som kan påverka områden från homogen katalys till elektrolytdesign för avancerade batterier, där de "tysta partnerna" i lösningen kanske alls inte är passiva.
Citering: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Nyckelord: koboltkomplex, svagt koordinerande anjoner, fluoridöverföring, jonparning, liganddesign