Clear Sky Science · sv
Metalliskt molybdenulfid katalyserar protometaboliska koldioxidreaktionsnätverk under extrema förhållanden
Hur berg kan ha kickstartat livets kemi
Långt innan levande celler utvecklade enzymer behövde jorden fortfarande sätt att omvandla enkla gaser som koldioxid till de organiska molekyler som livet är beroende av. Denna studie undersöker om vissa naturligt förekommande mineraler, liknande dem som hittas vid undervattensvarma källor, kan ha fungerat som primitiva ”kemiska motorer”. Genom att visa att en metallisk form av molybdenulfid kan omvandla koldioxid till ett överraskande rikt nätverk av organiska föreningar ger arbetet ett konkret scenario för hur livets kärnkemier kan ha börjat på en livlös planet.

Varma källor och dolda kemiska motorer
Modernt liv drivs av invecklade reaktionsnätverk som förflyttar kol genom celler och ekosystem. Dessa nätverk förlitar sig på proteiner kallade enzymer, som i sig är produkter av evolution. Den stora frågan är vad som fanns före dem. Författarna riktade blicken mot hydrotermala källor—naturliga heta vattenpelare på havsbotten rika på metalsulfider och vätegas—som troliga miljöer för den tidigaste kolkemi. På sådana platser möter hett, pressat vatten berg som innehåller metaller som järn, nickel och molybden. Tidigare experiment har visat att några av dessa metaller kan omvandla koldioxid till små organiska molekyler, men oftast bara längs fragment av livets vägar, inte fullständiga nätverk.
Ett mineral som imiterar forntida enzymer
Teamet fokuserade på en särskild form av molybdenulfid, kallad 1T′-fasen, vars atomarrangemang efterliknar metall–svavel-centra som finns i moderna enzymer som bearbetar koldioxid. Under hög temperatur och tryck i vatten, med väte som bränsle, katalyserade detta mineral omvandlingen av löst koldioxid (modellerat som vätekarbonat) till ett oväntat brett spektrum av organiska syror. Genom att omsorgsfullt variera temperatur, reaktionstid och gastryck, och genom att spåra produkter med kromatografi, massespektrometri och NMR, identifierade de 32 olika intermediärer och slutprodukter som uppstod från samma enkla kolkälla.
Återuppbygga livets centrala kolförlopp utan enzymer
Dessa 32 föreningar är inte slumpmässiga. Många är samma molekyler som utgör kärnan i modern metabolism—såsom acetat, pyruvat, oxaloacetat, succinat och alfa-ketoglutarat. Tillsammans kan de kartläggas på fem stora kolfixeringsvägar som nutida mikrober använder: acetyl–CoA-vägen och varianter av Krebs-cykeln och relaterade slingor. I experimenten framträdde dessa vägar som ett sammankopplat nätverk: acetat länkar flera cykler; större molekyler bryts ner och byggs upp igen; och viktiga intermediärer försvinner och dyker upp igen när förhållandena förändras. Bildandet av flerkoliga syror nådde hög effektivitet, upp till omkring 70 % av det omvandlade kolet hamnade i molekyler med två eller fler kolatomer. Reaktionsnätverket visade även svängningar där mängderna av vissa produkter ökade och minskade över tid, vilket ekar levande kemiska systemens dynamiska beteende.
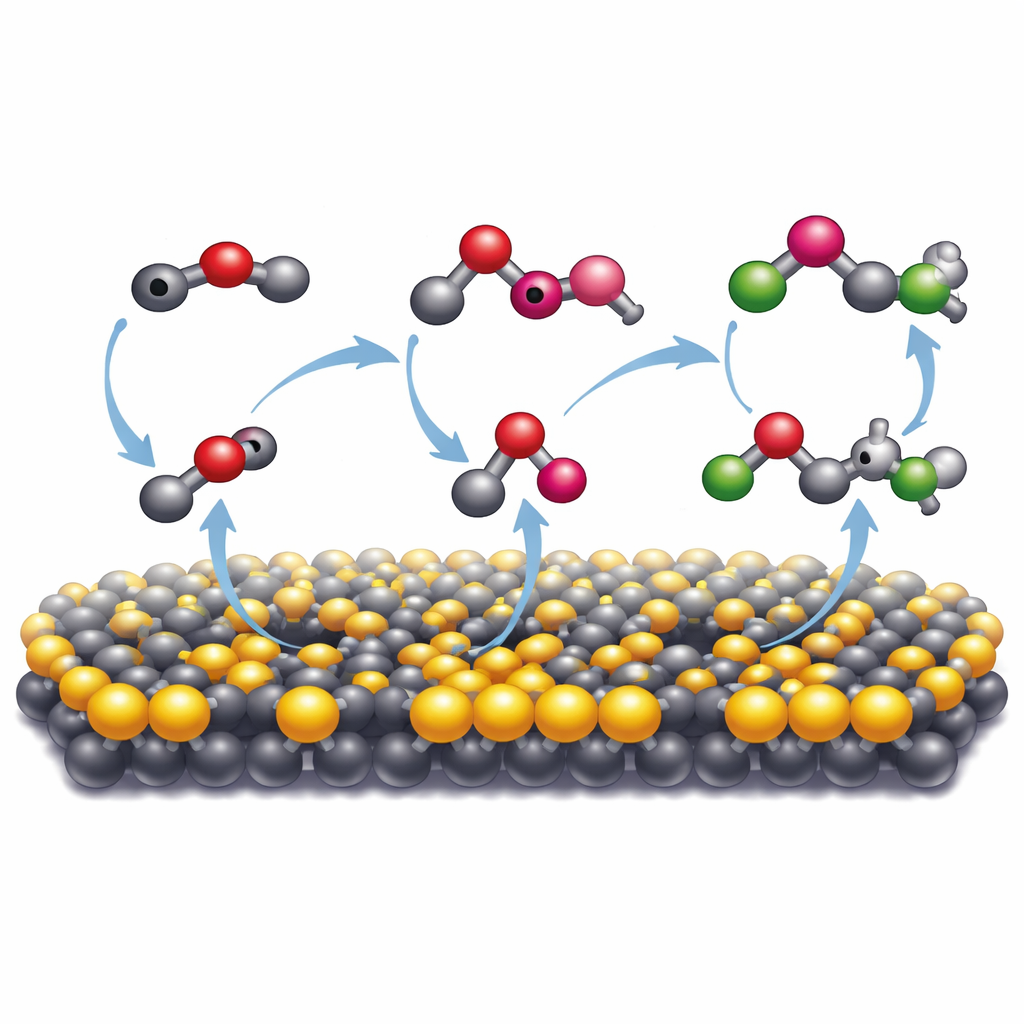
Hur mineralet får kolatomer att förena sig
För att förstå varför detta särskilda mineral var så effektivt jämförde forskarna det med en vanligare form av molybdenulfid som har en annan atomstruktur. Endast den metalliska, förvrängda formen—with många saknade svavelatomer—driv omfattande bildning av större organiska molekyler. Spektroskopiska tekniker avslöjade att på denna yta binder kolmonoxid, härledd från koldioxid, starkt och reduceras vidare till högreaktiva fragment, eller radikaler. Dessa radikaler stabiliseras precis tillräckligt på mineralsytan för att kollidera med varandra och bilda nya kol–kol-bindningar. Elektronspinnmätningar bekräftade närvaron av sådana radikaler, och tillsats av ett radikalfångstämne undertryckte kraftigt flerkolprodukterna. Datorsimuleringar stöder denna bild och visar att svavelvakanser och den förändrade elektroniska strukturen i 1T′-fasen gör det lättare för ytan att donera elektroner och att föra kolfragment nära varandra så att de kan kombineras.
Från stenkemi till den första metabolismen
Tillsammans tyder dessa fynd på att vissa metalsulfidmineraler på den tidiga jorden kan ha drivit komplex, självorganiserande kolkemi långt innan enzymer existerade. I hydrotermala miljöer, där heta, väterika vätskor möter koldioxid och metallbärande berg, kunde ett mineral som 1T′-molybdenulfid kontinuerligt omvandla oorganiskt kol till ett nätverk av sammankopplade organiska vägar som liknar moderna metabola cykler. För en icke-specialist är huvudbudskapet att livets centrala kemi kanske inte behövde livet för att komma igång: under rätt förhållanden kan enkla stenar, vatten och gas spontant bygga många av samma molekyler och reaktionsslingor som levande celler fortfarande använder idag.
Citering: Chen, P., Liu, X., He, D. et al. Metallic molybdenum sulfide catalyses protometabolic carbon dioxide reaction networks under extreme conditions. Nat Commun 17, 2395 (2026). https://doi.org/10.1038/s41467-026-69255-w
Nyckelord: livets uppkomst, prebiotisk kemi, hydrotermala källor, koldioxidfixering, molybdenulfid