Clear Sky Science · sv
Tolkbara och generativa djupinlärningsmodeller förklarar fasseparerande intrinsiskt oordnade motiv
Varför små proteinkomponenter spelar roll
Inuti varje cell samlas viktiga molekyler ofta i droppformiga skikt kallade biomolekylära kondensat. Dessa droppar hjälper till att organisera kemin utan membranväggar, och påverkar hur gener slås på, hur signaler överförs och hur celler svarar på stress. Många sådana droppar bildas av flexibla proteinsträckor kända som intrinsiskt oordnade regioner. Ändå har biologer fortfarande svårt att peka ut de korta sekvenserna som faktiskt får dessa droppar att bildas. Denna studie presenterar ett djupinlärningsramverk, PhaSeMotif, som både kan hitta dessa nyckelsegment och designa nya sådana, vilket ger forskare ett kraftfullt nytt sätt att undersöka och omprogrammera cellulära droppar.
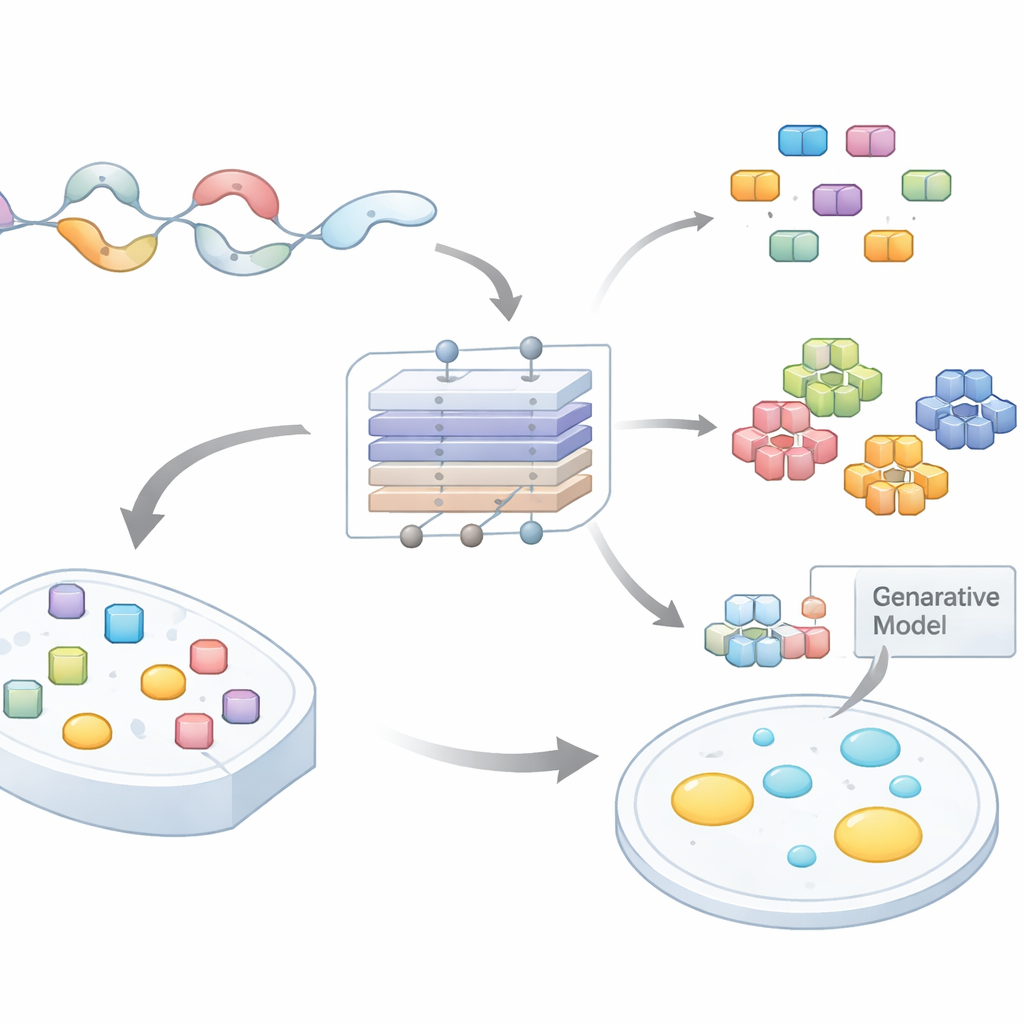
Från röriga proteintailar till testbara hypoteser
Många proteiner innehåller långa, flexibla svansar som inte viks till fasta former. Dessa oordnade regioner är berikade i vissa aminosyror och hyser ofta upprepade mönster eller korta motiv. En växande mängd forskning visar att sådana motiv driver kondensation genom att möjliggöra många svaga interaktioner samtidigt. Att skanna hela proteomer för att hitta vilka korta sträckor som är viktiga — och varför — har dock varit en stor flaskhals. Befintliga beräkningsverktyg bedömer vanligtvis hela proteiner eller stora regioner och ger lite vägledning om var man ska mutera eller vad som bör testas i labbet. Författarna ville bygga en modell som inte bara förutsäger om en oordnad region kan bilda droppar, utan också vilka exakta subsekvenser som utför huvudjobbet.
En djupinlärningskarta över droppdrivande motiv
Teamet sammanställde stora dataset av oordnade regioner från flera arter och märkte dem efter om deras värdproteiner sannolikt genomgick fass separation. De tränade sedan ett uppmärksamhetsbaserat neuralt nätverk, PhaSeMotif, som tar en aminosyrasekvens av godtycklig längd och ger en poäng för droppbildningsförmåga. Avgörande är att nätverket använder en kombination av konvolutionslager och attentionmekanismer för att bedöma hur mycket varje kort fönster i sekvensen bidrar till den poängen. Genom att spåra tillbaka genom modellen (med tekniker liknande guidad backpropagation) extraherade författarna högt viktade fragment — korta motiv ofta under 20 rester — som modellen ansåg vara väsentliga för droppbildning.
Sätta förutsägelser på prov i levande celler
För att se om dessa motiv verkligen spelade roll vände forskarna sig till ett ljustaktiverat system i mänskliga celler. De fäste förutsagda droppbildande oordnade regioner vid en ljuskänslig oligomeriseringsmodul och en fluorescerande tagg. Under blått ljus kondenserade dessa konstruktioner snabbt till ljusa punkter och rapporterade fass separation i realtid. Teamet tog sedan bort enskilda motiv genom att ersätta dem med neutrala, flexibla länkar av samma längd. I 82 % av de 17 förändrade sekvenser som testades försvagades droppbildningen dramatiskt eller försvann helt, medan kontrollmutationer utanför PhaSeMotif-segment ofta hade liten effekt. Viktigt är att många av dessa nyckelmotiv överlappade med platser där sjukdomsassocierade mutationer är kända för att störa kondensation, vilket understryker deras biologiska relevans.
Att avslöja ett vokabulär av motvityper
Med mer än 17 000 motiv i handen frågade författarna nästa om det fanns vanliga "smaker" av droppdrivande segment. De analyserade aminosyrasammansättning och mönster och klustrade sedan motiven i nio grupper. Vissa kluster var rika på aromatiska rester och glycin, förenligt med klibbiga π–π- och kation–π-interaktioner. Andra innehöll separata fläckar av positiva och negativa laddningar, vilket gynnar elektrostatiska attraktioner och selektiv partitionering till särskilda kondensat. Ytterligare kluster dominerades av prolin och glycin, som stödjer flexibilitet, eller av långa repeterade glutaminsekvenser som kan bilda täta nätverk av vätebindningar. Olika cellulära kompartment och kondensattyper visade karakteristiska blandningar av dessa motvityper, vilket antyder att motivens sammansättning hjälper bestämma var och med vilka partner ett protein kommer att kondensere.
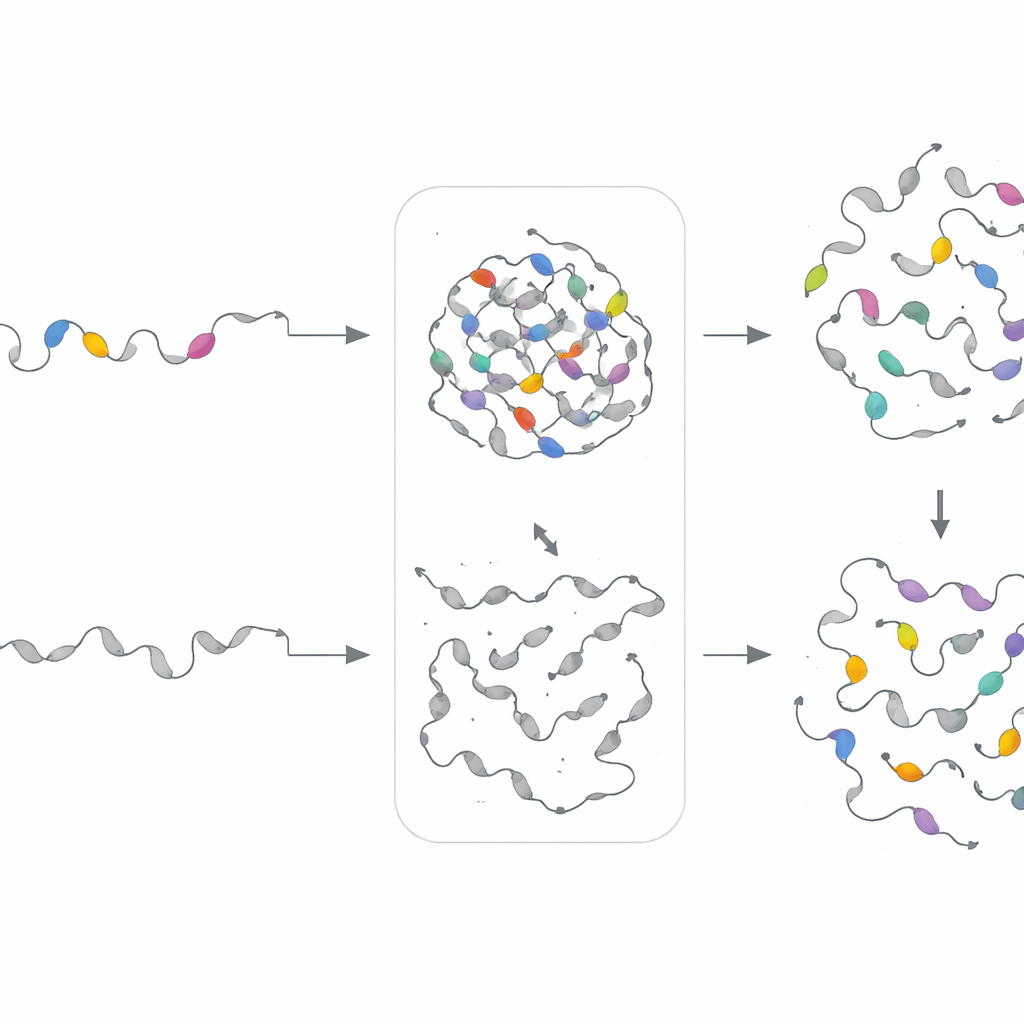
Designa nya motiv för att bevisa reglerna
För att testa om motivets "recept" — snarare än exakta sekvenser — styr droppbeteendet byggde teamet separata generativa modeller för varje motivkluster. Dessa variational autoencoders lärde sig de statistiska mönstren för ett givet kluster och producerade sedan nya, artificiella sekvenser med samma sammansättningsfingeravtryck men annan exakt ordning. Forskarna bytte experimentellt in dessa syntetiska motiv i proteiner där de ursprungliga segmenten hade tagits bort. Anmärkningsvärt återställde de konstruerade motiven i 18 av 21 fall fass separation i celler, ibland till och med justerande hastigheten eller densiteten i droppbildningen. Detta visar att PhaSeMotif fångar underliggande designregler som kan återanvändas för att bygga eller reparera droppbildande regioner.
Vad detta betyder för biologi och sjukdom
Genom att länka tolkbar djupinlärning med generativ design och direkta cellulära tester förvandlar detta arbete den vaga idén om "oordnade droppbildande regioner" till en konkret uppsättning korta, komponerbara motiv. För icke-experter är slutsatsen att forskare nu kan läsa och skriva de små proteinkomponenter som styr hur cellulära droppar monteras, blandas och går fel. Detta öppnar dörren för snabbare upptäckt av sjukdomsframkallande mutationer i dessa segment, tydligare mekanistiska studier av hur kondensat organiserar cellfysiologi och så småningom rationell ingenjörskonst av proteiner som styr droppar för terapeutiska eller syntetiska biologitillämpningar.
Citering: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
Nyckelord: biomolekylära kondensat, intrinsiskt oordnade proteiner, fasseparation, djupinlärning, proteinmotiv