Clear Sky Science · sv
Hepatocyter funktionellt omprogrammerade av KIAA1199-höga kolorektala cancerceller gynnar ansamling av pro-metastatiska Egr1+ neutrofiler
När koloncancer siktar på levern
De flesta föreställer sig att cancer sprider sig när avvikande celler lossnar och driver till nya organ. Denna studie berättar en mer oroande historia: kolorektala (colon) tumörer kan tyst omprogrammera levern långt innan några cancerceller anländer och bygga en välkomnande ”jordmån” där framtida tumörer lätt kan slå rot. Att förstå denna dolda förberedelsefas kan öppna dörren för behandlingar som stoppar levermetastaser – huvudorsaken till död vid kolorektal cancer – innan de ens börjar.
En smygande uppbyggnad innan tumörerna anländer
Kolorektal cancer sprider sig ofta till levern, men bara vissa tumörer gör det aggressivt. Författarna fokuserade på ett molekylärt protein kallat KIAA1199, som är rikligt uttryckt i högriskkolorektala cancerformer. I musmodeller och patientprover visade tumörer med högt KIAA1199 inte bara snabbare tillväxt; de förbereddes också levern till att bli en ”pre-metastatisk nisch”, ett mikromiljö som är ovanligt gästvänligt för inkommande cancerceller. Även när levermetastaser experimentellt såddes inifrån en separat källa utvecklade djur med KIAA1199-höga colonstumörer mycket fler levermetastaser och dog tidigare. Det visade att signaler från primärtumören, inte bara vandrande cancerceller, omformade levern i förväg.
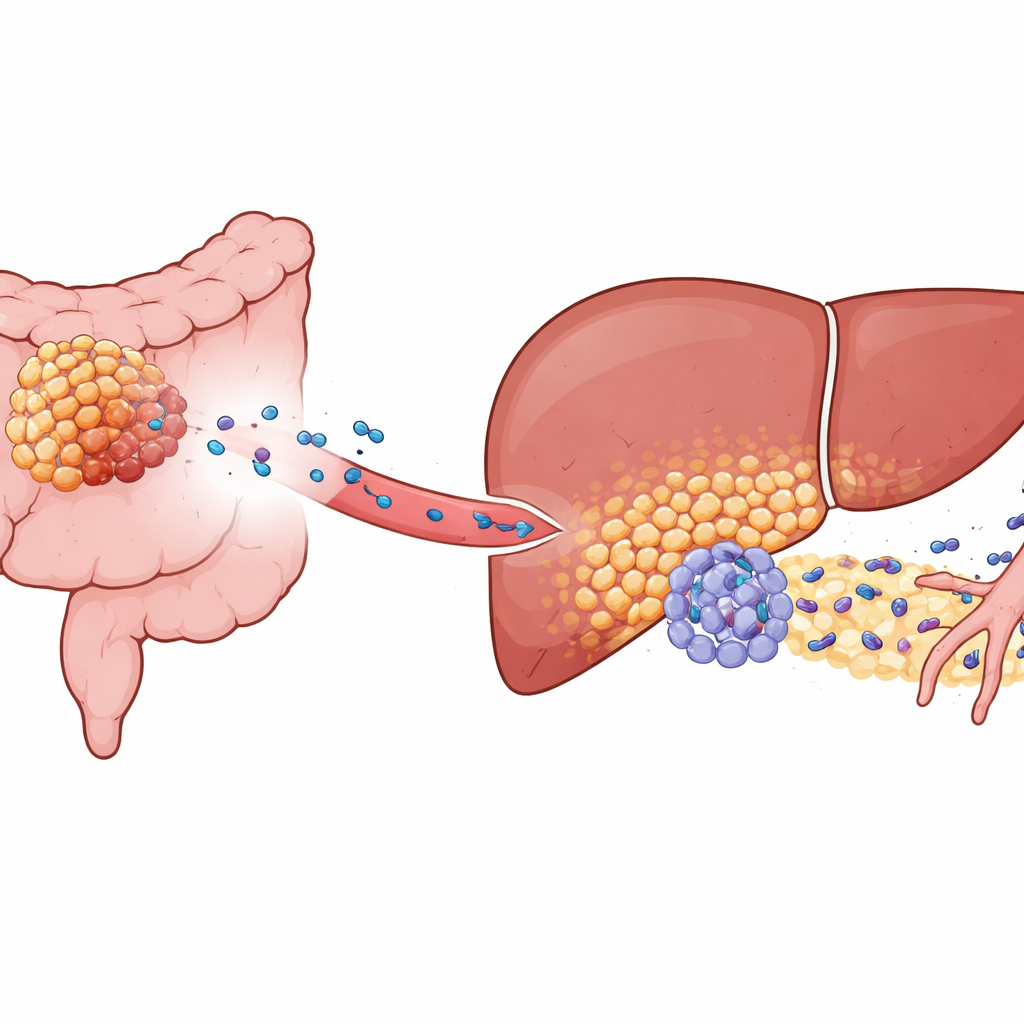
Leverceller omprogrammerade till tumörhjälpare
Genom att gå djupare använde forskarna single-cell-sekvensering och spatial kartläggning för att undersöka levertissue med hög upplösning. De fann en distinkt undergrupp av hepatocyter—normalt leverns arbetsmyror—som blivit ”funktionellt omprogrammerade.” Dessa celler dök bara upp när KIAA1199-höga tumörer fanns närvarande. Istället för att tyst sköta metabolismen övergick de förändrade hepatocyterna till en mer malignliknande metabolisk profil och dämpade en skyddande regulator kallad PPARγ, som vanligtvis hjälper till att hålla inflammation och stressrespons i schack. Med PPARγ undertryckt började dessa hepatocyter producera höga nivåer av ett protein kallat SAA2, som de släppte ut i sin omgivning, särskilt vid gränsen där levertissue möter invaderande tumörceller.
Förvandla vanliga försvarare till pro-metastatiska neutrofiler
Neutrofiler—vita blodkroppar mest kända för att bekämpa infektioner—betecknade sig också märkligt i denna förberedda lever. Författarna identifierade en särskild undergrupp med ett ”Egr1+” signaturmönster, namngivet efter en transkriptionsfaktor som omformar hur dessa celler fungerar. Istället för att anlända från blodomloppet redan förändrade verkade neutrofiler omutbildas lokalt av de omprogrammerade hepatocyterna. SAA2 som frigjordes från hepatocyterna band till en receptor kallad FPR2 på närliggande neutrofiler och slog på en intern PI3K-AKT-signalväg som stabiliserade Egr1-aktivitet. Resultatet var längrelevande, högaktiv neutrofiler som utsöndrade stora mängder VEGFA, en potent drivare av nyskapande blodkärl. Dessa Egr1+ neutrofiler klustrade sig vid tumör–leverkanten, precis där nya, sköra blodkärl grodde fram.
Bygga blodkärl som välkomnar tumörceller
Studien visar att dessa omutbildade neutrofiler inte är åskådare—de omformar aktivt leverns kärlstruktur. I cellkultur gjorde faktorer som släpptes av Egr1+ neutrofiler att endotelceller växte, migrerade och formade rörlika strukturer som påminde om nya kärl. I möss ökade tillförsel av Egr1+ neutrofiler levermetastaser och skyndade upp döden. Att blockera nyckelsteg i kedjan—antingen SAA2–FPR2-signalen till neutrofiler eller den nedströms PI3K-AKT-vägen—skar av neutrofilernas överlevnad och VEGFA-produktion, vilket minskade kärltillväxt och metastatisk spridning. På samma sätt minskade återställande av PPARγ-aktivitet i hepatocyter med diabetesläkemedlet rosiglitazon SAA2-nivåerna, hämmade uppkomsten av Egr1+ neutrofiler och reducerade kraftigt levermetastaser i prekliniska modeller.
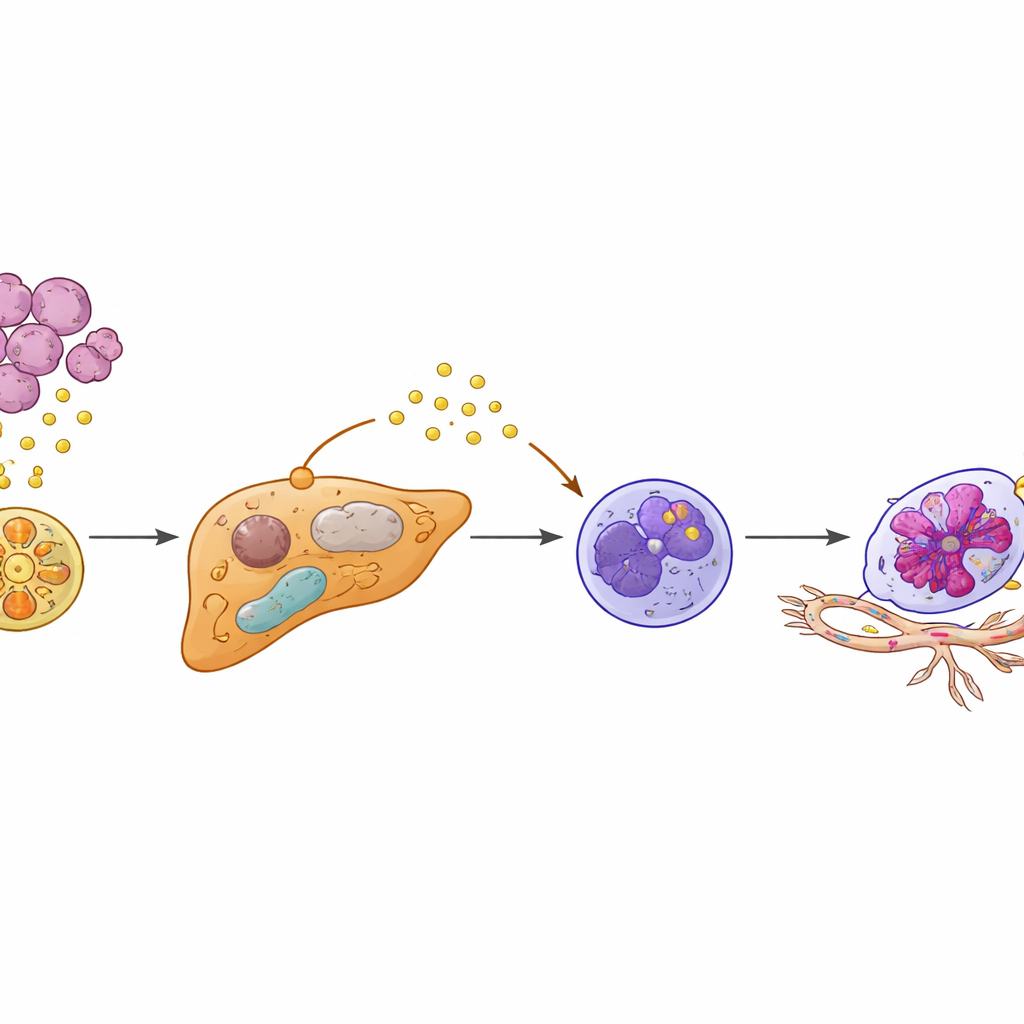
Från mekanism till förutsägelse och prevention
Eftersom KIAA1199 i tumörer och SAA2 i levern ligger högt upp i denna kaskad testade författarna om dessa proteiner kunde hjälpa till att flagga patienter med hög risk för levermetastas. I flera patientkohorter var personer med höga blodnivåer av båda markörerna mycket mer benägna att utveckla levermetastaser och att göra det snabbare. Ett enkelt kombinerat KIAA1199–SAA2-poäng överträffade vardera markören för sig i att förutsäga risk och paketades in i en klinisk nomogram som uppskattar en enskild patients sannolikhet för leverutbredning under de kommande två åren. Tillsammans målar fynden upp en tydlig bild: KIAA1199-höga coloncancer skickar ut vesikelburna signaler som omkopplar hepatocyter, vilka i sin tur omvandlar närliggande neutrofiler till långlivade, kärlbyggande medbrottslingar. Genom att rikta in sig på denna KIAA1199–PPARγ/SAA2–Egr1-axel—genom metabola läkemedel, immunmodulerande medel eller båda—kan det bli möjligt att inte bara behandla befintliga levermetastaser utan att förhindra att de överhuvudtaget fäster sig.
Citering: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Nyckelord: kolorektal cancer levermetastas, pre-metastatisk nisch, neutrofiler, hepatocytomprogrammering, tumörmikromiljö