Clear Sky Science · sv
Minskad metylering av histon 3.3 lysin 4 i mediala ganglionära eminensen och hypotalamus återger fenotyper vid neurodevelopmentella störningar
Hur små kemiska markörer formar hjärna och kropp
Varför orsakar vissa genetiska förändringar både inlärningssvårigheter och ovanlig tillväxt, som att vara mycket liten under barndomen men överviktig som vuxen? Den här studien undersöker små kemiska markörer på DNA-packningsproteiner i hjärnan och visar hur störningar i endast två nyckelregioner kan sprida sig till anfall, ångestliknande beteende, minnesproblem och dramatiska förändringar i kroppsstorlek hos möss.
Brytare på genomets dimmerknappar
Inuti varje hjärncell är DNA lindat runt spolliknande proteiner som kallas histoner. Kemiska märken på dessa histoner fungerar som dimmerknappar som vrider upp eller ner grupper av gener. Ett sådant märke, lagt på en plats kallad H3K4, är starkt kopplat till att slå på gener. Mänskliga genetiska studier har visat att personer som föds med fel i enzymer som lägger till eller tar bort detta märke ofta har neurodevelopmentella störningar som kombinerar intellektuell funktionsnedsättning, epilepsi och onormal kroppstillväxt. Det har dock varit oklart vilka hjärnceller som är mest känsliga för denna störning och hur deras funktionsnedsättning kan förena hjärnans excitabilitet med hela kroppens metabolism.
Riktade på två kritiska hjärnhubbar
Forskarna konstruerade möss där en mutant version av ett histonprotein (H3.3K4M) aktiverades endast i celler som härrörde från två embryonala hjärnregioner: den mediala ganglionära eminensen, som producerar många av hjärnans inhibitoriska ”broms”-celler, och den utvecklande hypotalamus, som hjälper till att reglera aptit, hormoner och energibalans. Denna mutation blockerar specifikt H3K4-metylering utan att eliminera histonerna själva. Tester bekräftade att det mutanta proteinet var utbrett i de riktade områdena och att normala H3K4-markörer var starkt reducerade där samtidigt som de övergripande histonnivåerna förblev stabila. Denna design efterliknar många mänskliga tillstånd där endast en kopia av ett H3K4-relaterat genfel är defekt, snarare än helt frånvarande.
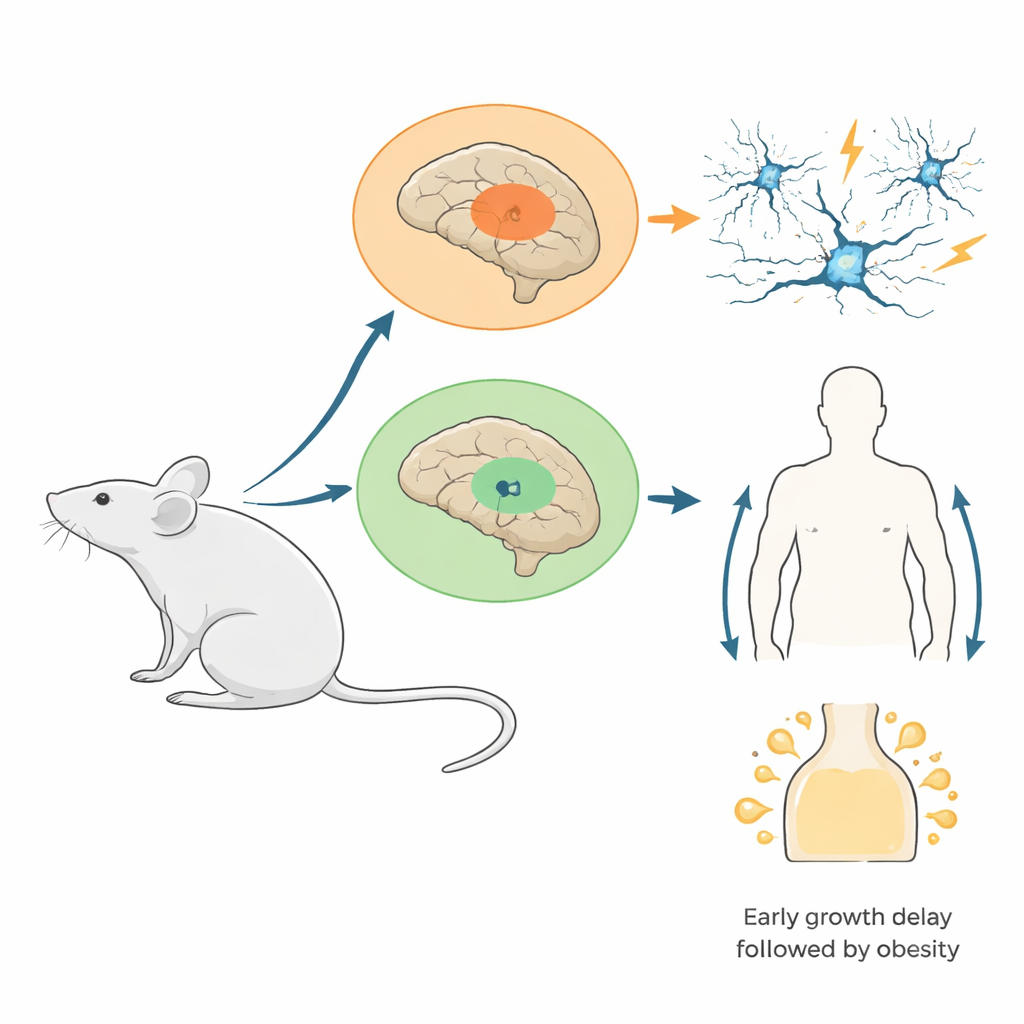
Från saknade bromsceller till anfallsbenägna kretsar
När dessa möss växte fram blev konsekvenserna för hjärnkretsarna tydliga. Unga mutanter hade färre inhibitoriska interneuroner i cortex och hippocampus, särskilt en snabbt fyrande typ som normalt håller neurala rytmer strikt tidsinställda. Detaljerade inspelningar visade att kvarvarande interneuroner fanns men var mer variabla i sina elektriska egenskaper, vilket tyder på att deras mognad var störd. När hippocampus stimulerades i hjärnskivor var de vanliga högfrekventa ”gamma”-oscillationerna — elektriska rytmer kopplade till informationsbearbetning — svagare och långsammare, och onormala burstliknande händelser dök upp. I levande djur utvecklade många mutanter, särskilt honor, spontana anfall och var mycket mer känsliga för läkemedelsinducerade anfall. Tidigt i utvecklingen spårade teamet denna cellförlust huvudsakligen till bristfällig migration av interneuroner in i cortex, inte till ökad celldöd eller minskad celldelning.
Omskrivning av genaktivitet i anfallsrelaterade celler
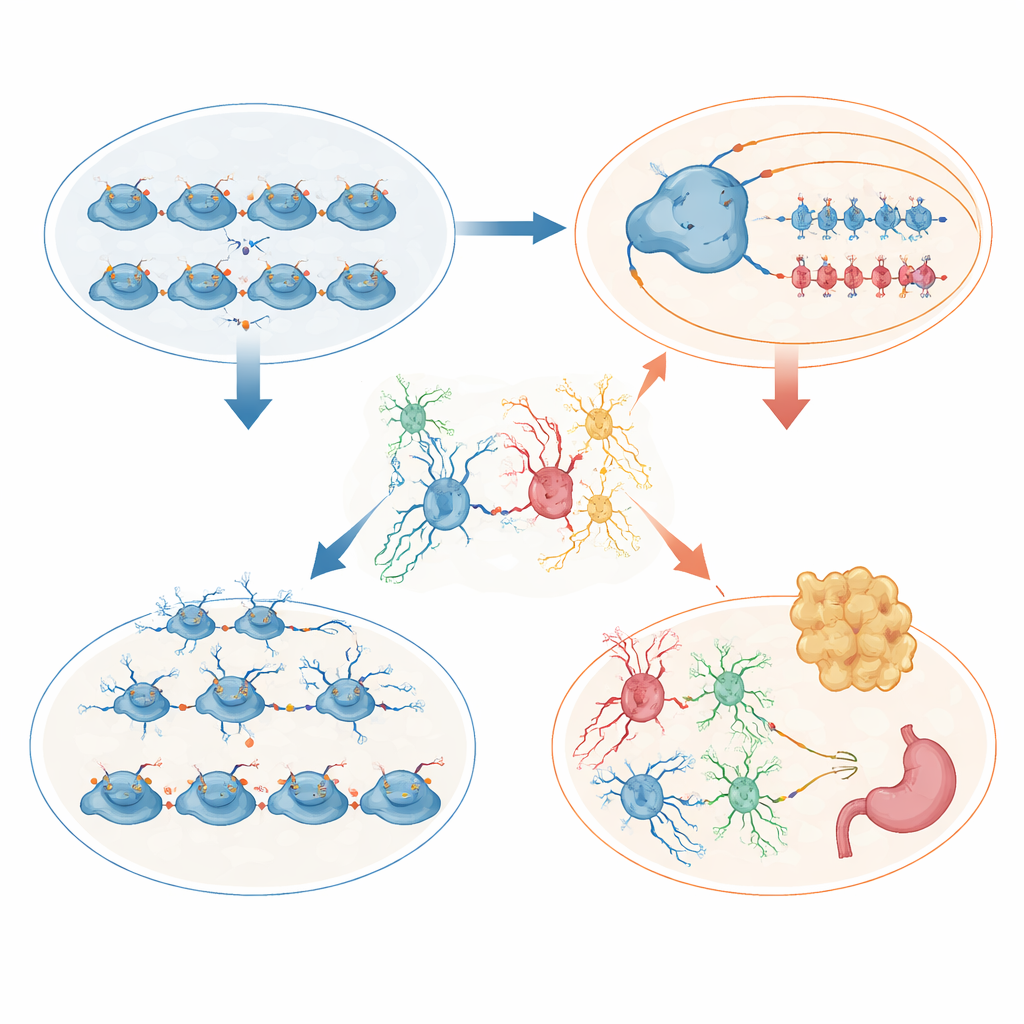
För att koppla dessa fysiska förändringar till genreglering använde teamet single-nucleus-sekvensering som läser både genaktivitet och DNA-tillgänglighet från enskilda celler. I embryonal mediala ganglionära eminensen var de flesta gener som förändrades i mutanter nedreglerade, inklusive viktiga regulatorer som styr celler mot specifika inhibitoriska öden. I adulta interneuroner skiftade balansen mellan undertyper, och grupper av gener involverade i att bilda synaptiska förbindelser och kontrollera kaliumströmmar — flöden som hjälper till att bestämma fyrningshastighet — var felreglerade. Nätverksanalys belyste koordinerad störning av kaliumkanalgener som redan är kända för att påverka epilepsi och hjärnrytmer, vilket ger en direkt molekylär koppling mellan förlusten av en histonmarkör, förändrad interneuronidentitet och anfallsbenägenhet.
Hypotalamisk obalans och en tvåfasig tillväxtkurva
Hypotalamus berättade en kompletterande historia centrerad på kroppstillväxt. Som ungar var mutantmössen mindre och en betydande andel dog tidigt. De som överlevde åt däremot senare mer, lade på sig fett och utvecklade höga nivåer av hormonet leptin, vilket signalerar fetma och sannolik leptinresistens. Single-cell-analys av embryonal hypotalamus avslöjade fler delande progenitorceller men färre celler som var avsedda för viktiga matrelaterade kärnor, särskilt regioner som normalt känner av näringstillstånd och reglerar tillväxthormon. I vuxen hypotalamus omformades den cellulära mixen: astrocyter ökade kraftigt, oligodendrocyter minskade, och specialiserade barriärceller kallade tanycyter och närliggande gliaceller förlorade sin ordnade struktur vid hjärnans gränsyta mot cirkulerande hormoner och näringsämnen. Dessa strukturella och genuttrycksändringar förvränger sannolikt hur hjärnan känner av energiförråd och kontrollerar aptit.
Beteendemässiga ekon av mänskliga neurodevelopmentella störningar
Mössens beteende speglade symtom som ses i många neurodevelopmentella tillstånd. De visade starkare ångestliknande beteenden, förändrad gångstil, minskad spontan rörelse hemma och dåliga prestationer i uppgifter som testar minne, objektrekognition och filtrering av överraskande ljud. Vissa tester visade också ökad impulsivitet. I flera mätningar tenderade honor att vara mer drabbade än hanar, vilket antyder att könsspecifika hormonsystem och genreglering kan interagera med histonmärken för att forma sårbarhet.
Vad detta betyder för människors hälsa
Tillsammans visar resultaten att försvagning av en uppsättning histonmarkörer i bara två embryonala hjärnhubbar är tillräckligt för att reproducera en bred konstellation av problem: färre inhibitoriska ”bromsar”, instabila hjärnkretsar, anfall, störda matningskretsar och onormal kroppstillväxt. För icke-specialister är huvudbudskapet att epigenetiska märken som H3K4-metylering inte är vaga tillägg utan precisa kontrollrattar som hjälper utvecklande hjärnceller att bli rätt typ, på rätt plats, vid rätt tidpunkt. När de rattarna står fel, som i många sällsynta genetiska syndrom, kan resultatet bli en tätt sammanlänkad kombination av kognitiva, beteendemässiga och metabola symtom. Att förstå dessa gemensamma rötter kan i förlängningen vägleda terapier som korrigerar inte bara ett symtom, som anfall eller fetma, utan det sammankopplade system som ger upphov till dem.
Citering: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Nyckelord: epigenetik, interneuroner, hypotalamus, anfall, fetma