Clear Sky Science · sv
Att skilja fasavgränsning från fibrillisering bevarar aktiviteten hos biomolekylära kondensat
Varför detta är viktigt för hjärnhälsan
Många hjärnsjukdomar, inklusive Alzheimers, involverar proteiner som med tiden klumpar ihop sig till hårda, fibrösa trassel. Samma proteiner kan också bilda mjukare, droppliknande strukturer i cellerna som hjälper till att organisera kemin, ungefär som små, flytande arbetsstationer. Denna studie ställer en avgörande fråga: kan vi stoppa den skadliga förhårdningen av dessa droppar till fibrer utan att förstöra deras nyttiga, vardagliga funktion? Författarna visar att en vanlig cellmetabolit, aminosyran L-arginin, kan göra just det för ett centralt Alzheimersrelaterat protein kallat Tau.
Från fritt flytande protein till små droppar
Inuti celler stannar vissa proteiner inte alltid jämnt uppblandade i den flytande inre miljön. Istället kan de samlas i droppar, kallade biomolekylära kondensat, som beter sig som mycket mjuka geléer eller trögflytande vätskor. Teamet fokuserade på Tau, ett protein som normalt hjälper till att bygga och stabilisera mikrotubuli—hålfilament som fungerar som vägar inne i nervceller. Tau är också beryktat för att bilda amyloida fibriller, de styva fibrerna som finns i de trassel som kännetecknar många neurodegenerativa sjukdomar. För att studera hur Tau-droppar utvecklas över tid konstruerade forskarna en variant av proteinet, döpt SynTag-Tau, som bildar aktiva kondensat som åldras till amyloida fibriller på en experimentellt lämplig tidsskala, utan hårda tillsatser.
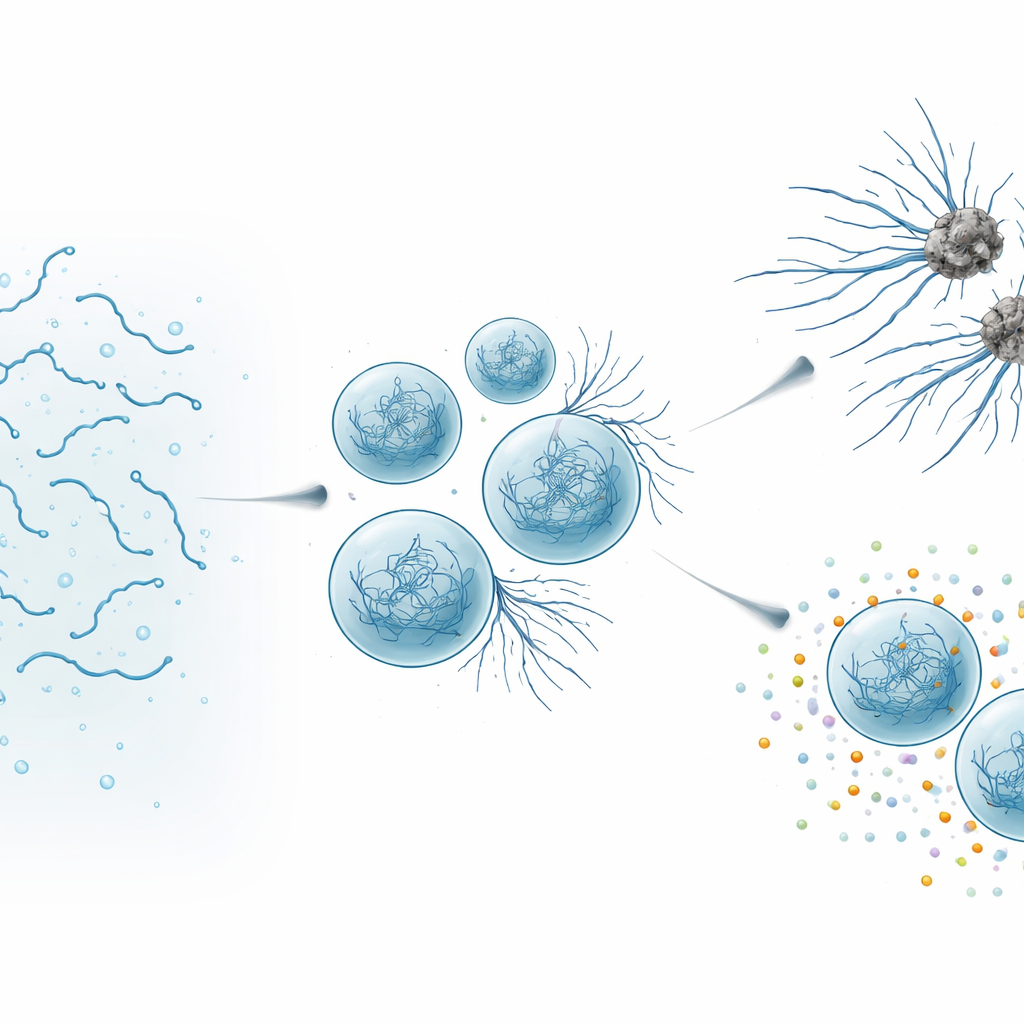
När hjälpsamma droppar blir skadliga
Med högupplöst mikroskopi och biofysiska mätningar följde författarna SynTag-Tau-dropparnas förändring över flera timmar. Färska droppar uppträdde som vätskor: de förenades lätt, deras molekyler rörde sig snabbt och det fanns inga tecken på ordnad struktur. Med tiden saktade dropparna ner och stelade till, och tunna fibrer började skjuta ut från deras ytor ut i den omgivande lösningen. Känsliga optiska metoder visade att dessa fibrer innehöll den tättpackade ”cross–beta”-arkitekturen som är typisk för amyloid. Viktigt var att gränsytan—skillet mellan det täta dropparna och den omgivande vätskan—agerade som en het fläck där fibriller först dök upp. När dropparna åldrades och fick fler utskott försämrades Taus normala funktion: kondensaten blev sämre på att dra in tubulin, byggstenen i mikrotubuli, och förlorade så småningom helt förmågan att stödja mikrotubulibyggnad.
Små molekyler som tippar balansen
Forskarna undersökte sedan om enkla metaboliska molekyler kunde bromsa eller förhindra denna övergång från vätska till fibrer samtidigt som dropparna i sig förblev intakta. Vid screening av flera naturligt förekommande småmolekyler fann de att de positivt laddade aminosyrorna L-arginin och L-lysin kraftigt försenade eller blockerade bildningen av amyloida fibriller från SynTag-Tau-droppar, men inte stängde av droppbildningen vid realistiska, låga millimolära koncentrationer. I kontrast påskyndade negativt laddade aminosyror som glutamat och aspartat fibrillbildningen, och allmänna proteinstörande kemikalier antingen misslyckades med att hjälpa eller störde dropparna själva. En fluorescerande analog till L-arginin visade att denna molekyl föredrar att sitta inne i Tau-kondensaten snarare än utanför, vilket antyder att den verkar där den behövs som mest.
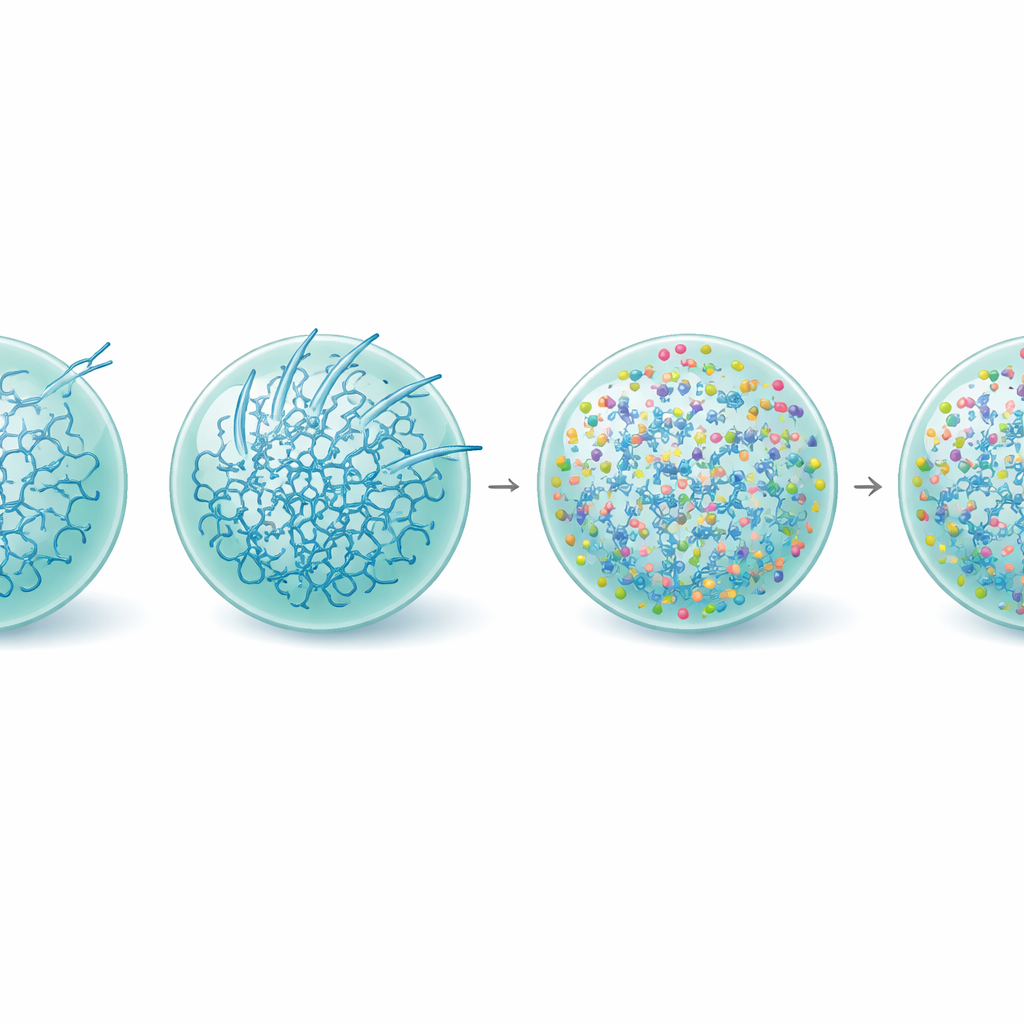
Stelare droppar, bevarad funktion
Närmare analyser visade hur L-arginin omformar det inre livet i Tau-dropparna. Mätningar av proteinstruktur visade att andelen Tau-molekyler som antar de styva beta-rika formerna kopplade till amyloid minskade när L-arginin var närvarande, även i äldre droppar. Videobaserad nanorheologi—som spårar små pärlors rörelse inne i kondensat—visade att L-arginin faktiskt gjorde Tau-dropparna mer viskoelastiska, vilket betyder att deras interna nätverk blev starkare och mer sammanlänkat samtidigt som det förblev vätskeliknande. Denna förstärkning verkar hålla systemet i ett metastabilt, funktionellt tillstånd och höjer den energibarriär som krävs för att bilda fibriller, särskilt vid droppens yta. I linje med detta fortsatte L-argininbehandlade kondensat att rekrytera tubulin jämnt och stödde mikrotubuliväxt långt efter att obehandlade droppar hade blivit inaktiva.
Vad detta betyder för framtida terapier
Arbetet visar att krafterna som driver proteiners droppbildning och de som driver skadlig fibrilbildning är besläktade men separerbara. Genom att justera kemin inne i kondensat med en metabolit som L-arginin är det möjligt att bevara det fördelaktiga, vätskebaserade tillståndet samtidigt som övergången till sjukdomsrelaterade amyloida fibrer fördröjs eller förhindras. Även om denna studie använder ett särskilt konstruerat Tau-system in vitro erbjuder den ett principbevis: små molekyler som selektivt stärker kondensatens stabilitet kan en dag hjälpa till att skydda celler från den gradvisa uppbyggnaden av giftiga proteinaggregat utan att blockera biomolekylära kondensats normala, organiserande roller.
Citering: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Nyckelord: Tau-protein, biomolekylära kondensat, amyloida fibriller, L-arginin, neurodegeneration