Clear Sky Science · sv
Epilepsiassocierade varianter i FOXJ3 kopplar ett transkriptionsprogram för PTEN–mTOR-vägen till neuronbestämning och kortikal lamination
När hjärnans ledningar går lite fel
Epilepsi börjar ofta i barndomen, men hos många unga patienter ser läkarna inget uppenbart fel på hjärnavbildningar. Denna studie tar itu med en dold orsak: små förändringar i en gen som heter FOXJ3 som tyst omformar hur hjärnans yttre skikt, cortex, byggs upp. Genom att följa genens verkan i familjer med fokal epilepsi och i utvecklande mushjärnor visar forskarna hur tidiga misstag i cellbildning, förflyttning och lagring så småningom kan ge upphov till anfall.
En subtil missbildning bakom svårbehandlade anfall
Många barn med läkemedelsresistent fokal epilepsi har en tillstånd som kallas fokal kortikal dysplasi (FCD), där partier av cortex är felaktigt formade. Dessa områden innehåller felplacerade och onormalt stora nervceller och är en vanlig anledning till att mediciner inte kontrollerar anfallen. Trots det är den molekylära orsaken till FCD ofta okänd, och standard-MRI kan missa små eller ytliga defekter. Författarna började med en familj där flera medlemmar hade fokal epilepsi och tecken på FCD. Noggrann genomanalys pekade på sällsynta förändringar i FOXJ3, en gen som tidigare inte kopplats till epilepsi. Ytterligare fall i stora genetiska databaser visade fler individer med ovanliga FOXJ3-varianter och fokala anfall, vilket tyder på att denna gen kan vara en återkommande aktör i sådana störningar.
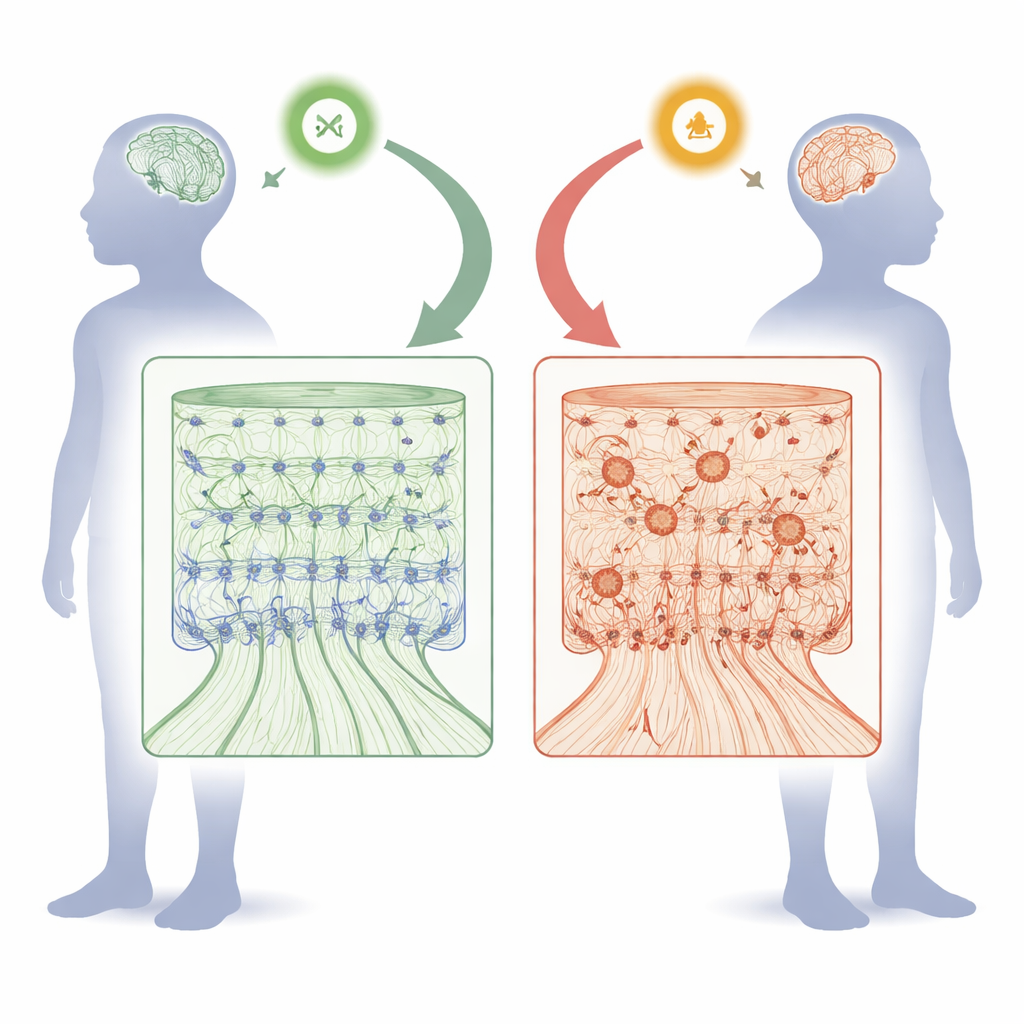
Hur FOXJ3 hjälper till att forma hjärnans tänkande yta
Under fostrets utveckling byggs cortex upp som en flerplansbyggnad. Stamliknande celler som linjerar hjärnans inre yta delar sig och skickar sedan nyfödda neuroner utåt längs radiala ”stommar” för att bilda sex ordnade lager. Teamet fann att FOXJ3 är aktiv både i dessa stamliknande progenitorer och i unga neuroner, men dess aktivitet i progenitorerna sjunker naturligt efter en viss tidpunkt i mitten av dräktigheten. Genom att använda gendämpande verktyg i musembryon minskade forskarna Foxj3-nivåerna vid olika stadier och observerade vad som hände. Tidig förlust av Foxj3 gjorde att nyfödda neuroner migrerade långsammare och hamnade i fel lager. Celler som skulle blivit djupa-lager-neuroner antog i stället identiteter typiska för övre lager, och callosala projektionneuroner, som förbinder hjärnhalvorna, bildades i överskott. Senare i utvecklingen hade däremot minskad Foxj3 långt mildare effekter, vilket visar att dess roll är mycket tidskänslig.
Att hålla celldelning och tillväxt i balans
För att förstå varför FOXJ3 har sådan påverkan kombinerade forskarna flera storskaliga angreppssätt. De kartlade var FOXJ3 binder på DNA och vilka gener som är aktiva i tusentals enskilda kortikala celler. Detta pekade starkt mot gener som styr cellcykeln och hjärntillväxt, särskilt PTEN, en viktig broms på en tillväxtväg känd som mTOR. I progenitorceller gynnade FOXJ3-bindning PTEN-aktivitet, vilket i sin tur hjälpte cellerna att lämna delningscykeln, omvandlas till neuroner och migrera utåt på ett ordnat sätt. När Foxj3 slogs ned stannade fler progenitorer kvar i delande tillstånd, färre lämnade cykeln i tid, och migrationen stannade i mellanzoner. Avgörande nog återställde återinförande av PTEN-nivåer i Foxj3-defekta hjärnor i stor utsträckning migrationen, lagrings- och cellödesproblemen, medan ett uppsving av en annan tillväxtregulator, TSC1, inte gjorde det. Detta placerar PTEN i centrum för FOXJ3:s kontroll över kortikal konstruktion.
Från felreglerade vägar till förstorade neuroner
Teamet undersökte därefter hur patientlika FOXJ3-varianter beter sig. En sjukdomsassocierad version av FOXJ3 misslyckades med att höja PTEN-nivåerna och tillät mTOR-vägen att bli överaktiv, vilket syntes genom ökad fosforylering av ett nyckelprotein kopplat till tillväxt. Hos tonårsmöss som genmodifierats för att uttrycka denna mutanta form i utvecklande cortex framträdde senare neuroner tydligt svullna, med större cellkroppar och omkrets, vilket efterliknar de dysmorfiska celler som ses vid mänsklig FCD. Den mutanta proteinet nådde trots allt fortfarande kärnan korrekt, vilket indikerar att problemet ligger i felaktig genreglering, inte i felaktig lokalisation. Tillsammans knyter dessa fynd FOXJ3-mutationer till en kaskad av händelser — mindre PTEN, mer mTOR-signalering, försenat utträde ur cellcykeln, störd migration och hypertrofiska neuroner — som kan lägga grunden för epileptiska nätverk.
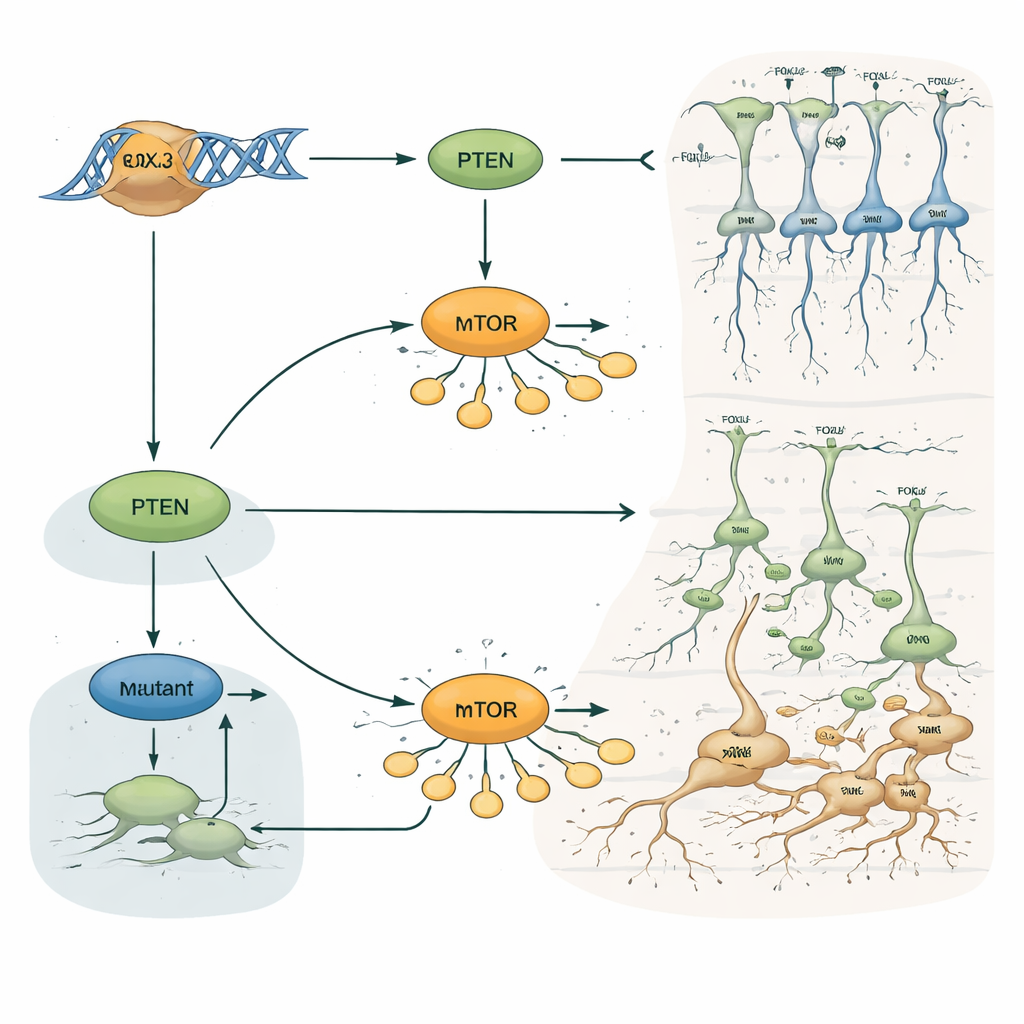
Varför detta är viktigt för epilepsi och dolda hjärnskador
För en icke-specialist är huvudbudskapet att en enda transkriptionsfaktor, FOXJ3, hjälper bestämma när och var kortikala neuroner föds, hur de rör sig och vilket lager de slutligen hamnar i. Genom att verka via PTEN–mTOR-tillväxtvägen håller FOXJ3 hjärnbygget i tidsschema. Sällsynta förändringar i denna gen kan rubba den balansen och orsaka små områden av cortex att kopplas och läggas fel, även när MR-bilder ser normala ut. Detta arbete föreslår inte bara FOXJ3 som en ny genetisk orsak till fokal kortikal dysplasi och epilepsi, utan visar också hur subtila förskjutningar i tidig hjärnutveckling kan eka årtionden senare som svårbehandlade anfall.
Citering: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Nyckelord: fokal kortikal dysplasi, FOHJ3-genen, PTEN mTOR-vägen, kortikal utveckling, fokal epilepsi