Clear Sky Science · sv
Molekylär grund för kollagen‑galaktosylering av GLT25D1
Hur små sockermärken hjälper till att bygga starka vävnader
Kollagen är kroppens vanligaste protein och utgör stomme för hud, ben, blodkärl och många andra vävnader. Men kollagen fungerar inte ensam: det måste dekoreras med små sockermolekyler på precisa platser för att få rätt styrka och flexibilitet. Denna studie avslöjar, på atomär nivå, hur ett nyckelenzym, GLT25D1, fäster ett särskilt socker på kollagen och hur fel i denna process kan leda till sköra kärl, muskelproblem och kanske till och med cancer.
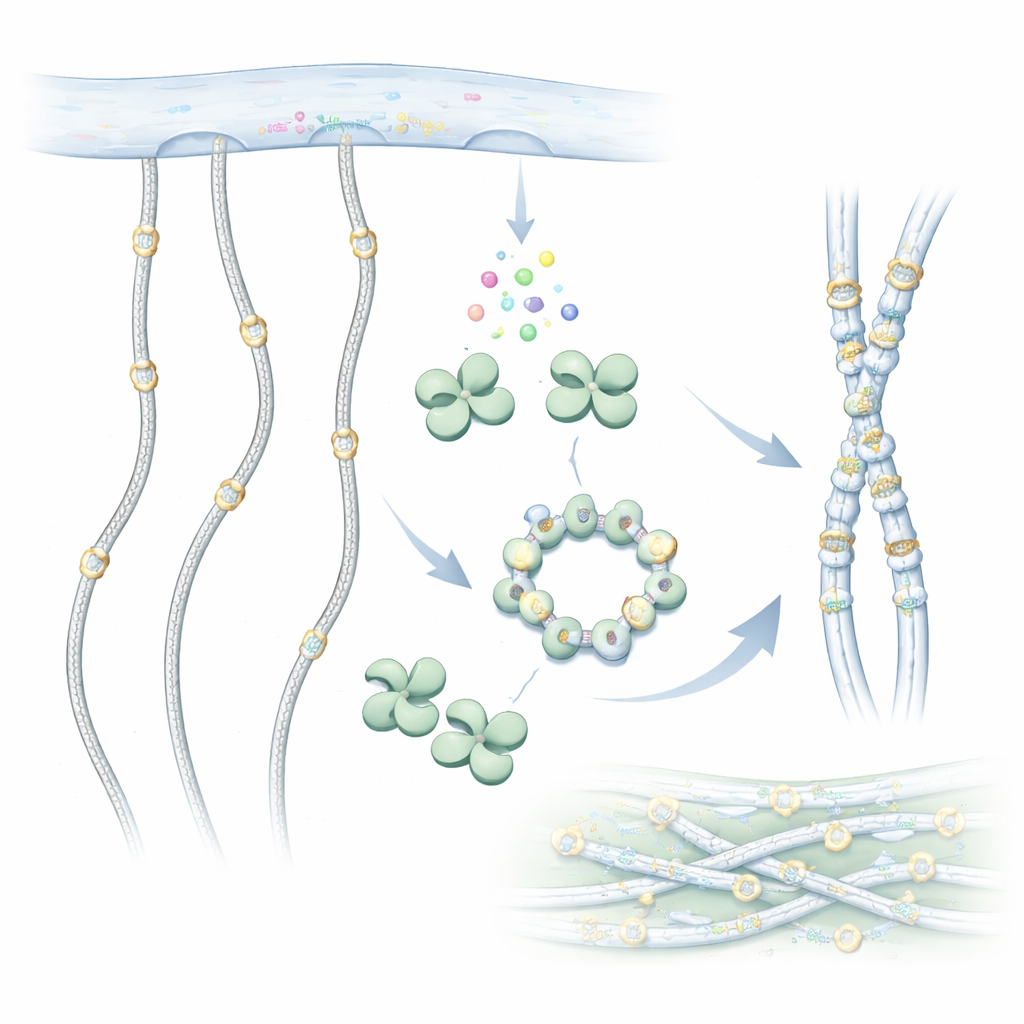
Närmare koll på kollagens dolda förändring
Kollagenmolekyler är långa, rep‑lika kedjor som bygger upp robusta fibrer utanför cellerna. Innan de lämnar cellen redigeras de kemiskt. En viktig redigering är tillägg av sockergrupper på speciella byggstenar kallade hydroxylysiner längs kollagenkedjan. GLT25D1 utför det första steget i denna sockermärkning genom att överföra en galaktos från en donormolekyl till hydroxylysinen. Denna sockerdekoration är bevarad från enkla djur till människan och hjälper kollagen att fälla korrekt, interagera med celler och motstå slitage.
Avslöjar formen hos en kollagendekoratör
För att förstå hur GLT25D1 fungerar använde forskarna kryo‑elektronmikroskopi för att avbilda det humana enzymet i nästan atomär upplösning. De upptäckte att varje GLT25D1‑molekyl har två liknande lober, båda relaterade till en vanlig enzymveckning som ses i sockeröverförande proteiner. Dessa lobar parar ihop sig till förlängda dimerer, och tre dimerer kan ytterligare montera sig till en hexamer formad som en ring. I dessa sammankopplingar sitter de verkliga arbetshästarna — katalytiska center — långt ifrån varandra, en utformning som kan tillåta flera sockertilläggsplatser att verka längs en utsträckt kollagenkedja samtidigt.
De verksamma delarna: där sockeroverföring verkligen händer
Teamet löste strukturer av GLT25D1 bundet både till dess sockerdonator och en kort kollagenlik peptid som innehåller hydroxylysine. Detta ternära komplex visade att endast den andra loben, kallad C‑terminala domänen, faktiskt utför kemin. Där vilar donormolekylen i en ficka stabiliserad av en metalljon, medan peptiden ligger i en smal fåra som tvingar fram ett specifikt lokalt mönster: en hydroxylysine följd omedelbart av en liten glycin. En enda asparaginsyrarest agerar som en kemisk bas och aktiverar hydroxylysins hydroxylgrupp så att den kan attackera sockret och slutföra överföringen. Förändringar i någon av dessa nyckelaminosyror minskar eller eliminerar aktiviteten drastiskt, vilket bekräftar deras avgörande roller.
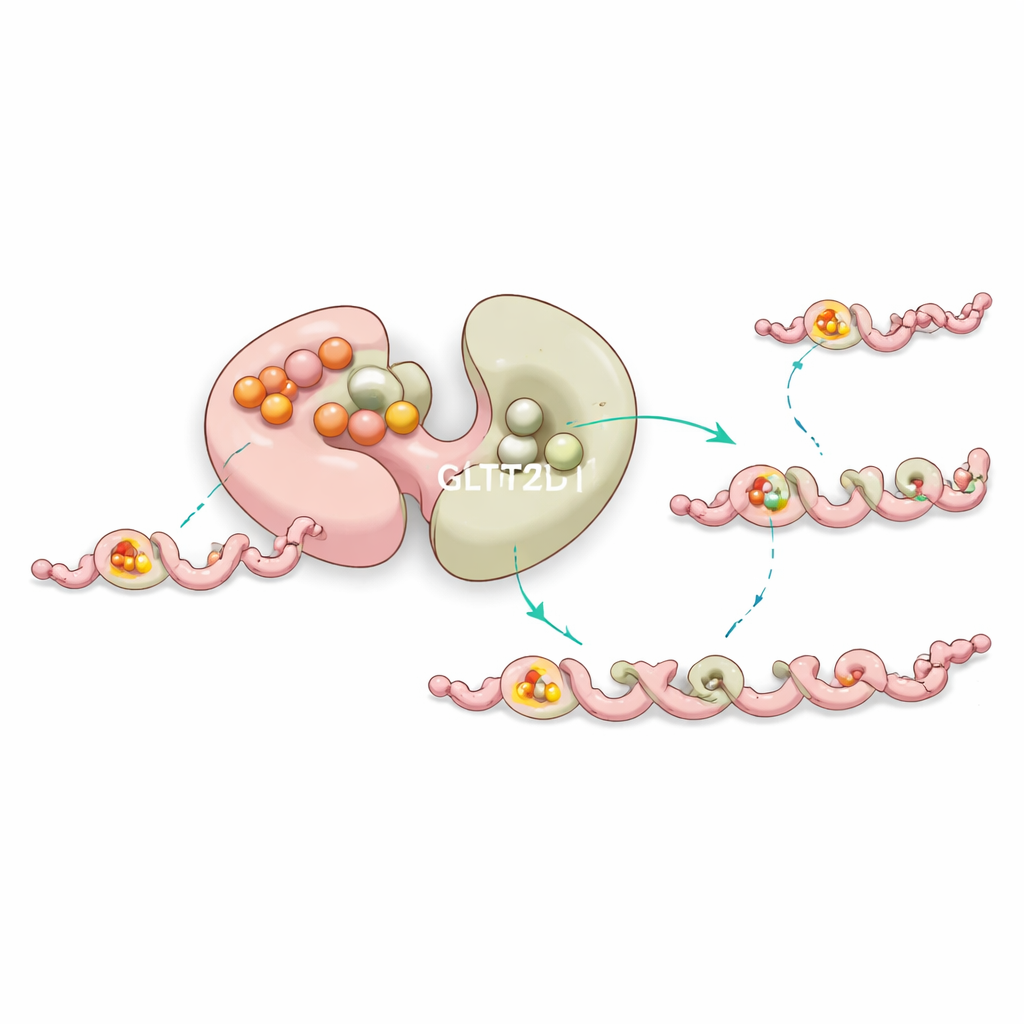
En inbyggd stabilisator och fjärrstyrning
Förvånande nog binder den första loben av GLT25D1 en sockerdonator mycket hårt men utför inte överföringen. Istället antyder experiment och datorsimuleringar att denna ”tysta” site hjälper till att stabilisera enzymet och subtilt finjusterar beteendet hos den aktiva loben genom långdistanskommunikation inom proteinet. Mutationer nära denna icke‑katalytiska ficka destabiliserar ofta enzymet eller ändrar dess effektivitet, vilket tyder på att naturen använder denna extra bindningsplats som en form av intern kvalitetskontroll för att hålla kollagenmodifieringen stabil.
När dekoratören fallerar: kopplingar till sjukdom
Genom att kartlägga patienthärledda mutationer på sin strukturella modell kunde författarna förklara hur fel i GLT25D1 leder till mänsklig sjukdom. Vissa mutationer avkapar den katalytiska loben helt, andra destabiliserar proteinkärnan, och ytterligare några slår rakt mot sockar‑ eller kollagenbindande ytor. Dessa fel minskar eller eliminerar sockertillägg till kollagen och har kopplats till småkärlssjukdom i hjärnan, kognitiva problem samt muskel‑ och skelettdefekter. Cancerassocierade mutationer klustrar sig också i avgörande regioner, vilket antyder att ändrad kollagendekoration kan påverka tumörtillväxt och spridning.
Varför detta spelar roll för hälsa och framtida behandlingar
Genom att lägga fram en detaljerad tredimensionell blåkopi av GLT25D1 i funktion förklarar detta arbete hur precisa sockermärken adderas till kollagen och varför detta steg är så viktigt för vävnadsintegritet. För icke‑specialister är huvudbudskapet att små kemiska förändringar på kollagen kan få oproportionerligt stora effekter på blodkärl, ben och möjligen cancerrisk. Den strukturella kartan över GLT25D1 erbjuder nu en vägledning för att diagnostisera skadliga varianter och för att utforma terapier — vare sig småmolekyler som stabiliserar felaktiga enzymer eller genbaserade strategier — som en dag skulle kunna korrigera defekter i kollagens sockermärkning vid källan.
Citering: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Nyckelord: kollagen‑glykosylering, GLT25D1, extracellulär matrix, kärlsjukdom, cryo‑EM‑struktur