Clear Sky Science · sv
Sclerostinbrist gör vita adipocyter känsligare för termogena signaler som inducerar beigeing hos möss
Varför uppvärmning av fett kan dämpa sjukdom
De flesta av oss ser ben och kroppsfett som skilda världar: det ena ger struktur, det andra lagrar energi. Denna studie i möss visar att ben och fett ständigt för en kemisk dialog, och att ett protein som produceras av benceller kan avgöra om vårt "vita" fett bara lagrar kalorier eller förvandlas till mer aktivt, kalori-brännande "beige" fett. Att förstå denna dolda kommunikation kan öppna nya vägar för att samtidigt angripa fetma, diabetes och benförlust.
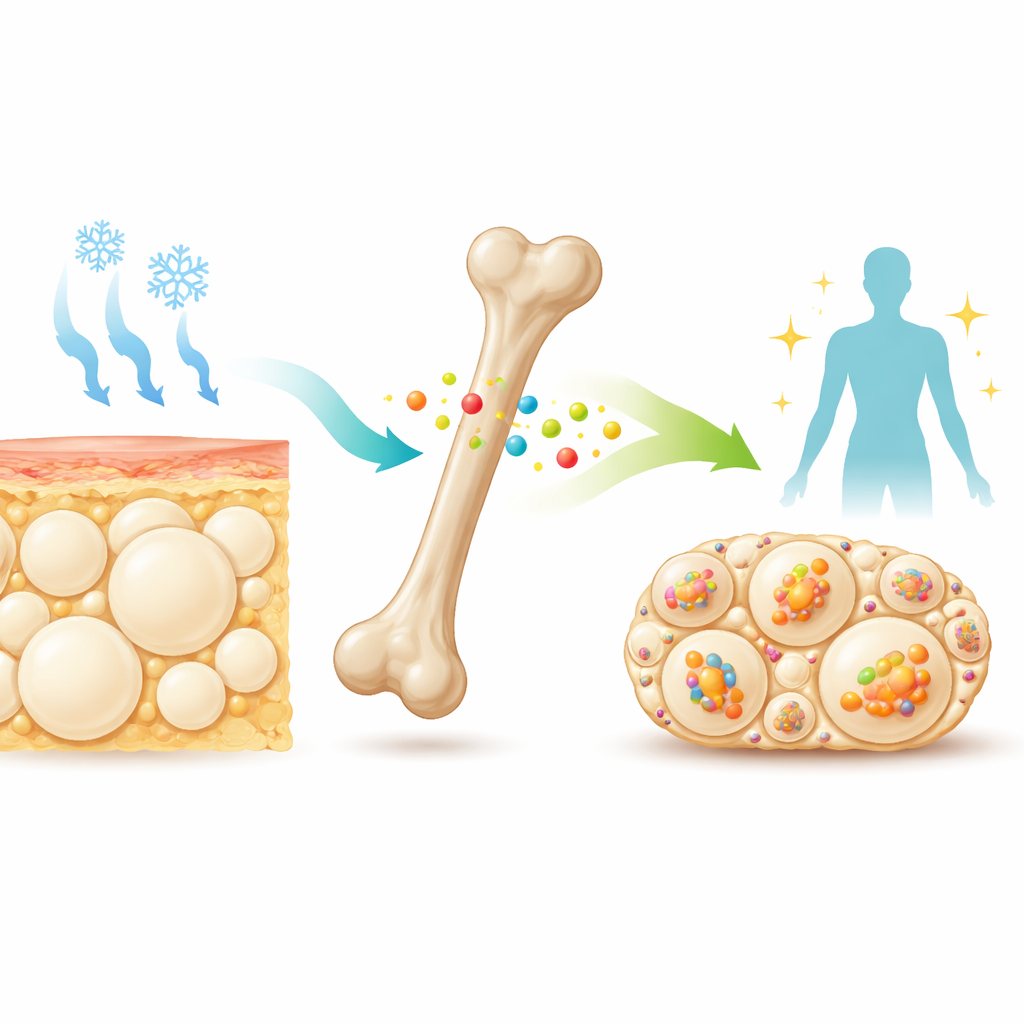
En tyst budbärare från benet
Djupt inne i benen frisätter specialiserade celler ett litet protein kallat sclerostin till blodomloppet. Läkare riktar redan läkemedel mot sclerostin för att stärka ben hos patienter med frakturrisk. Tidigare arbete visade att möss som saknar sclerostin inte bara har mycket starka ben, utan också är magrare och mer insulinkänsliga. Deras subkutana fett, särskilt runt höfterna (inguinalt vitt fett), innehåller små, multikompartmentsfettrum som liknar "beige" fett, vilket kan bränna bränsle för att skapa värme. Dessa ledtrådar fick forskarna att fråga om sclerostin normalt fungerar som en broms för kroppens förmåga att omvandla vitt fett till beige fett när det utsätts för kyla eller för läkemedel som efterliknar nervsignaler till fett.
Kylsignaler, bensignaler och fettantändning
Teamet exponerade normala möss och möss utan sclerostin-genen (Sost-/-) för ett läkemedel som aktiverar en specifik fettcellsreceptor (β3-adrenerg receptor), eller för mild kyla. Hos normala djur ökade dessa termogena signaler produktionen av sclerostin i ben och höjde dess nivå i blodet. Denna ökning kopplades till förlust av spongiöst ben men endast måttliga förändringar i subkutant fett. I kontrast visade sclerostin-deficienta möss en mycket starkare respons: deras inguinalfett tog upp mer glukos, släppte ut fler fettsyror, krympte i storlek och fylldes med beige-liknande celler packade med mitokondrier, cellernas kraftverk. Viktiga termogena gener slog på starkare i dessa möss, särskilt i subkutant fett, medan klassiskt brunt fett i stort var oförändrat.
Finjustering av fettförbränning genom en gemensam brytare
För att förstå hur sclerostin utövar denna kontroll fokuserade forskarna på β-katenin, ett protein som ingår i Wnt-signalvägen som sclerostin normalt undertrycker i ben. I fett drev aktivering av β-katenin efter födseln vita celler mot ett beige-liknande tillstånd och ökade deras respons på β3-adrenerga signaler, men denna effekt försvann när mössen hölls vid en varm, termoneutral temperatur där kroppen inte längre behöver extra värme. Omvänt raderade deletion av β-katenin specifikt i fettceller hos sclerostin-deficienta möss deras beige fett, återställde större vita fettceller och reverserade förbättringar i insulin- och fettsyranivåer. Dessa experiment tyder på att när sclerostin är låg blir β-katenin i fettceller en viktig intern spak som gör vitt fett mer mottagligt för termogena signaler.
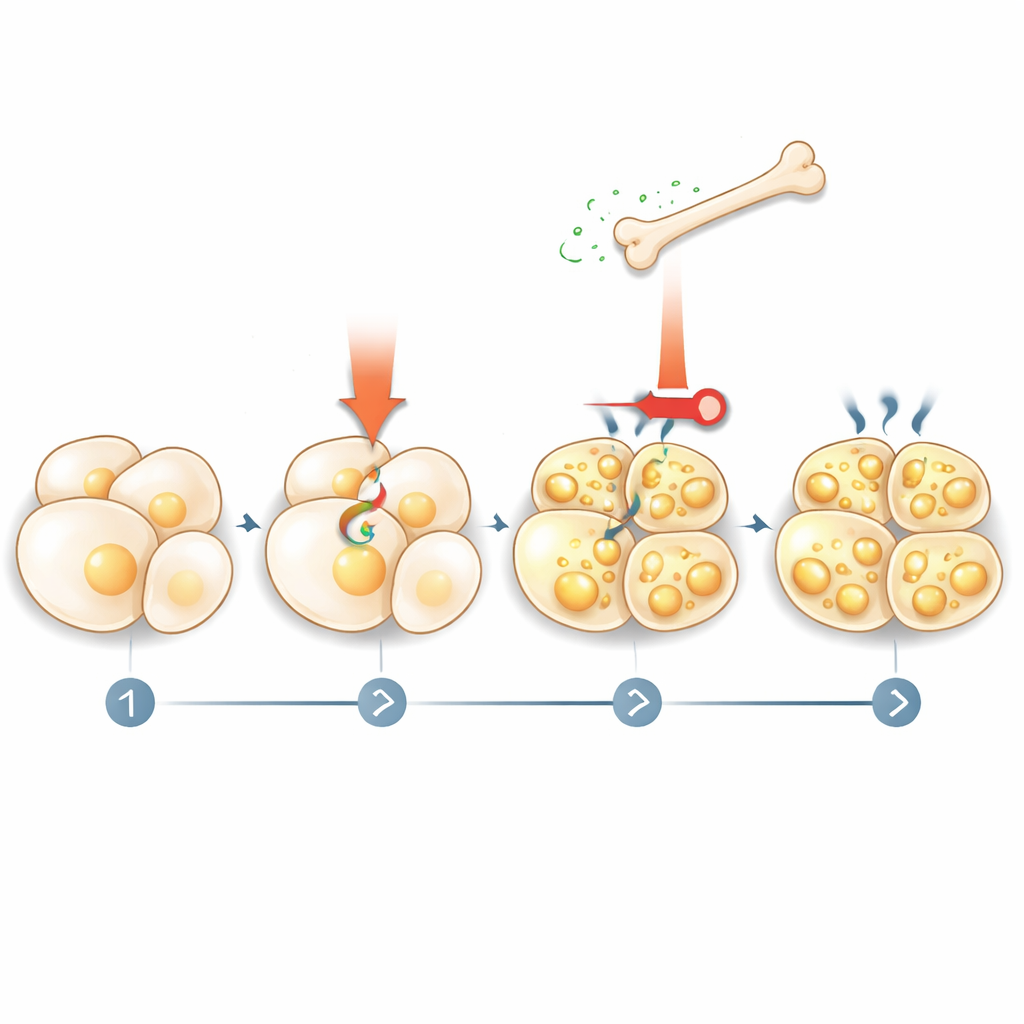
Hur fett svarar tillbaka på benet
Berättelsen slutade inte med att benet talade om för fettet vad det skulle göra. Teamet fann att termogen stimulering aktiverar fettupplösning (lipolys), vilket frigör fettsyror i blodet. Dessa fettsyror verkar i sin tur på benceller via en nukleär receptor kallad PPARγ och ökar sclerostinproduktionen. När forskarna blockerade lipolys i fettceller eller tog bort PPARγ från benceller kunde kylafterliknande läkemedel inte längre höja sclerostinnivåerna. Detta avslöjar en återkopplingsslinga: termogena signaler får fett att frigöra bränsle, detta bränsle instruerar ben att utsöndra mer sclerostin, och sclerostin bromsar sedan vidare fettaktivering och beigeing.
Att kombinera ben- och fettläkemedel för metabol hälsa
Slutligen testade forskarna om avbrott i denna slinga kunde vara fördelaktigt i ett sjukdomsliknande sammanhang. Feta möss på högfettskost fick en låg dos mirabegron (ett β3-adrenerg läkemedel som redan används vid blåssjukdom), en antikropp som neutraliserar sclerostin (romosozumab, godkänt för osteoporos), eller båda. Medan endera behandlingen ensam hade måttliga effekter, minskade kombinationen fettmassan i nyckeldepåer, försköt fett mot mindre, mer aktiva celler, sänkte insulin, triglycerider och kolesterol, och bevarade benstyrkan. Varmt boende, vilket minskar kroppens behov av värme, utplånade till stor del de metaboliska fördelarna av sclerostinbrist, vilket understryker att denna väg är viktigast när termogena signaler är närvarande.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt visar detta arbete att ben inte bara är ett passivt skelett utan en aktiv regulator av hur mycket energi fettceller förbränner. Sclerostin fungerar som en volymvred som håller termogen aktivitet i fett, och därmed bränsleanvändning, i schack. Att vrida ner det vredet—genetiskt eller med läkemedel—gör att vissa vita fettdepåer blir mer benägna att växla till ett värmeproducerande läge när kroppen påverkas av kyla eller specifika läkemedel. Eftersom samma intervention kan stärka ben och förbättra metabol hälsa hos möss, kan noggrant utformade kombinationer av ben- och fettinriktade terapier en dag hjälpa till att behandla fetma, diabetes och osteoporos tillsammans, snarare än en sjukdom i taget.
Citering: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
Nyckelord: sclerostin, beige fett, ben–fett kommunikation, termogenes, metabolisk sjukdom