Clear Sky Science · sv
Lokal syntes av PI(4,5)P2 av septin-associerade PIPKIγ-isoformer styr centralspindlin-associationen med midkroppen under cytokines
Hur celler fullbordar delningen
Cytokines – den slutliga ihopknytningen som delar en cell i två – är lätt att ta för given, men när den går fel kan det främja cancer och andra sjukdomar. Denna studie avslöjar hur en specifik uppsättning molekyler fungerar som byggarbetsplatsens förmän vid den smala bron som förbinder två nyfödda celler, och säkerställer att delningen slutförs rent istället för att gå tillbaka eller stanna upp.
Den sista bron mellan dottercellerna
Efter att en cell kopierat sitt genetiska material och separerat kromosomerna måste den dela sig fysiskt. En kontraktil ring av proteinfilament drar ihop cellens mitt, vilket skapar en djup fåra kallad klyvningsfåran. När denna fåra dras in förblir de två dottercellerna förbundna av en tunn intercellulär bro som innehåller en kompakt kärna, midkroppen. Midkroppen är en liten men komplex struktur bestående av buntade mikrotubuli, stomproteiner och signaleringslipider, och fungerar både som förankring och som ett kontrollcentrum som samordnar de sista stegen i delningen och det slutgiltiga snittet mellan cellerna. 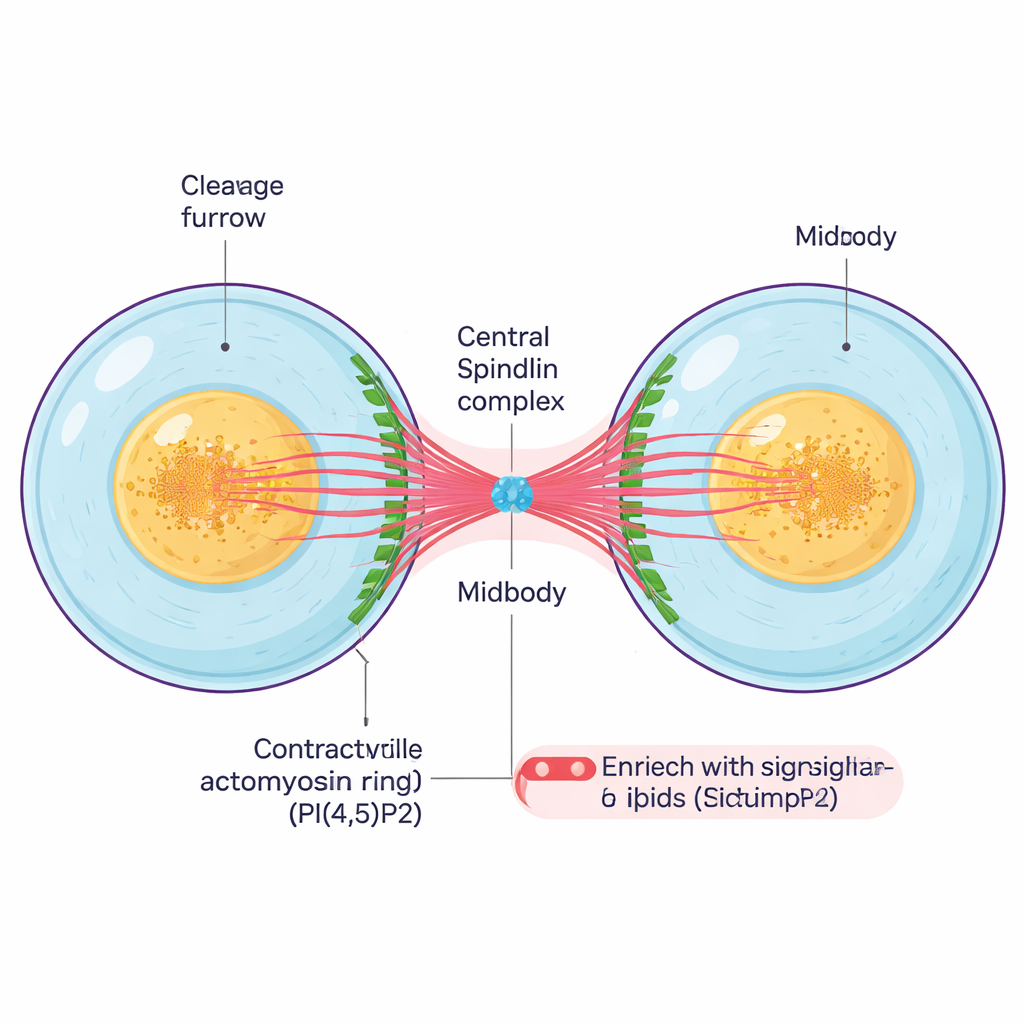
En lipidsignal som måste vara på rätt plats
En nyckelspelare i denna process är ett signalerande fettmolekyl i cellmembranet kallad PI(4,5)P2. Denna lipid hjälper till att förankra många proteiner som bygger och drar ihop den kontraktila ringen samt stabiliserar bron. Gåtan har varit hur celler styr var och när PI(4,5)P2 uppträder, med tanke på att den kan diffundera i membranet. Författarna fokuserade på enzymer kallade typ I PIP-kinaser, som skapar PI(4,5)P2, och särskilt på en gen, PIPKIγ, som finns i flera subtilt olika spliceformer. Genom att selektivt minska varje kinas i humana celler och observera effekterna med avancerad mikroskopi fann de att PIPKIγ har en särskild roll sent i cytokines, när bron och midkroppen bildas, även om det inte kraftigt förändrar de övergripande PI(4,5)P2-nivåerna vid cellytan.
Septin-stommar rekryterar ett specialiserat enzym
Teamet upptäckte att två splicevarianter av PIPKIγ, kallade i3 och i5, fungerar som precisionsverktyg som förses till rätt plats av strukturella proteiner kända som septiner. Septiner bildar filament och ringar som hjälper till att forma bron och organisera andra komponenter. Biokemiska pull-downs och cellbilder visade att PIPKIγ-i3 och PIPKIγ-i5 fysiskt binder till septinkomplex och dekorerar septinfilament, medan andra PIPKIγ-varianter inte gör det. När forskarna muterade två specifika aminosyror i dessa spliceinsatser kunde enzymerna inte längre binda septiner. I delande celler flyttar normala PIPKIγ-i3/i5 från ett diffust membranmönster för att koncentrera sig vid klyvningsfåran och sedan markera den intercellulära bron och midkroppen i takt med septiner och ett annat stomprotein, anillin. Att ta bort endast i3- och i5-varianterna spridde anillin och septiner bort från midkroppen längs bron, och många celler misslyckades med cytokines och fick flera cellkärnor.
Lokal lipidproduktion låser fast delningsmaskineriet
För att testa om dessa effekter berodde på lokal PI(4,5)P2-produktion mätte författarna PI(4,5)P2 runt midkroppen och manipulerade enzymer som adderar eller tar bort denna lipid. Att depletera PIPKIγ-i3/i5 minskade PI(4,5)P2 vid midkroppen, medan blockering av ett PI(4,5)P2-nedbrytande enzym gav motsatt effekt. Viktigt var att återställande av en normal, septinbindande, katalytiskt aktiv PIPKIγ-spliceform räddade den korrekta klustringen av anillin och septiner vid bron, medan kinase-döda eller septinbindnings-defekta mutanter inte gjorde det. Med hjälp av liveavbildning och en expansionsmikroskopiteknik som fysiskt blåser upp provet för att avslöja fina detaljer visade teamet att utan PIPKIγ-i3/i5 flyttar septiner inte längre ut på bronens mikrotubuli, bron blir kortare och mindre buntad, och ett avgörande komplex kallat centralspindlin misslyckas med att förbli tätt associerat med midkroppen. 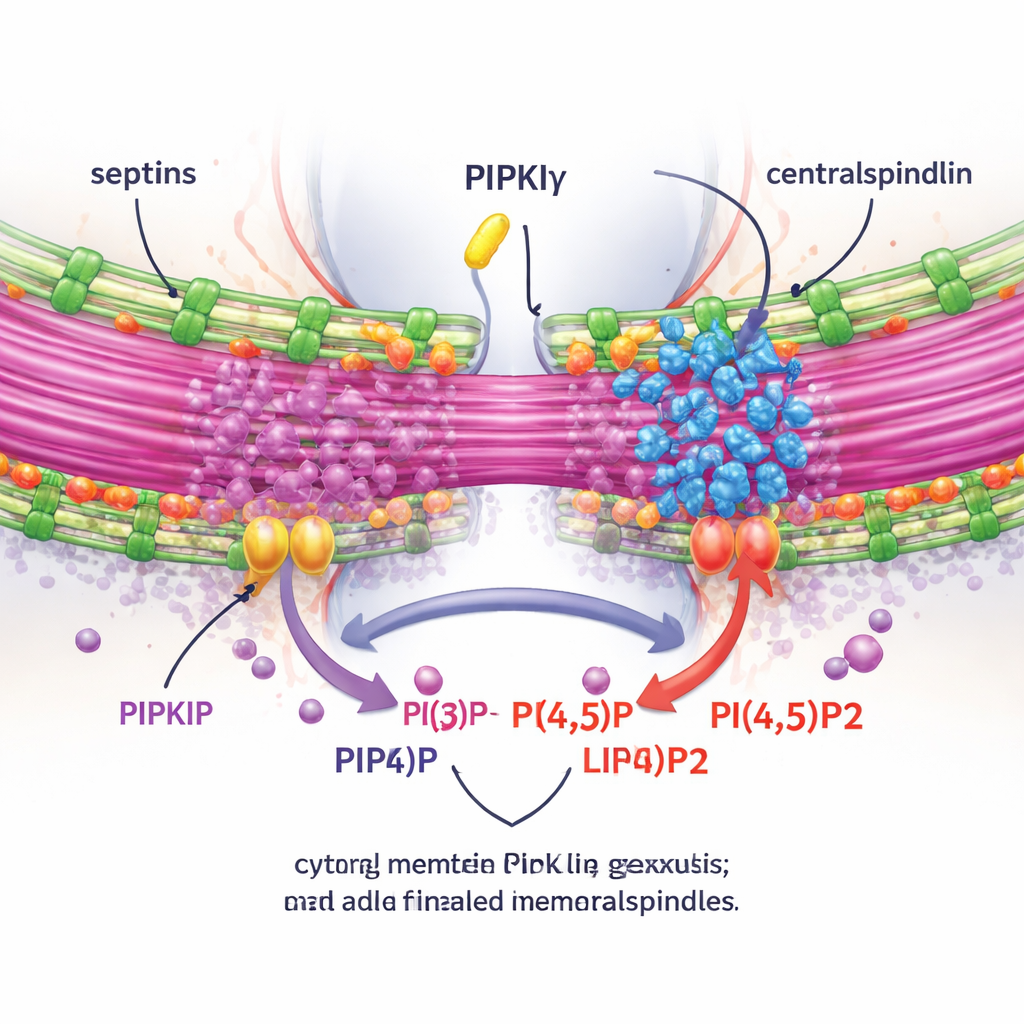
Bygger en kontrollpunkt för ett rent snitt
Centralspindlin hjälper till att länka midkroppens mikrotubuli till det omgivande membranet och reglerar små molekylära switchar som kontrollerar cellformen. Studien visar att centralspindlin associerar med både septiner och PIPKIγ, och att förlust av endera partnern liknande försvagar dess närvaro vid midkroppen. Författarna föreslår att septiner rekryterar PIPKIγ-i3/i5 till den insjunkna fåran, där dessa enzymer skapar en koncentrerad plätt av PI(4,5)P2. Denna lokala lipidpool stabiliserar i sin tur anillin, centralspindlin och septiner nära midkroppen, främjar buntning och stabilisering av bronens mikrotubuli och tillåter att den intercellulära bron mognar tills det slutliga avgränsningssnittet sker. Om detta system rubbas uppträder PI(4,5)P2 på fel platser, stomproteiner sprids, mikrotubuli blir dåligt buntade och cytokines misslyckas ofta.
Varför detta är viktigt bortom grundläggande cellbiologi
Genom att fastställa hur specifika PIPKIγ-splicevarianter och septiner samarbetar för att generera en lokal lipidsignal vid midkroppen förklarar detta arbete hur celler ger rumslig precision åt en mycket rörlig signalmolekyl. Denna precision är avgörande för en säker fullföljning av celldelningen och hjälper till att förhindra felaktig kromosomsegregering och onormala cellantal som kan gynna tumörutveckling. Samma midkroppsstrukturer påverkar också cellöde och proliferation efter delning, så att förstå hur de byggs upp öppnar nya vägar för att utforska hur fel i dessa nanoskaliga stommar kan bidra till cancer och möjligen till manipulerbarhet av stamceller.
Citering: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Nyckelord: celldelning, cytokines, signaleringlipider, septiner, cancerbiologi