Clear Sky Science · sv
Pan-RAF‑hämmaren exarafenib riktar sig mot BRAF klass II/III i NSCLC och avslöjar ARAF‑KSR1‑resistens samt kombinationsstrategier
Varför denna forskning spelar roll för lungcancerpatienter
De flesta känner till riktade cancerläkemedel som angriper specifika genetiska förändringar. Men för många patienter med lungcancer, särskilt de vars tumörer bär mindre vanliga mutationer i genen BRAF, fungerar dagens riktade läkemedel helt enkelt inte. Denna studie presenterar ett nytt experimentellt läkemedel, exarafenib, utvecklat för att slå mot ett bredare spektrum av BRAF‑drivna tumörer och visar hur cancerceller försöker undkomma det—vilket avslöjar kombinationsbehandlingar som kan hålla dessa tumörer under kontroll längre.
En dold majoritet av förbisedd mutationer
Forskarna började med en grundläggande fråga: hur vanliga är de olika typerna av BRAF‑mutationer i avancerade cancerformer, och särskilt i icke‑småcellig lungcancer (NSCLC)? Genom att använda en mycket stor databas med blodprov (liquid‑biopsy) från över 160 000 patienter analyserade de fragment av tumör‑DNA som cirkulerar i blodet. De fann att BRAF‑mutationer i lungcancer förekommer hos ungefär 4–5 % av patienterna, vilket ändå motsvarar många tusen människor globalt. Viktigt är att omkring två tredjedelar av dessa lungtumörer bar så kallade klass II‑ och klass III‑BRAF‑mutationer—typer som dagens godkända BRAF‑läkemedel inte effektivt riktar mot. Patienter med någon av dessa klasser, särskilt klass II, hade en tendens att leva kortare än de med den mer välkända klass I‑mutationen, troligen eftersom klass I‑patienter har tillgång till etablerade riktade terapier medan klass II/III‑patienter mestadels får standardkemoterapi eller immunterapi.
Ett nästa generations läkemedel som riktar sig mot hela vägen
BRAF är en del av en kedja av proteiner (MAPK‑vägen) som för tillväxtsignaler från cellens yta in till kärnan. Många befintliga BRAF‑läkemedel är konstruerade för att blockera endast en mutant form och kan till och med oavsiktligt stimulera närliggande proteiner i normala celler. Exarafenib byggdes annorlunda: det är en ”pan‑RAF”‑hämmare utformad för att stänga ner flera RAF‑familjemedlemmar (ARAF, BRAF och CRAF) i både enkla och parbildande former, samtidigt som de flesta andra cellulära enzymer skonas. I biokemiska tester över hundratals mänskliga kinaser blockerade exarafenib starkt alla tre RAF‑proteinerna men hade få off‑target‑effekter, vilket tyder på en renare säkerhetsprofil än tidigare pan‑RAF‑föreningar.
Kraftfulla effekter i modeller av svårbehandlade tumörer
Teamet testade exarafenib i en rad cellinjer och musmodeller som bär olika BRAF‑ och RAS‑mutationer, inklusive patientnära tumörer. I cellkulturer dämpade exarafenib tillväxten och slog av MAPK‑signaleringen inte bara i klassiska BRAF V600E‑celler utan också i de med klass II‑ och klass III‑mutationer och i många RAS‑mutanta celler som i dag saknar bra riktade alternativ. I möss med lungtumörer med dessa förändringar krympte eller bromsades tumörerna upp i dosberoende grad och visade tydliga samband mellan läkemedelsnivåer, hämning av vägen och tumörsvar. Tidiga kliniska uppgifter från två patienter med avancerad BRAF‑muterad lungcancer—en med en sällsynt BRAF‑fusion och en annan med en punktmutation i klass II—visade partiella responser och betydande symtomlindring, vilket stödjer relevansen av prekliniska fynd.
Hur cancern lär sig att kringgå läkemedlet
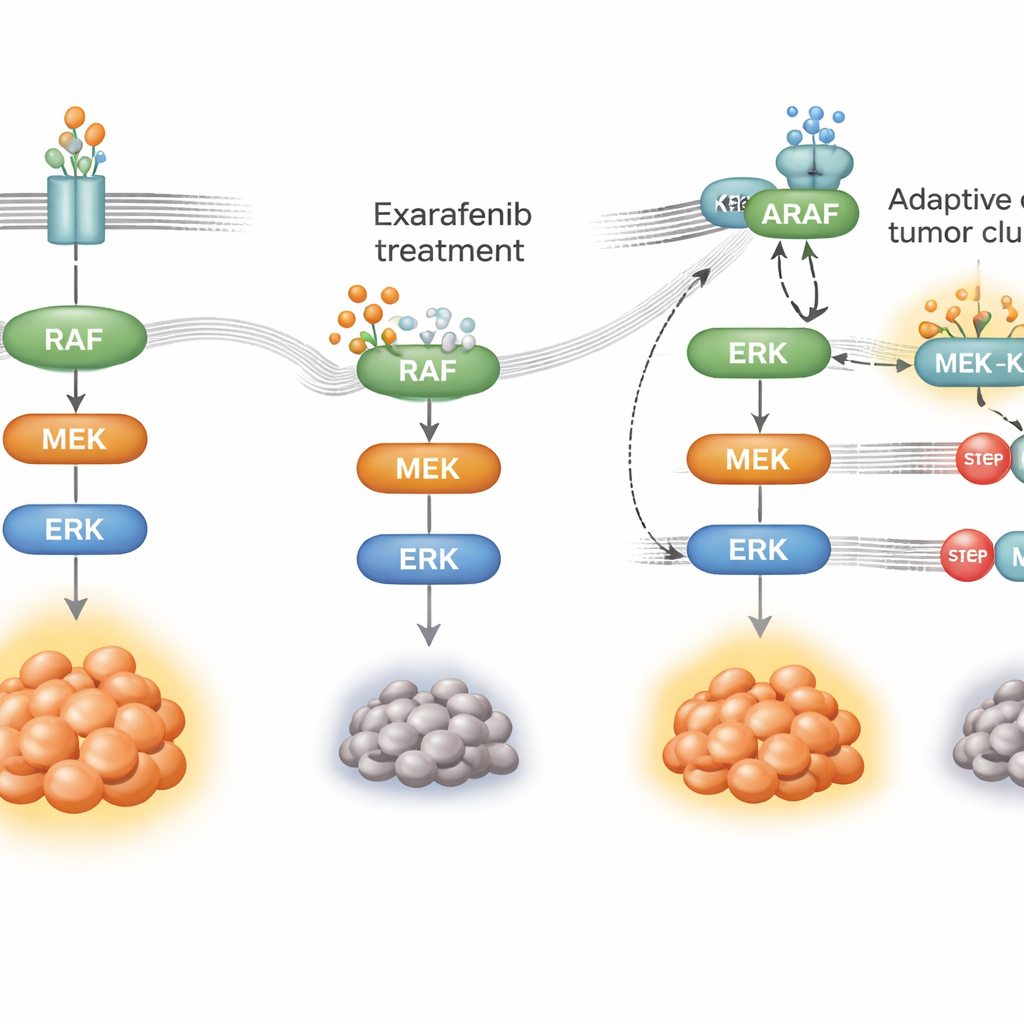
Ingen riktad terapi fungerar för alltid; cancerceller anpassar sig. För att se hur tumörer kan bli resistenta mot exarafenib exponerade forskarna BRAF‑mutanta lungcancerceller för läkemedlet under månader tills resistenta populationer uppstod. Dessa celler var fortfarande beroende av samma tillväxtväg men hade omkopplat hur de använde den. Istället för att i första hand förlita sig på mutant BRAF ökade de aktiviteten hos en uppströms strömbrytare kallad RAS och skiftade mot att använda en annan familjemedlem, ARAF, tillsammans med ett scaffold‑protein som heter KSR1. Under läkemedelspåverkan bildade ARAF och KSR1 täta komplex som hjälpte till att hålla MAPK‑kedjan igång även när exarafenib var bundet. När forskarna selektivt tystade ARAF eller KSR1, eller minskade RAS‑aktiviteten, blev de resistenta cellerna åter känsliga för exarafenib och överlevnadssignalerna kollapsade.
Kombinationsstrategier för att ligga steget före resistens
Med denna mekanistiska karta sökte teamet efter partnerläkemedel som kunde blockera vägen vid flaskhalsar som delas av både ursprungs‑ och kringgående rutter. De fann att kombinationen av exarafenib med läkemedel som hämmar MEK eller ERK—viktiga nedströmssteg i MAPK‑kedjan—gav stark synergisk effekt i många cell‑ och musmodeller, inklusive tumörer som var intrinsiskt mindre känsliga eller hade förvärvat resistens. Dessa kombinationer höll vägen stängd längre, utlöste mer celldöd och fungerade i djur ofta lika bra som eller bättre än högre doser av exarafenib ensam, utan uppenbar ökad toxicitet. Agenser som direkt riktar RAS förbättrade också exarafenibs effekter i modeller där RAS tydligt drev resistens, vilket tyder på ytterligare en kliniskt lovande taktik.
Vad detta betyder för patienter
För personer med NSCLC som bär klass II‑ eller klass III‑BRAF‑mutationer—eller komplexa BRAF‑fusioner och RAS‑sammamutationer—finns för närvarande inga godkända riktade terapier, och utfallen ligger efter de för patienter med vanligare förändringar. Denna studie ger ett starkt vetenskapligt underlag för att exarafenib kan bidra till att fylla detta gap genom att brett stänga av RAF‑driven signalering. Den förklarar också hur tumörer kan anpassa sig via en ARAF‑KSR1‑bypass och visar att man kan slå mot vägen på flera nivåer, särskilt genom att kombinera RAF‑ och MEK‑hämmare eller lägga till RAS‑hämmare, för att ge djupare och mer varaktig tumörkontroll. Tillsammans banar dessa insikter väg för kliniska prövningar som syftar till att föra skräddarsydda, kombinerade riktade behandlingar till en stor och tidigare eftersatt grupp lungcancerpatienter.
Citering: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Nyckelord: BRAF‑muterad lungcancer, pan‑RAF‑hämmare, MAPK‑signalering, läkemedelsresistens, kombinationer av riktade behandlingar