Clear Sky Science · sv
Ärftliga förändringar i kromatinkontakter kopplade till transgenerationell känslighet för kostinducerad insulinstörning och fetma
När förfädernas kost möter moderna midjor
Varför går vissa personer lättare upp i vikt och får problem med blodsockret än andra, även när deras egen livsstil verkar sund? Denna studie utforskar en oroande möjlighet: att exponering för vissa industrikemikalier under graviditet tyst kan ”förbereda” ättlingar, flera generationer senare, att reagera dåligt på energirik kost. I möss visar forskarna en mekanism för hur denna risk kan föras vidare utan att DNA-bokstäverna ändras, genom att omforma hur genomet viks inne i cellerna.
En kemikalie som lämnar en lång skugga
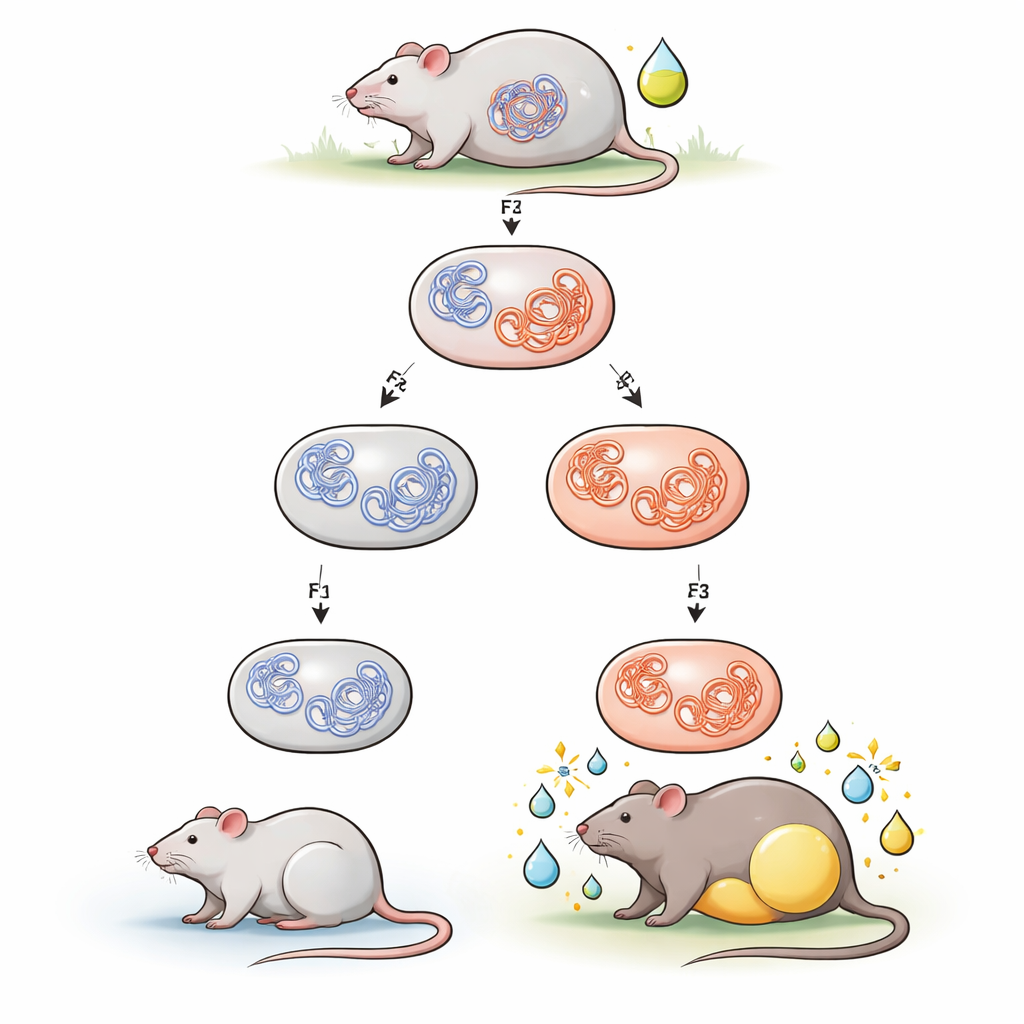
Gruppen koncentrerade sig på tributyltin, en tidigare vanlig antifouling- och industriförening känd som obesogen eftersom den främjar fettinlagring. Dräktiga möss gavs låga doser tributyltin i dricksvattnet under dräktigheten. Deras avkomma (första generationen) exponerades i livmodern, deras barnbarn (andra generationen) exponerades som utvecklande germceller inne i dessa avkommor, och deras barnbarnsbarn (tredje generationen) exponerades aldrig direkt. När unga vuxna ättlingar byttes från standardfoder till en fettrikare kost fick hannar vars förfäder utsatts för tributyltin mer kroppsfett och större viktökning än oexponerade kontroller. Honor, däremot, visade liten eller ingen förändring. Denna hannspecifika benägenhet för kostinducerad fetma stämmer överens med tidigare arbete från samma grupp.
Genomvikning som ett dolt minne
För att förstå hur denna egenskap kan ärvas utan DNA-mutationer undersökte forskarna primordiala germceller från embryo i de första tre generationerna. Det är de omogna cellerna som så småningom bildar spermier och ägg. Med en teknik som kartlägger vilka DNA-bitar som rör vid varandra i tredimensionellt utrymme sökte de bestående förändringar i kromosomernas vikningsmönster. De fann att kontaktmönstret överlag var relativt stabilt. Men i manliga germceller stack en liten region på kromosom 19 ut: en kluster av nya, förstärkta kontakter uppträdde och bestod från de direkt exponerade embryona genom två oexponerade generationer. Denna region innehåller genen Ide, som kodar för insulin-degraderande enzym, ett centralt protein som normalt hjälper till att rensa insulin från blodomloppet.
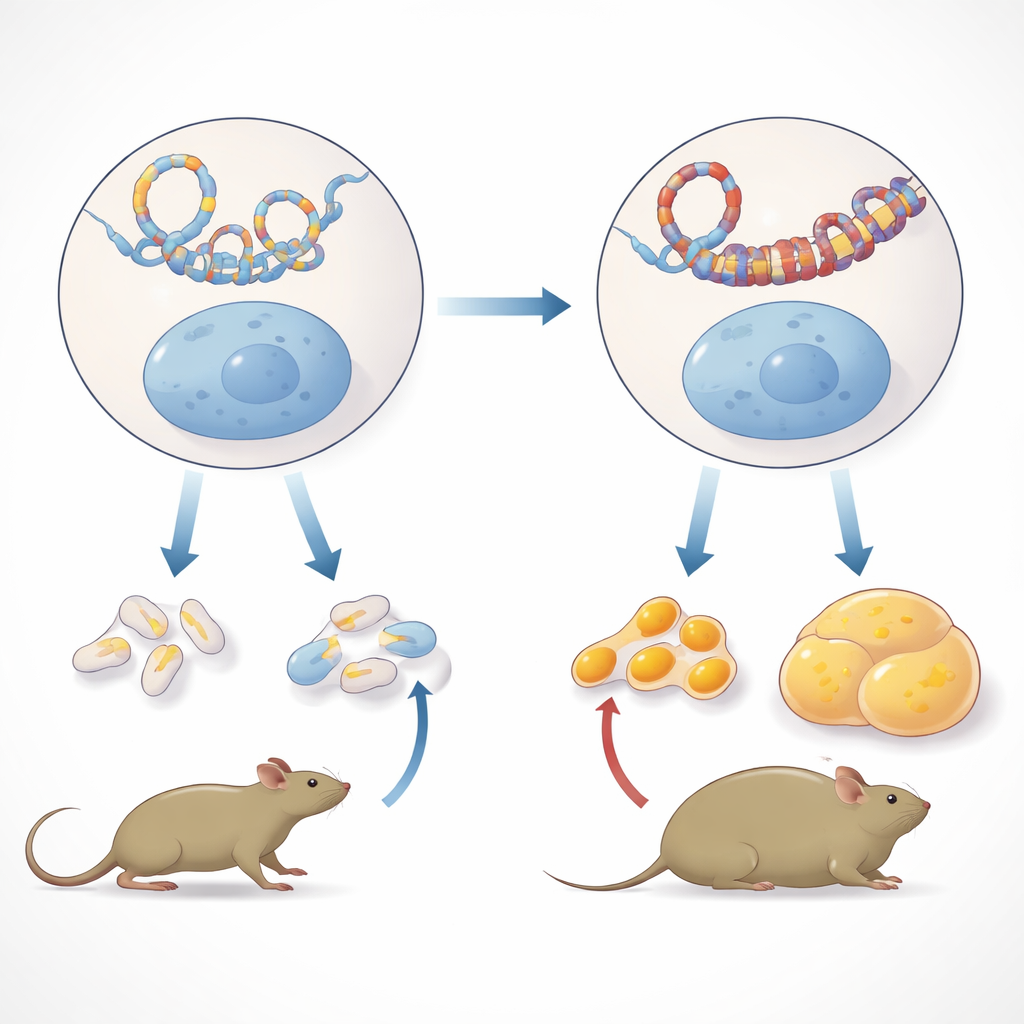
En enda gen i hjärtat av det metabola skiftet
Forskarna frågade sedan om dessa förändrade DNA-kontakter fick följder i vanliga kroppsvävnader. I levern hos vuxna barnbarnsbarn till de exponerade mössen såg de starkare bindning av ett genom-organiserande protein kallat CTCF vid flera platser inom Ide-regionen, vilket är förenligt med bildandet av en ny kromatinloop. Samtidigt sjönk Ide-aktiviteten i hannars lever, medan närliggande gener Hhex och Kif11 blev mer aktiva. Mönstret framträdde inte i honors lever eller i andra manliga vävnader såsom muskel, fettkuddar, hjärna eller mjälte, vilket understryker dess vävnads- och könsspecifika natur. Viktigt är att författarna uteslöt en enkel strukturell duplikation av denna kromosomdel som förklaring, genom att visa att kopieringssiffran för Ide-regionen inte skiljde sig mellan exponerade och kontrollinjer.
Från förändrad insulinrensning till fetma
Eftersom insulin-degraderande enzym hjälper till att avlägsna insulin från cirkulationen borde minskad Ide-aktivitet lämna mer insulin i blodet. Det var precis vad forskarna observerade. Redan innan fettrikedieten hade manliga ättlingar till tributyltinexponerade honor förhöjda insulinnivåer och högre värden på ett standardindex för insulinresistens, trots normalt fasteblodsocker. Efter veckor på en rikare diet utvecklade de både högt blodsocker och höga insulinnivåer, tillsammans med större fettdepåer och förhöjt leptin, ett hormon kopplat till kroppsfett. Nivåerna av C‑peptid, som speglar hur mycket insulin som produceras, ökade likartat i exponerade och kontroll‑djur. Den avgörande skillnaden var förhållandet mellan C‑peptid och insulin, vilket pekade mot nedsatt nedbrytning av insulin snarare än ökad sekretion—i linje med den observerade minskningen av hepatic Ide.
Vad detta betyder för arv och hälsa
Tillsammans beskriver fynden en händelsekedja: förfäders exponering för en obesogen kemikalie omformar subtilt hur en specifik region av genomet viks i manliga germceller; denna nya 3D‑struktur återskapas i levern hos manliga ättlingar och dämpar en enskild insulinrensande gen; som följd bär dessa djur kroniskt högre insulinnivåer och är förberedda att lägga på sig fett och utveckla blodsockerproblem när de utsätts för fettrik kost. För en allmän läsare är huvudbudskapet att det förfäder möter i sin miljö kan lämna ett fysiskt ”minne” i hur DNA paketteras — inte genom att ändra den genetiska koden utan genom att ändra dess form. Det minnet kan tyst påverka hur senare generationer reagerar på moderna dieter, vilket betonar vikten av att begränsa skadliga exponeringar långt innan hälsoproblem uppträder.
Citering: Chang, R.C., Egusquiza, R.J., Amato, A.A. et al. Heritable changes in chromatin contacts associated with transgenerational susceptibility to diet-induced insulin dysregulation and obesity. Nat Commun 17, 2662 (2026). https://doi.org/10.1038/s41467-026-69214-5
Nyckelord: transgenerationell epigenetik, obesogener, insulinresistens, kromatinstruktur, miljöexponering