Clear Sky Science · sv
Ingenjörskonst med cytokrom P450-enzym som peroxygenas för selektiv hydroxylering av steroider
Att göra mediciner av svårstyrda molekyler
Steroida läkemedel — från antiinflammatoriska tabletter till hormonterapier — är bland de mest använda medicinerna i världen. Att finjustera dessa molekyler, genom att lägga till en enskild syreatom exakt på rätt ställe, är emellertid notoriskt svårt med traditionell kemi. Denna studie visar hur forskare omformade ett naturligt enzym så att det kan precisera "putsa" steroidmolekyler med enkel väteperoxid, vilket potentiellt ger grönare och billigare vägar till viktiga läkemedel.
Varför steroider är svåra att anpassa
Steroider är uppbyggda av en kompakt stapel av kolringar, med många nästan identiska kol–väte-bindningar. Konventionella kemiska metoder har svårt att rikta in sig på bara en av dessa bindningar utan att påverka andra, och kräver ofta hårda reagenser, höga temperaturer och flera skydds‑ och avskyddssteg som genererar avfall. Ändå kan små förändringar — som att lägga till en enskild hydroxylgrupp (–OH) på en specifik position — dramatiskt ändra hur en steroid beter sig i kroppen. Enzymer från cytokrom P450-familjen är naturens specialister på denna typ av precis C–H‑aktivering, men i sin naturliga form behöver de vanligtvis dyra hjälpmolekyler och syre‑hanterande maskineri, vilket begränsar deras direkta användbarhet i tillverkning.
Att hitta en lovande enzymutgångspunkt
Genom genommining identifierade forskarna ett självförsörjande P450-enzym, kallat P450stri, från en jordbakterie. Till skillnad från den klassiska arbetshästen P450BM3, som föredrar små fettsyror, accepterar P450stri naturligt skrymmande steroider som testosteron. Under sina naturliga förhållanden, drivs av det cellulära kofaktorn NADH, adderar P450stri hydroxylgrupper på tre positioner på testosteron och ger en blandning av produkter. Denna inneboende förmåga att känna igen steroider gjorde P450stri till en attraktiv "startstomme" för att skapa en mer selektiv, industriellt vänlig katalysator.
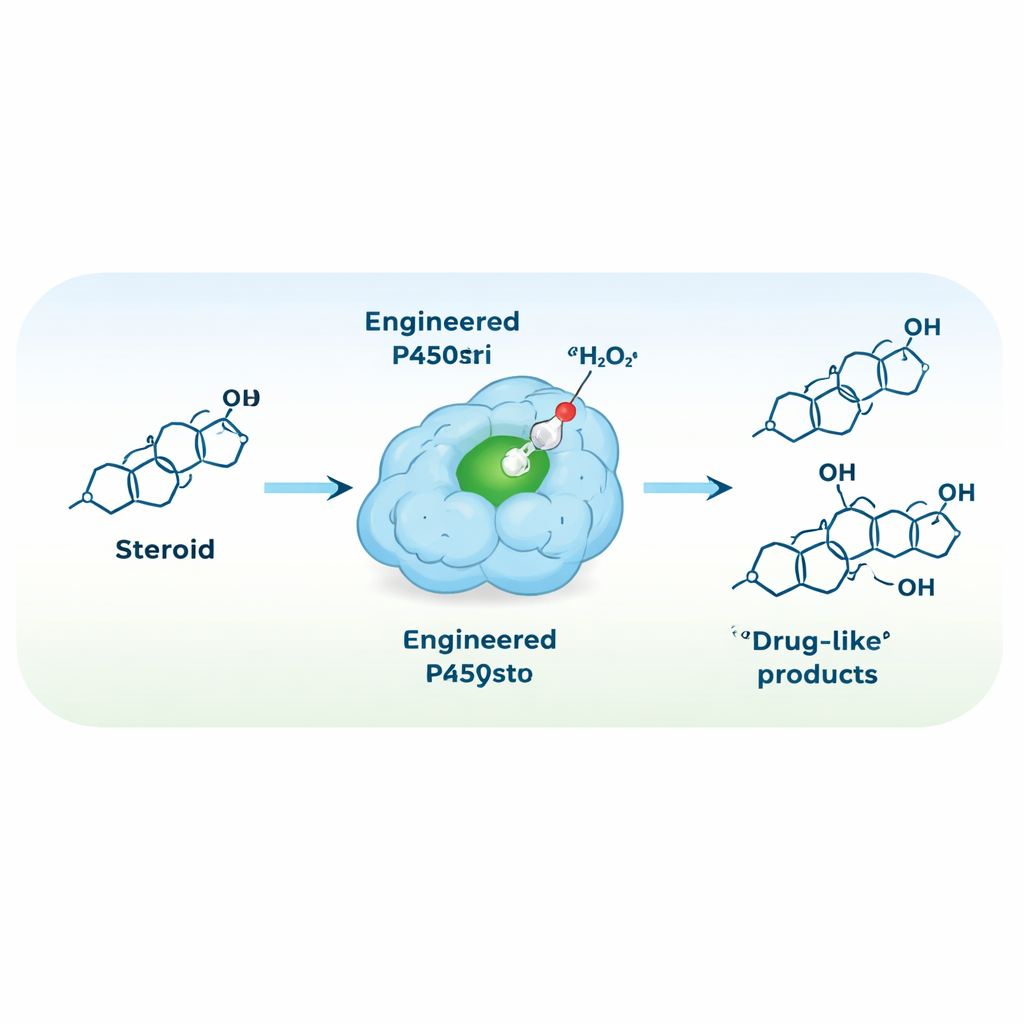
Omprogrammera enzymet att gå på väteperoxid
För att förenkla reaktionsuppställningen ville teamet omvandla P450stri till ett peroxygenas — ett enzym som använder väteperoxid direkt som oxideringsmedel och därmed eliminerar behovet av dyra kofaktorer och hjälpproteiner. En enda strategisk mutation, där en klumpig fenylalanin precis ovanför heme‑centret byttes mot en mindre alanin, skapade en variant kallad M1. Denna förändring öppnade utrymme kring den reaktiva järncentret och gjorde förvånansvärt nog enzymet både mer tolerant mot höga väteperoxidsnivåer och betydligt mer selektivt. I det nya, peroxiddrivna läget omvandlade M1 testosteron huvudsakligen till en enda produkt, hydroxylerad vid 15β‑positionen, med cirka 94 % selektivitet — upp från 35 % i ursprungsenzymet.
En "rund kolv"-modell för smartare enzymdesign
För att driva prestandan längre introducerade författarna ett designkoncept de kallar "Round Flask"‑modellen. De ser den aktiva platsen där kemin sker som den rundade botten och de smala åtkomsttunnlarna som halsen och locket. Botten bestämmer vilken position på steroiden som modifieras, medan halsen kontrollerar hur lätt steroiden och väteperoxiden når det reaktiva centret. Med vägning av computersimuleringar och tunnelkartläggningsprogramvara justerade de systematiskt en liten uppsättning aminosyror som kantar dessa tunnlar och stämde deras storlek och hydrofobicitet. Denna tvådimensionella strategi gav en särskilt framstående variant, M4, som bibehöll hög 15β‑selektivitet samtidigt som den kraftigt ökade reaktionshastigheten och tolererade väteperoxidskoncentrationer upp till flera hundra millimolar.
Från labb-bänk till skalbara steroiduppgraderingar
Det designade M4‑enzymet testades sedan i större skala med testosteron och en närbesläktad steroid som används i prestationshöjande sammanhang. I enkla vattenbaserade blandningar vid rumstemperatur, drivna endast av väteperoxid, omvandlade M4 över 90 % av startmaterialet och gav isolerade 15β‑hydroxylerade produkter i utbyten kring 75–80 %. Dessa förhållanden är mycket mildare och renare än typiska kemiska vägar. Slutligen visade teamet att genom att överföra de nyckelmutationerna till flera relaterade P450‑enzymer i samma evolutionära "gren" kunde de pålitligt omvandla dem till liknande selektiva och effektiva peroxygenaser, vilket lyfter fram generaliteten i deras designregler.
Vad detta betyder för framtida läkemedel
För en icke‑specialist är slutsatsen att forskarna har lärt ett naturligt enzym att fungera som en högt precis, peroxiddriven "mikrofabrik" för modifiering av steroidläkemedel. Genom att kombinera en enkel konceptuell modell med riktade mutationer skapade de ett enzym som kan lägga till en OH‑grupp på precis rätt ställe, under skonsamma och skalbara förhållanden, och sedan överföra denna strategi till närbesläktade proteiner. Detta angreppssätt kan effektivisera produktionen av befintliga steroider, öppna vägar till nya läkemedelskandidater och tjäna som en ritning för att ingenjörsmässigt skapa andra enzymer som rent aktiverar svårforcerade C–H‑bindningar i komplexa molekyler.
Citering: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Nyckelord: steroidbiokatalys, cytochrom P450-ingenjörskonst, peroxygenas, väteperoxidkatalys, selektiv hydroxylering