Clear Sky Science · sv
Encells-strukturbio med intracellulär elektronkristallografi
Att se livets form, en cell i taget
Proteiner är de små maskiner som håller varje cell vid liv, men för att verkligen förstå hur de fungerar behöver forskare se deras tredimensionella former i detalj. Traditionellt har det inneburit att rena stora mängder protein och odla stora, känsliga kristaller utanför cellen—ofta en lång och felbenägen process. Denna studie presenterar ett nytt sätt att läsa av proteinstruktur direkt från en enskild kristall inuti en enskild cell, med elektroner istället för röntgenstrålar. Det pekar mot en framtid där högupplöst strukturbio kan utföras i vanliga laboratorier, och till och med på nivån av enskilda celler.
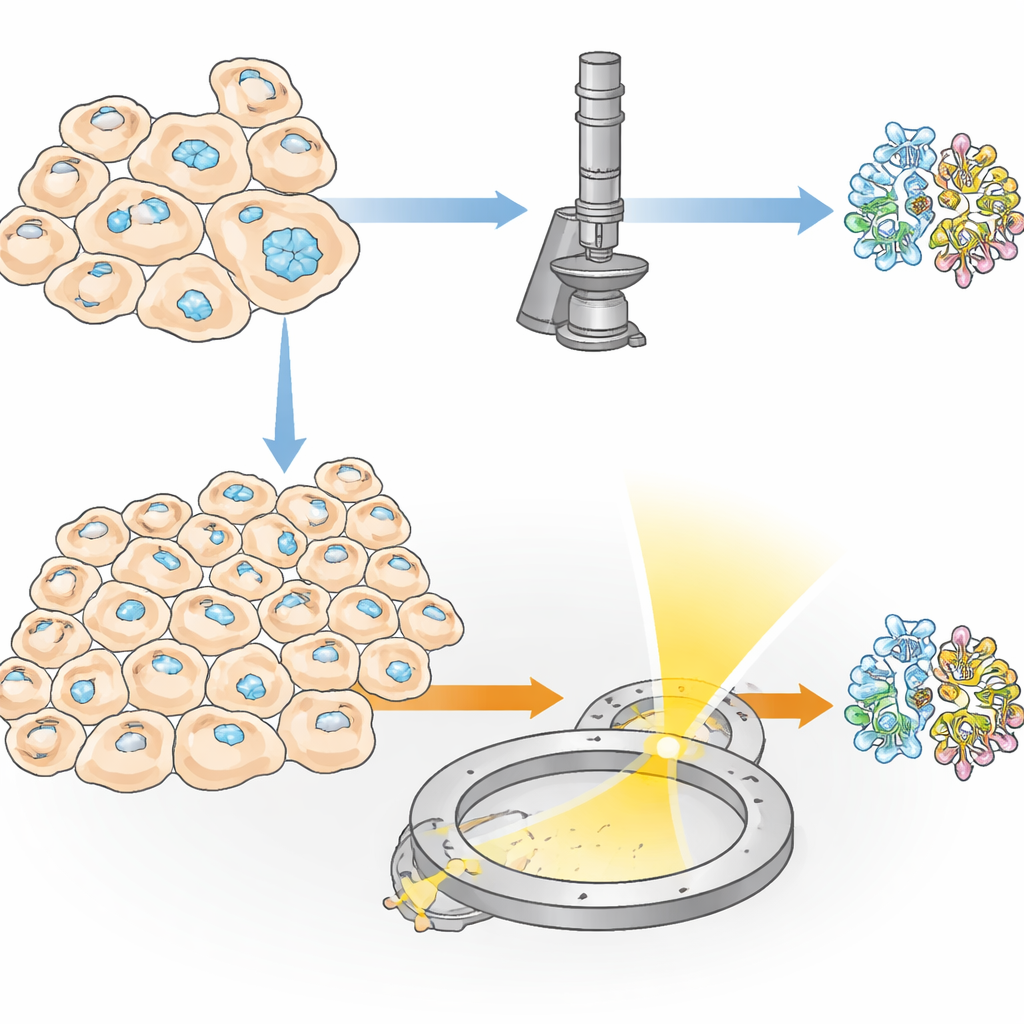
Kristaller dolda inne i levande celler
Vissa proteiner samlas naturligt i små kristaller inne i levande celler och tjänar syften som lagring, skydd eller att hjälpa celler att svara på stress. Forskare kan också få celler att producera sådana kristaller genom att konstruera dem för att framställa stora mängder av ett valt protein. Denna ”in‑cell”-kristallisering har två stora fördelar: proteinet lämnar aldrig sin naturliknande miljö, och ömtåliga detaljer—som sockergrupper eller små bundna molekyler—kan bevaras på sätt som ofta misslyckas vid vanlig provrörskristallisering. Ett stort hinder har dock bestått: i många experiment bildar bara en liten bråkdel av cellerna faktiskt kristaller, så traditionella röntgenmetoder behöver tiotusentals kristaller och därmed enorma mängder celler.
En ny väg: elektroner istället för röntgen
Författarna introducerar en metod de kallar IncelluloED, som förenar in‑cell‑kristallisering med tredimensionell elektrondiffraction. Elektroner interagerar mycket starkare med materia än röntgenstrålar, vilket innebär att användbara data kan samlas in från kristaller som både är mindre och färre till antalet. Teamet valde ett svampprotein kallat HEX‑1, som normalt bildar hexagonala kristaller som hjälper till att täppa igen små porer mellan svampceller under stress. Genom att producera detta protein inne i insektsceller skapade de regelbundna mikroskopiska kristaller som tjänade som ett testfall för den nya arbetsflödet.
Att förvandla en kristall till en detaljerad karta
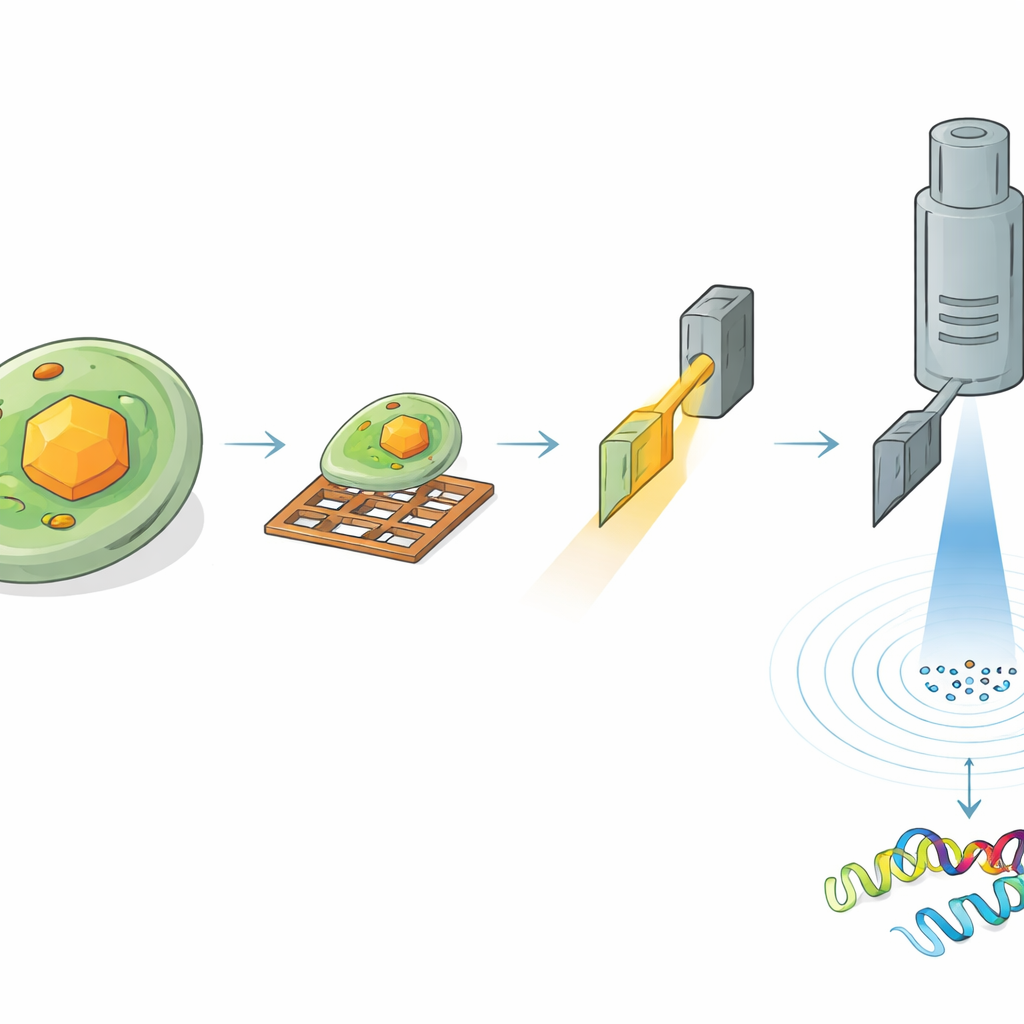
För att läsa strukturen av HEX‑1 inne i en cell behövde forskarna hitta och försiktigt glesa ut rätt region av provet. Först frös de de kristallbärande cellerna på små metallgaller och belade ytan med ett tunt platinaskikt. Med kryogen ljusmikroskopi skannade de stora områden av gallret för att lokalisera celler som innehöll kristaller och mätte kristallernas tredimensionella positioner under ytan. Därefter flyttade de samma prov till ett specialiserat instrument som kombinerar svepelektronmikroskop med fokuserad jonstråle. Med vägledning av de tidigare ljusbilderna fräste de bort omgivande material för att karva ut en ultratunn skiva, eller lamella, som passerade genom en vald kristall, bara ett par hundra nanometer tjock—idealisk för att elektroner ska kunna passera igenom.
Elektroner avslöjar atomdetaljer från mikroskopiska volymer
De förberedda lamellerna fördes sedan över till ett avancerat elektronmikroskop som kördes vid kryogena temperaturer. När kristallskivan långsamt roterades i mikroskopet passerade en finkontrollerad elektronstråle genom den och skapade en serie diffraktionsmönster—delikata punktarrangemang som kodar atomernas positioner. Från en kristallvolym på ungefär 1,6 kubikmikrometer rekonstruerade teamet hela 3D‑strukturen av HEX‑1 vid 1,9 ångströms upplösning, tillräckligt skarp för att modellera de flesta av proteinets sidokedjor. Ännu mindre volymer på omkring 0,8 kubikmikrometer gav en nästan identisk struktur med bara något lägre upplösning. Viktigt är att de resulterande modellerna stämde väl överens med dem som erhölls med en konventionell seriel röntgenmetod som krävde mer än 60 000 kristaller och en total kristallvolym ungefär sju miljoner gånger större.
Hur detta förändrar spelet i strukturbio
Sidosvisa jämförelser visade att strukturen bestämd från en enda in‑cell elektrondiffraktionskristall i huvudsak är densamma som den som genomsnittligt erhålls från tiotusentals kristaller med röntgen. Eventuella skillnader var små och mest begränsade till flexibla slingor, där naturlig rörelse förväntas. Forskarna visade också att de elektrondoser som användes var tillräckligt låga för att undvika allvarliga strålningsskador, och att varje kristall de bearbetade gav data av hög kvalitet. Även om förberedelsen av de tunna lamellerna fortfarande kräver skicklighet och tid, är de nödvändiga instrumenten—kryo‑ljusmikroskop, fokuserade jonsystem och kryo‑elektronmikroskop—nu vanliga i många forskningscentra.
Från många celler till ett enkelscells‑strukturlabb
Denna studie visar att det nu är möjligt att bestämma en atomnivå proteinstruktur från bara en kristall inne i en cell, utan att någonsin rena proteinet. IncelluloED kan vara särskilt kraftfull när endast några få celler bildar kristaller, eller när proteiner är svåra att isolera utan att förlora viktiga partners eller kemiska grupper. När arbetsflödet blir mer automatiserat och kan tillämpas på andra proteiner kan det göra det möjligt för forskare att utforska hur strukturer varierar från cell till cell, studera sjukdomsrelaterade förändringar i deras naturliga miljö och till och med stödja läkemedelsupptäckt direkt i levande celler. I praktiken för detta arbetet visionen om ett ”enkeltcells‑strukturlaboratorium” mycket närmare verkligheten.
Citering: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Nyckelord: elektrondiffraction, in cellulo-kristallografi, strukturbio på enskild cell, proteinstruktur, cryo-EM