Clear Sky Science · sv
14-3-3ζ interagerar med DNA-bindande domän hos FOXO3a och dissocierar DNA konkurrerande genom dubbel-motiv-tethering
Hur cancerceller stänger av sin egen nödstoppsignal
Våra celler har inbyggda felsäkringssystem som kan utlösa celldöd när de blir för skadade eller farliga. Ett av dessa system regleras av ett protein kallat FOXO3a, som slår på gener som får avvikande celler att begå självmord. Många cancerformer hittar dock sätt att tysta FOXO3a och fortsätta växa. Denna studie går på djupet i de molekylära detaljerna för hur ett annat protein, 14-3-3ζ, hjälper cancerceller att dra loss FOXO3a från DNA och inaktivera detta nödstoppssystem.
Vaktproteinet som skjuter tillbaka mot cancer
FOXO3a fungerar som en säkerhetsinspektör för cellen. Det binder till specifika platser på DNA och aktiverar gener som bromsar tillväxt eller utlöser programmerad celldöd (apoptos) när något går fel. I friska celler hjälper detta till att förhindra tumörbildning. I många cancerformer däremot blir en tillväxtfrämjande signalväg driven av muterade Ras-proteiner permanent påslagen. Denna väg aktiverar ett kinas kallat AKT, som kemiskt märker FOXO3a på flera platser med fosfatgrupper. Dessa märken skapar anslutningspunkter för 14-3-3ζ, ett dimeriskt "adapter"-protein som känner igen fosforylerade motiv på många mål. När 14-3-3ζ hakar fast vid FOXO3a börjar cellens interna bromsar att svikta.
Varför enkel bindningsstyrka inte kunde förklara effekten
Tidigare arbete på ett närbesläktat protein, FOXO4, föreslog att 14-3-3-proteiner drar FOXO-faktorer från DNA helt enkelt för att de binder starkare. Men FOXO3a föredrar sina naturliga DNA-mål mer strikt än den äldre modellen antog. I denna studie framställde forskarna en version av FOXO3a som inkluderar den DNA-bindande domänen och två viktiga fosforyleringsställen. De mätte hur starkt detta protein binder antingen DNA eller 14-3-3ζ och fann att skillnaderna i bindningsstyrka var måttliga: 14-3-3ζ var bara ungefär två gånger starkare partner än DNA. Ändå kunde 14-3-3ζ i blandningsförsök som följer hur molekyler rör sig genom en kromatografikolonn driva nästan fullständig frigörelse av DNA från FOXO3a, som om det var ungefär 100 gånger mer konkurrenskraftigt än väntat. Denna diskrepans antydde att en extra mekanism var i spel.
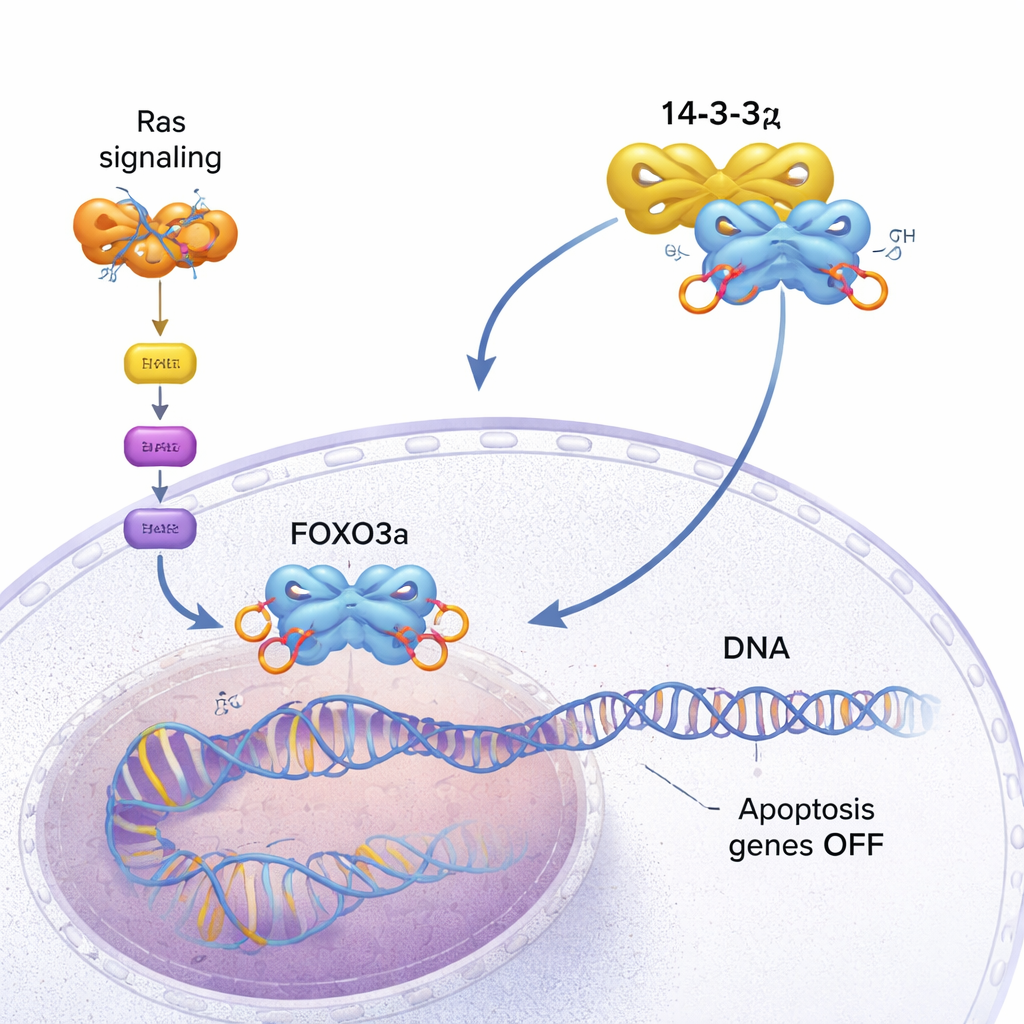
Ett trepunktsgrepp som tränger ut DNA
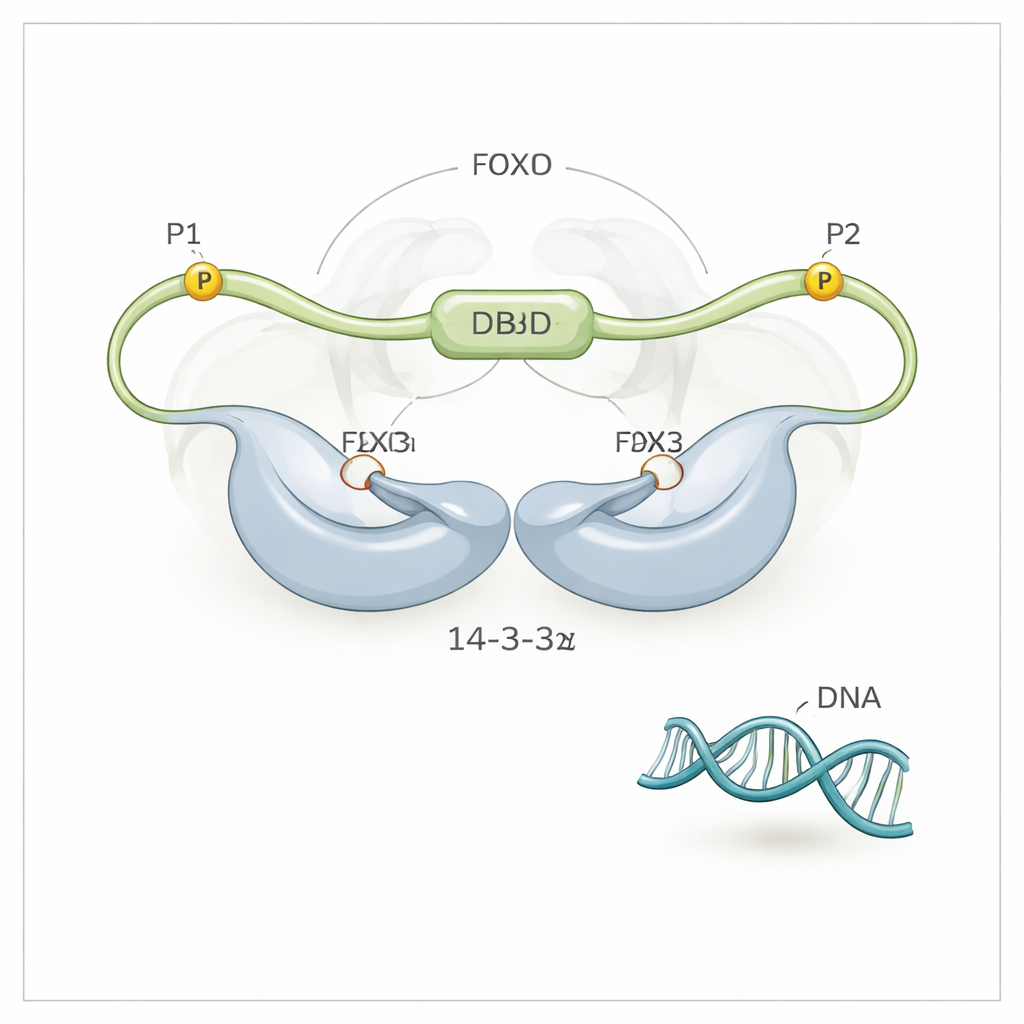
Med hjälp av högupplöst NMR-spektroskopi upptäckte teamet att 14-3-3ζ gör mer än att bara gripa FOXO3a vid dess två fosforylerade motiv (kallade P1 och P2). Det gör också direkt, om än svagare, kontakt med FOXO3as DNA-bindande domän (DBD) själv — just den yta som normalt ligger an mot DNA. 14-3-3ζ-proteinet bildar en symmetrisk dimer med två fåra. Varje fåra klämmer fast ett av de fosforylerade motiven på FOXO3a och förankrar FOXO3a i två punkter till 14-3-3ζ. Eftersom ett av dessa motiv (P2) ligger mycket nära i kedjan till den DNA-bindande domänen, håller denna "dubbel-motiv-tethering" effektivt 14-3-3ζ intill DBD, vilket kraftigt ökar chansen att DBD:n stöter på och binder ytan på 14-3-3ζ istället för DNA. Forskarna kunde till och med se att DBD:n växlar fram och tillbaka mellan de två sidorna av 14-3-3ζ-dimern och tillbringar större delen av tiden skärmad från DNA.
Vilka fosfattaggar spelar störst roll
För att reda ut rollerna för de två fosforylerade ställena konstruerade teamet FOXO3a-varianter där endast ett ställe i taget kunde fosforyleras. När endast P2-stället nära DBD var aktivt kunde 14-3-3ζ delvis lossa DNA men inte fullständigt. När endast det mer avlägsna P1-stället var aktivt kunde 14-3-3ζ binda FOXO3a men påverkade knappt dess grepp om DNA. Fullständig DNA-frigörelse krävde att båda ställena samarbetade: P1 ger en högaffinitet initial landningspunkt för 14-3-3ζ, och P2 positionerar dimern tillräckligt nära DBD för att göra den lokala koncentrationen av 14-3-3ζ i det området effektivt enorm. Denna flerstegs-tethering förstärker en måttlig bindningspreferens till en kraftfull förmåga att tränga ut DNA.
Från molekylärt dragkamp till nya läkemedelsidéer
För en icke-specialist är huvudpoängen att cancerceller utnyttjar en smart bit molekylär geometri, inte bara rå bindningsstyrka, för att tysta ett viktigt tumörsuppressorprotein. 14-3-3ζ använder två små fosfatberoende ankare på FOXO3a som fästpunkter och når sedan över för att täcka den DNA-greppande ytan på FOXO3as kärndomän, vilket hindrar det från att slå på gener för celldöd. Eftersom samma FOXO- och 14-3-3-familjer används brett i många vävnader är denna dubbel-tethering-strategi sannolikt vanlig i andra cancerformer också. Att störa antingen de fosfatberoende ankarlänkarna eller den svagare kontakten med FOXO3as DNA-bindande yta skulle kunna återställa dess förmåga att aktivera självdödsprogram i tumörceller och erbjuder lovande nya vägar för anticancerläkemedelsdesign.
Citering: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Nyckelord: FOXO3a, 14-3-3-proteiner, apoptos, Ras–AKT-signalering, cancerterapier