Clear Sky Science · sv
Vävnadsresidenta makrofagers överlevnad beror på mitokondriefunktion reglerad av SerpinB2 vid kronisk inflammation
Varför fettets immunceller spelar roll
De flesta ser kroppsfett som passiv lagring, men det är i själva verket en livlig vävnad fylld med immunceller som hjälper till att styra inflammation och blodsocker. Denna studie visar hur en specifik grupp långlivade immunceller i djupt bukfett fungerar som väktare mot typ 2‑diabetes — och hur kronisk inflammation vid fetma tyst dödar dem genom att skada deras små kraftverk, mitokondrierna.
Två slags fettväktare
Visceralt fett — fettet packat runt de inre organen — innehåller två huvudtyper av immunceller kallade makrofager. En typ är kortlivad och ständigt förnyas från blodet; dessa ”inflammatoriska” makrofager tenderar att driva på svullnad och insulinresistens. Den andra typen är långvariga, vävnadsresidenta makrofager som föds tidigt i livet och normalt hjälper till att hålla vävnaden lugn, stödja sund fettlagring och främja kroppens insulinkänslighet. Genom att spåra dessa celler hos möss och jämföra genaktivitet visade forskarna att residenta makrofager är rika på antiinflammatoriska och insulinkänsliggörande gener, medan inkommande monocyt‑deriverade makrofager uttrycker gener som försämrar blodsockerreglering.
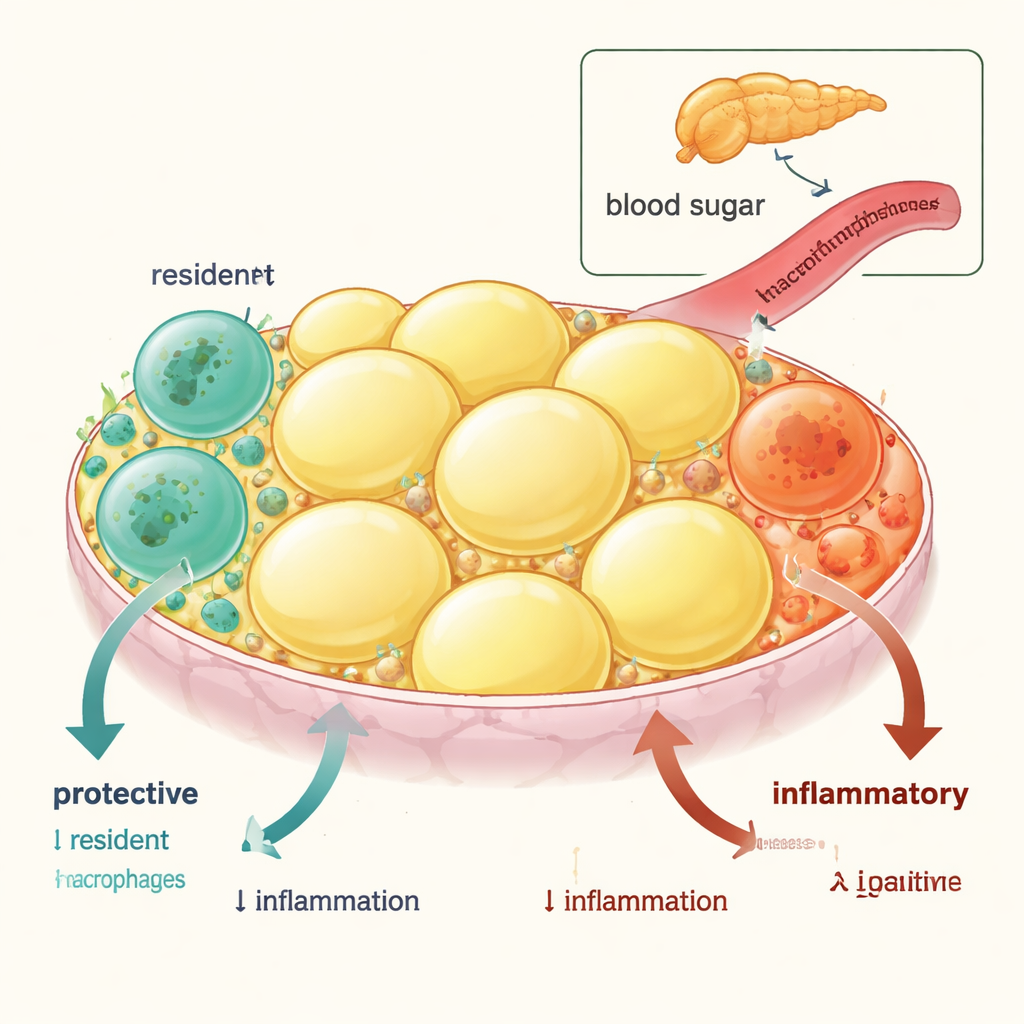
När inflammation dödar de goda
Vid fetma förskjuts denna skyddande balans. Teamet fann att både hos feta möss och hos feta eller diabetiska människor minskar antalet residenta makrofager i visceralt fett, medan inflammatoriska makrofager ökar. Noggrann bilddiagnostik och cell‑dödsmarkörer avslöjade orsaken: residenta makrofager genomgår mer programmerad celldöd (apoptos), medan de inflammatoriska cellerna inte gör det. Anmärkningsvärt nog återhämtade sig den residenta populationen långsamt genom lokal proliferation när feta möss togs bort från en fettrik diet, och den metaboliska hälsan förbättrades — vilket visar att förlusten drivs av det inflammatoriska tillståndet och kan återgå.
Ett enda protein länkar mitokondrier till överlevnad
Ett viktigt ledtråd var ett protein kallat SerpinB2, mest känt för roller i blodkoagulation. Forskarna upptäckte att SerpinB2 produceras i mycket höga nivåer inne i residenta makrofager, men mycket mindre i inflammatoriska. Hos feta människor och möss minskade residenta makrofager kraftigt uttrycket av SerpinB2, och högre body mass index var associerat med färre SerpinB2‑positiva celler. Experiment i celler utan SerpinB2 visade ökad läckage av cytokrom c — ett avgörande protein — från mitokondrierna till cytoplasman, en klassisk utlösare av apoptos. Dessa SerpinB2‑defekta makrofager hade färre antioxidantförsvar, mer mitokondriell reaktivt syre (ROS) och högre syreförbrukning, alla tecken på stressade, överarbetade mitokondrier som driver celler mot inflammatoriskt beteende och död.
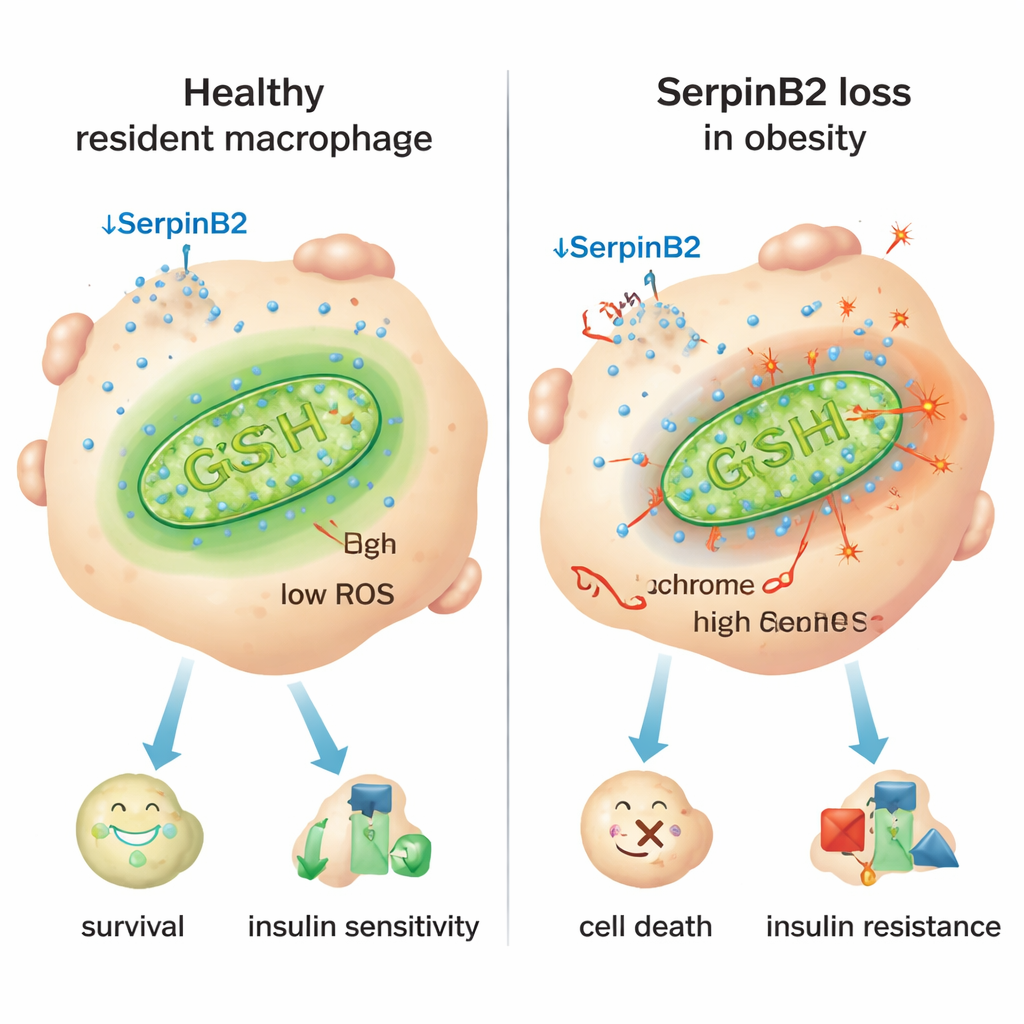
Den inflammatoriska brytaren och en möjlig lösning
Studien spårade denna mitokondriella stress tillbaka till kroniska inflammatoriska signaler vid fetma, särskilt immungsmävaren interferon‑γ (IFN‑γ), som produceras i överskott i fettvävnad. IFN‑γ aktiverar en transkriptionsrepressor kallad Ikaros som binder till SerpinB2‑genens reglerande region och nedreglerar den. I möss som konstruerats så att deras myeloida celler inte kunde svara på IFN‑γ bevarade de residenta makrofagerna SerpinB2, överlevde bättre, och djuren visade lägre blodsocker, bättre insulinkänslighet och mindre fettceller. Omvänt förvärrade radering av SerpinB2 specifikt i makrofager glukosintolerans och insulinresistens, delvis för att fettvävnaden blev mer inflammerad och expanderade. Att öka nivåerna av antioxidantglutation med tillskottet N‑acetylcystein (NAC) återställde mitokondriellt skydd, räddade residenta makrofagers överlevnad, krympte adipocyter och förbättrade metabola mått även när SerpinB2 saknades.
Vad detta betyder för metabol hälsa
För en lekmannaläsare är huvudbudskapet att inte allt fett eller alla fettresiderande immunceller är skadliga. En specialiserad, långlivad grupp makrofager i visceralt fett skyddar oss faktiskt från okontrollerad inflammation och högt blodsocker genom att hålla sina mitokondrier friska via SerpinB2‑drivna antioxidantförsvar. Vid fetma slår kroniska inflammationssignaler ner SerpinB2, mitokondrierna blir stressade, dessa skyddande celler dör och mer skadliga makrofager tar över, vilket bidrar till insulinresistens. Arbetet pekar på att terapier som bevarar residenta makrofager — genom att blockera IFN‑γ/Ikaros‑bromsen på SerpinB2 eller genom att stödja glutationbaserade antioxidantförsvar — kan hjälpa till att förebygga eller behandla metabola sjukdomar kopplade till fetma.
Citering: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
Nyckelord: visceralt fett, makrofager, mitokondrier, insulinresistens, SerpinB2