Clear Sky Science · sv
Metabolisk ingenjörskonst för doxorubicin‑biosyntes genom optimering av P450‑redoxpartner och strukturanalys av DoxA
Varför en cancermedicins ursprungshistoria spelar roll
Doxorubicin är ett av hörnstenläkemedlen i modern cytostatikabehandling och används mot cancerformer från leukemi till brösttumörer. Trots decennier av användning är tillverkningsvägen för detta läkemedel förvånansvärt kringflackande: industrin bygger vanligen läkemedlet från ett närbesläktat föreningsstadium istället för att låta den ursprungliga mikroben slutföra processen. Denna studie klarlägger varför den producerande bakterien har svårt att genomföra de sista kemiska stegen och visar hur ombyggnad av dess interna maskineri kan kraftigt öka mängden fullständigt bildat doxorubicin, vilket öppnar för mer pålitliga och potentiellt billigare leveranser.
Från jordbakterier till livräddande medicin
Doxorubicin tillhör antracyklinerna, en familj av naturliga molekyler som byggs av jordlevande bakterier i släktet Streptomyces. Dessa föreningar delar ett styvt, platt kolramverk som kan glida in mellan DNA‑baspar, samt en sockerenhet som lägger sig i DNA:s fåror. Tillsammans låser dessa egenskaper cellens DNA‑hanteringsmaskineri och utlöser i förlängningen celldöd – användbart mot snabbt delande cancerceller. Den klassiska producenten, Streptomyces peucetius, tillverkar i huvudsak en prekursor som kallas daunorubicin och endast en måttlig mängd av det mer effektiva doxorubicinet, som skiljer sig med bara en enda extra syre‑bärande grupp. Den lilla strukturella skillnaden förbättrar aktiviteten dramatiskt men visar sig vara förvånansvärt svår för mikroben att åstadkomma effektivt.
Hitta rätt elektrisk koppling inne i cellen
Det avgörande enzymet som utför de sista tre oxidationsstegen på läkemedelsskellettet kallas DoxA, medlem i cytochrom P450‑familjen. Som en miniatyr kemisk fabrik behöver DoxA ett jämnt elektronflöde för att aktivera syre och införa nya syreatomer i läkemedelsmolekylen. Inne i bakterien levereras dessa elektroner via ett relä av hjälpproteiner kända som redoxpartners. Genomet hos S. peucetius innehåller flera kandidater, vilket gjorde oklart vilka som faktiskt paras ihop med DoxA. Genom att jämföra genaktivitet och metabolism i en normal stam, en daunorubicin‑rik mutant och en doxorubicin‑rik mutant identifierade forskarna en ferredoxin (Fdx4) och en ferredoxin‑reduktas (FdR3) som de naturliga partnerna. Återuppbyggnad av detta trio i provrörsreaktioner bekräftade att DoxA fungerar bäst när den kopplas till denna specifika elektronöverföringskedja, ungefär som att matcha rätt nätadapter till en apparat.
Lätta på enzymets självförorsakade avmattning
Även med korrekt elektrisk koppling tenderar DoxA att fastna vid det sista steget som konverterar daunorubicin till doxorubicin. Tidigare arbete antydde att produktmolekylen själv kan blockera enzymet. Gruppen vände sig till en närliggande gen, dnrV, vars funktion varit gåtfull. Biokemiska tester visade att DnrV‑proteinet tätt binder en rad antracyklineföreningar, inklusive doxorubicin, utan att kemiskt förändra dem. Att tillsätta DnrV till DoxA‑reaktioner förbättrade flödet av reaktionen avsevärt, vilket möjliggjorde fullständig omvandling av prekursorer till slutprodukten samtidigt som destruktiva sidoreaktioner undveks. I praktiska termer fungerar DnrV som en intern svamp som suger upp nysyntetiserat doxorubicin, vilket förhindrar att det proppar igen enzymet eller skadar DNA i den producerande cellen.
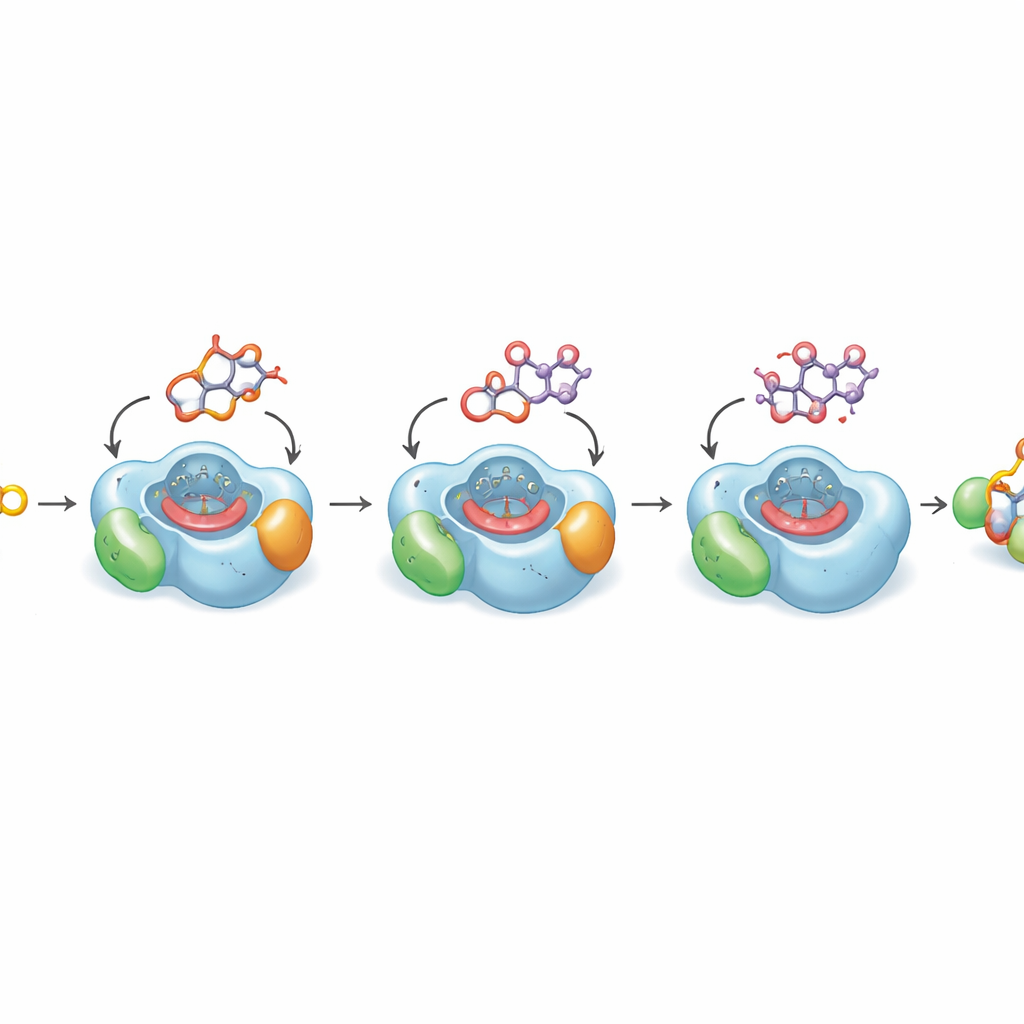
Se varför sista steget är så långsamt
För att förstå varför den avgörande sista oxidationens är inneboende långsam löste författarna högupplösta kristallstrukturer av DoxA bundet till tre successiva intermediärer. Dessa strukturer visar hur den platta läkemedelskärnan och dess bundna socker lägger sig i ett trångt fack ovanför enzymets heme‑grupp, den reaktiva metallcentra som utför oxidation. För de tidigare stegen sitter den kolatom som måste modifieras nära hemet i en ideal position för reaktion. Men i det sista substratet, daunorubicin, böjer sig den del av molekylen som behöver hydroxyleras bort från hemet in i ett litet oljigt hålrum, en arrangemang som kvantberäkningar visar är energetiskt favoriserat. Datorsimuleringar över mikrosekundskalor bekräftar att molekylen endast tillfälligt antar en produktiv position för den sista syreinsättningen. Denna strukturella bias förklarar varför omvandlingen till doxorubicin är naturligt ineffektiv.
Bygga en bättre doxorubicin‑producerande stam
Beväpnade med dessa insikter redesignade forskarna bakterien rationellt istället för att förlita sig på slumpmässig mutagenes. De introducerade en DNA‑reparationsgen för att stabilisera produktionen, och installerade sedan extra kopior av doxA, de optimala redoxpartnerna fdx4 och fdr3, samt den hjälpsamma bindaren dnrV under noga utvalda promotorer för att balansera deras uttryck. De finjusterade också odlingsförhållanden och använde specialharts för att suga upp giftiga och klibbiga intermediärer. I laboratoriekolvar och i en 20‑liters bioreaktor producerade den bästa konstruerade stammen 336 milligram doxorubicin per liter odling med en 81:19‑kvot av doxorubicin till daunorubicin—en ökning med cirka 180 % jämfört med utgångsstammen och en mycket renare produktblandning.
Vad detta betyder för framtida leveranser av cancerläkemedel
Genom att dissekera både det elektriska stödsystemet och 3D‑strukturen hos ett nyckelenzym förklarar detta arbete varför en medicinskt viktig mikroorganism presterar under förväntan i produktionen av vårt mest värdefulla antracyklin. Att matcha DoxA med dess naturliga redoxpartner, lägga till ett läkemedelsbindande hjälpprotein och återbalansera genuttrycket förvandlade en motvillig producent till en robust sådan. Även om vidare enzymoptimering kan snabba upp det sista kemiska steget ytterligare, förflyttar studien redan helt biologisk doxorubicinproduktion mycket närmare industriell verklighet. För patienter och vårdsystem kan sådana framsteg innebära säkrare, skalbara och kostnadseffektiva tillgångar till ett grundläggande cytostatikum.
Citering: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Nyckelord: produktion av doxorubicin, biosyntes av antracykliner, enzymteknik, mikrobiell läkemedelstillverkning, cytochrom P450