Clear Sky Science · sv
Aktivering av atypisk proteinkinas C driver intestinal glukosutsöndring vid diabetes mellitus
Gör tarmen till en sockerventil
Människor med diabetes lever med för mycket socker i blodet. Bariatriska ingrepp som gastric bypass kan normalisera blodsockret förvånansvärt snabbt, även innan mycket vikt har förlorats, men hur detta sker har varit ett mysterium. Denna studie avslöjar en tarmbaserad ”sockerventil” — ett sätt för tarmen att ta upp socker från blodet och spola en del av det tillbaka in i tarmlumen — vilket pekar på ett nytt läkemedelsmål som skulle kunna efterlikna operationens fördelar utan operation.
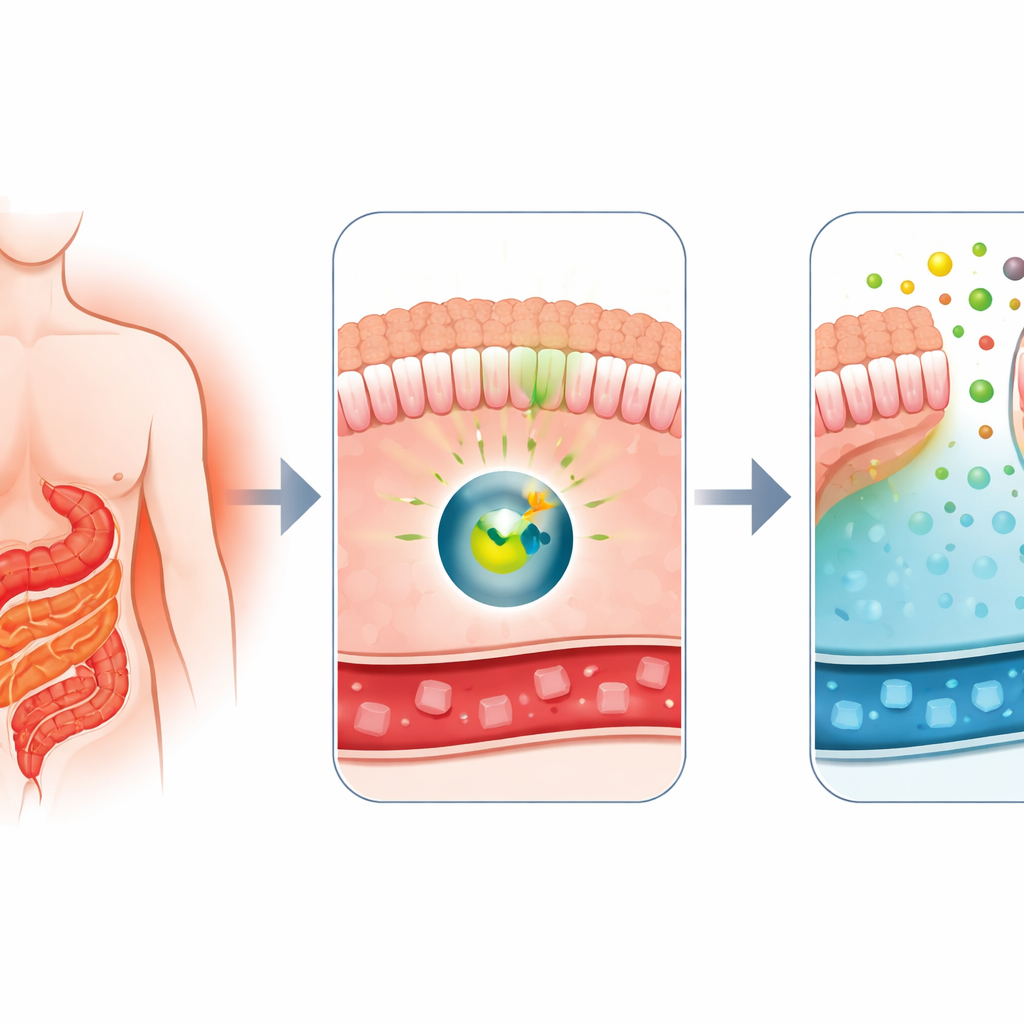
Varför kirurgi förändrar blodsockret så snabbt
Läkare har länge vetat att Roux-en-Y gastric bypass, en vanlig viktminskningsoperation, också är en av de mest effektiva behandlingarna för typ 2-diabetes. Kort efter operationen förbättras patienters blodsocker ofta dramatiskt, även innan de förlorat många kilo. Tidigare arbete från denna grupp visade att delar av tunntarmen efter bypass börjar fungera som en svamp, suga upp glukos från blodomloppet och släppa ut en del av det i tarmens inre. Det märkliga beteendet, kallat intestinal glukosutsöndring, verkade bero på en transportörprotein kallad GLUT1. Den stora frågan var: vilken molekylär strömbrytare säger åt tarmen att växla till detta sockerrensande läge?
Använde stora datamängder för att hitta en molekylär strömbrytare
För att leta efter den strömbrytaren använde forskarna ett storskaligt datorbaserat läkemedelsupptäcktsystem byggt på Connectivity Map, en databas som visar hur tusentals kemikalier ändrar genaktivitet i celler. De jämförde genuttrycksmönster från fem situationer där intestinal glukosutsöndring är hög — inklusive vävnad från bypassopererade råttor och celler behandlade med en intestinal tillväxtsignal — med mönster som produceras av kända läkemedel. En klass av föreningar stack konsekvent ut: aktivatorer av proteinkinas C (PKC), en familj enzymer som vidarebefordrar signaler inuti celler. När de grävde djupare koncentrerade sig teamet på den ”atypiska” undergruppen av PKC-enzymer, särskilt en kallad PKCζ, vars aktivitet i tarmceller bäst matchade det bypass-liknande, glukosutsöndrande tillståndet.
Tarmcellernas sockerpump i arbete
När författarna zoomade in på individuella tarmceller med hjälp av enkelcells-RNA-sekvensering fann de att bypasskirurgi ökar både PKCζ och GLUT1 i specifika näringsabsorberande celler som bekläder den distala tunntarmen. I cellkulturer och mänskliga intestinala organoider drev artificiellt ökat PKCζ eller behandling med prostratin — en växtbaserad förening som säkert aktiverar dessa atypiska PKC-enzymer — GLUT1 till cellens yta. Där fungerade GLUT1 som en tvåvägspump: den drog mer glukos från blodsiden av cellerna och gjorde det möjligt för överskottsglukos att lämna ut i tarmens inre. Viktigt är att denna omdirigering av socker inte signifikant ökade cellernas egen sockeranvändning (glykolys), vilket indikerar att huvud effekten var avyttring av glukos, inte ökad energiproduktion.
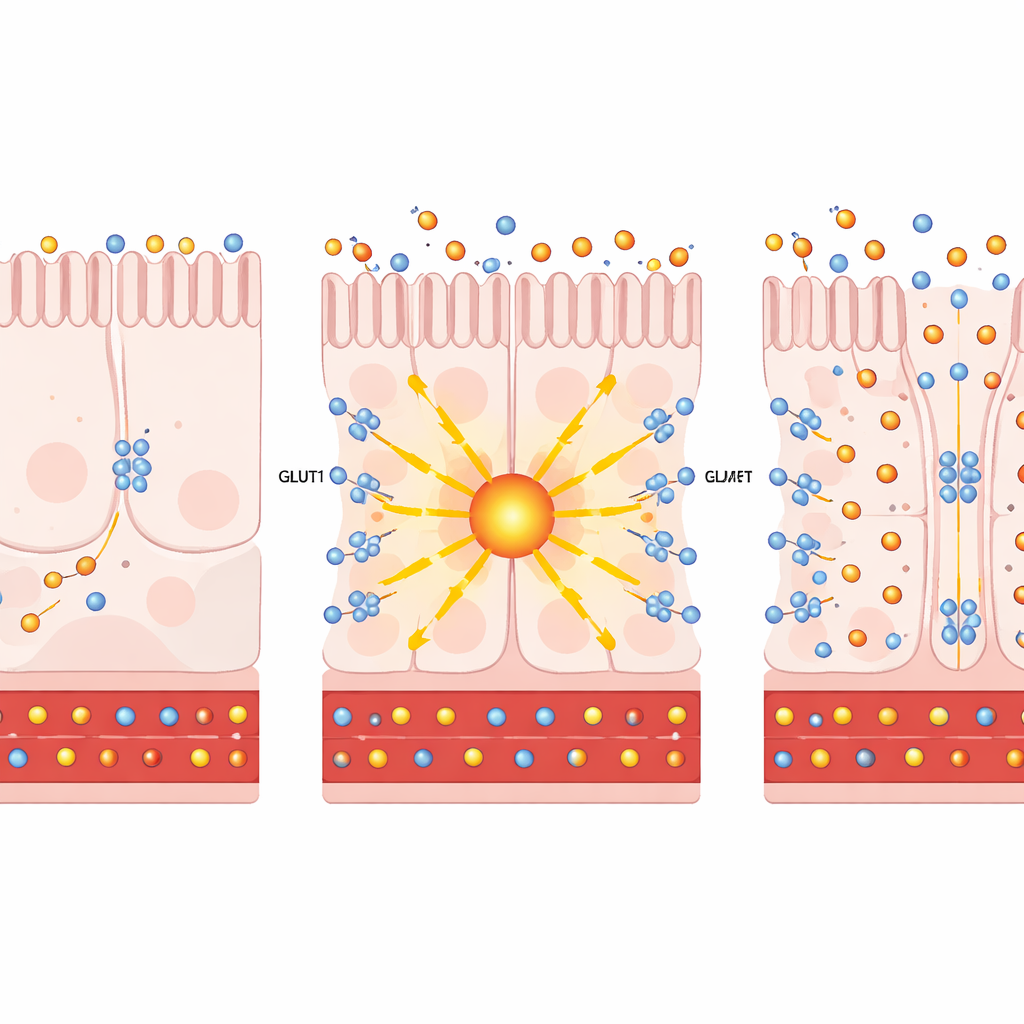
Från celler till möss: efterlikna kirurgi utan skalpell
Teamet testade sedan om aktivering av denna väg i levande djur kunde förbättra diabetes. Hos feta, insulinresistenta möss ledde leverans av extra PKCζ specifikt till tarmen till långsammare viktuppgång, lägre fasteblodsocker och bättre glukostolerans. Radioaktiva sockerspårämnen visade att mer socker togs upp av den distala tarmen och spolades ut i tarmens lumen. En liknande bild framkom i diabetiska musmodeller behandlade med prostratin: de gick upp mindre i vikt, hanterade sockerbelastningar bättre och omdirigerade mer glukos till tarmkanalen, allt utan förändringar i insulinnivåer, födointag eller tarmbarriärens integritet. I vävnadsskivor syntes GLUT1 på både blodvendande och tarmsidiga ytor av cellerna, perfekt placerad för att dra socker från cirkulationen och trycka det in i tarmen.
Vad detta kan innebära för framtida diabetesvård
För en icke-specialist är huvudbudskapet att tarmen kan omvandlas till en kontrollerad flyktväg för överskottssocker i blodet. Genom att aktivera ett specifikt enzym inne i tarmcellerna — atypisk PKC — kunde forskarna få celler att flytta fler GLUT1-transportörer till sin yta och bete sig som ett reversibelt avlopp, dra socker från blodet och dumpa en del tillbaka i tarmen. I möss förbättrade denna tarmdrivna sockeravyttring blodsockret och begränsade viktökning utan att överstimulera insulin, förändra aptit eller skada tarmen. Även om prostratin och besläktade föreningar ännu inte är godkända diabetesläkemedel, pekar detta arbete ut aPKC–GLUT1-vägen som ett lovande mål för framtida läkemedel som delvis skulle kunna reproducera de metabola fördelarna med gastric bypass utan att kräva operation.
Citering: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Nyckelord: intestinal glukosutsöndring, typ 2-diabetes, GLUT1-transportör, atypisk proteinkinas C, prostratin