Clear Sky Science · sv
MerTK-utlöst TGFβ1-autokrin signal reglerar mikroglials svar på neurodegeneration
Hur hjärnans städgrupp formar sjukdom
När nervceller i hjärnan och synnerven dör lämnar de efter sig ett spår av skräp. Specialiserade immunceller kallade mikroglia fungerar som hjärnans städgrupp och slukar detta avfall. Men mikroglia gör mer än att bara städa upp: hur de reagerar kan antingen skydda nervkretsar eller förvärra sjukdomar som Alzheimers. Denna studie avslöjar en dold självkommunikationsslinga inne i mikroglia som aktiveras av skräp från döende nervfibrer och hjälper avgöra hur starkt dessa celler svarar på skada.
En trigger gömd i döende nervfibrer
För att undersöka denna process använde forskarna en musmodell där synnerven krossas, vilket får de långa utskotten från ögonens neuroner att degenerera utan att döda cellkropparna. Det isolerar tydligt efterverkningarna av axon-sönderfall. På ytan av dessa degenererande fibrer vänder ett fetthaltigt molekyl utåt och fungerar som en ”ät mig”-signal för närliggande mikroglia. Dessa signaler uppfattas av en receptor på mikroglia kallad MerTK, en av en liten familj proteiner som känner igen skräp. Genom att selektivt ta bort MerTK i mikroglia visade teamet att utan denna receptor lyckades inte mikroglia uppbåda sitt vanliga skaderespons: de delade sig mindre, rörde sig mindre och slog på färre gener kopplade till skadekontroll och inflammation.
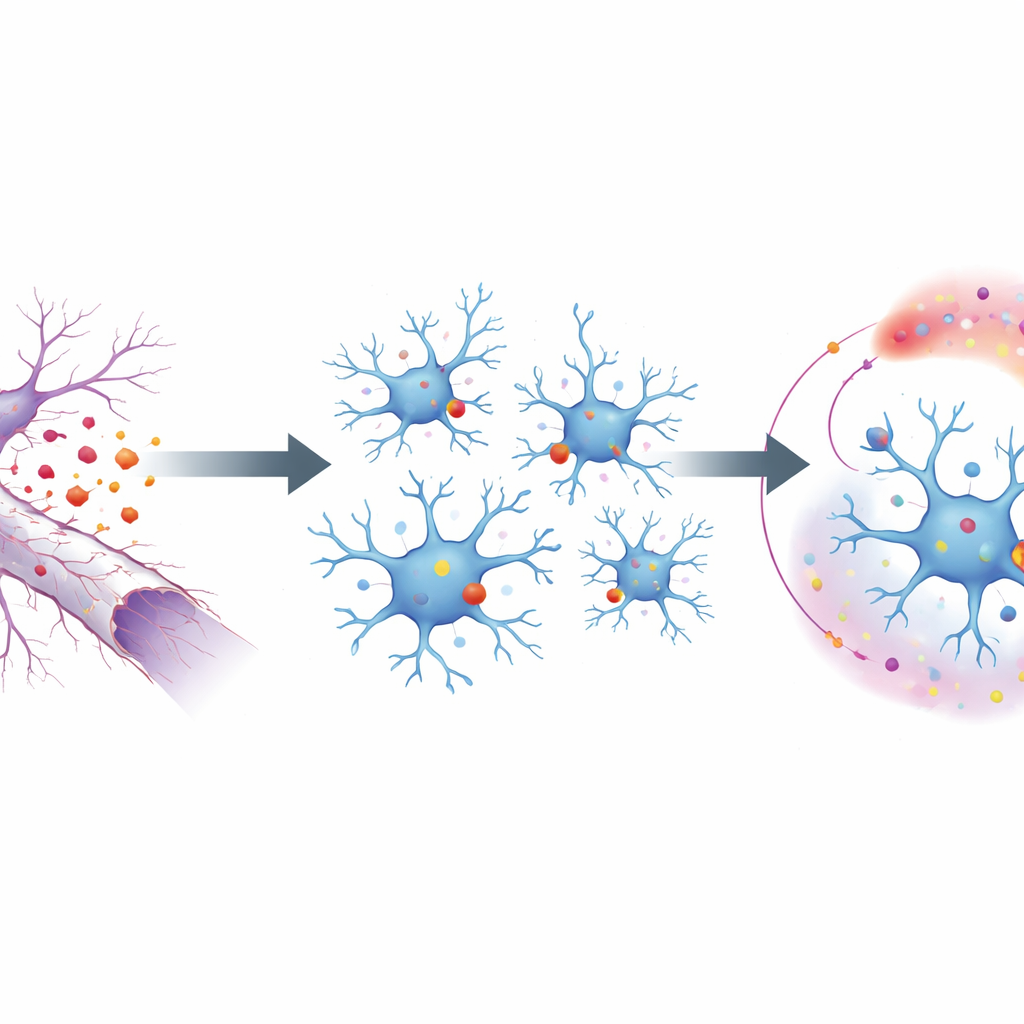
Från ytsignal till genetisk omprogrammering
När forskarna tittade inuti mikroglia spårade de hur MerTK:s ytsignal omvandlas till förändringar i genaktivitet. De fann att MerTK aktiverar en molekylär reläväg kallad fosfolipas C, som i sin tur stärker två huvudreglerande proteiner i kärnan, PU.1 och IRF8. Dessa faktorer fungerar som arbetsledare på mikroglialinjen och slår på många gener som behövs för ett aktiverat tillstånd. Genom att använda DNA-bindningskartor upptäckte teamet att PU.1 och IRF8 binder direkt till en specifik plats i genen som kodar för TGFβ1, ett kraftfullt signalprotein. När denna bindningsplats muterades så att arbetsledarna inte längre kunde fästa där, kunde mikroglia i skadade nerver inte längre öka sin produktion av TGFβ1, trots att andra basala funktioner förblev intakta.
En självförstärkande slinga i mikroglia
Nästa fråga var vad TGFβ1 faktiskt gör i detta sammanhang. Studien visar att mikroglia producerar TGFβ1 och sedan själva svarar på det, vilket bildar en autokrin, eller självåterkopplande, slinga. När TGFβ1 eller dess receptorer genetiskt togs bort endast i mikroglia, orsakade skadan fortfarande axondegeneration, men mikroglia visade inte längre sitt fulla aktiveringsprogram. De prolifererade mindre och uttryckte färre gener för skaderespons och inflammation, även om många homeostatiska identitetsmarkörer fortfarande var nedtryckta av andra signaler. En viktig downstream-molekyl i TGFβ-signaleringen, fosforylerad SMAD2, uppträdde specifikt i mikrogliala kärnor efter skada och försvann i stor utsträckning när TGFβ1 eller dess receptorer slogs ut, vilket bekräftar att självåterkopplingsslingan bröts.
Från musens synnerv till Alzheimers hjärnor
För att testa om den här vägen spelar roll bortom en artificiell skademarkör undersökte författarna en allmänt använd musmodell för Alzheimers sjukdom. Hos dessa djur visade mikroglia som klustrade runt amyloida plack höga nivåer av PU.1, IRF8, TGFβ1 och aktiverad TGFβ-signalering, vilket ekade fynden från synnerven. Teamet vände sig sedan till mänskliga data från single-nucleus RNA-sekvensering av hjärnvävnad från Alzheimerspatienter. Där utmärkte sig mikroglia som de huvudsakliga cellerna som uttryckte de mänskliga motsvarigheterna till MerTK, PU.1, IRF8 och TGFB1. I postmortem hjärnsektioner från patienter visade mikroglia också tydliga tecken på aktiv TGFβ-signalering, i kontrast till vävnad från kontrollgivare. Tillsammans talar dessa observationer för att samma självkommunikationsslinga verkar i mänsklig sjukdom.
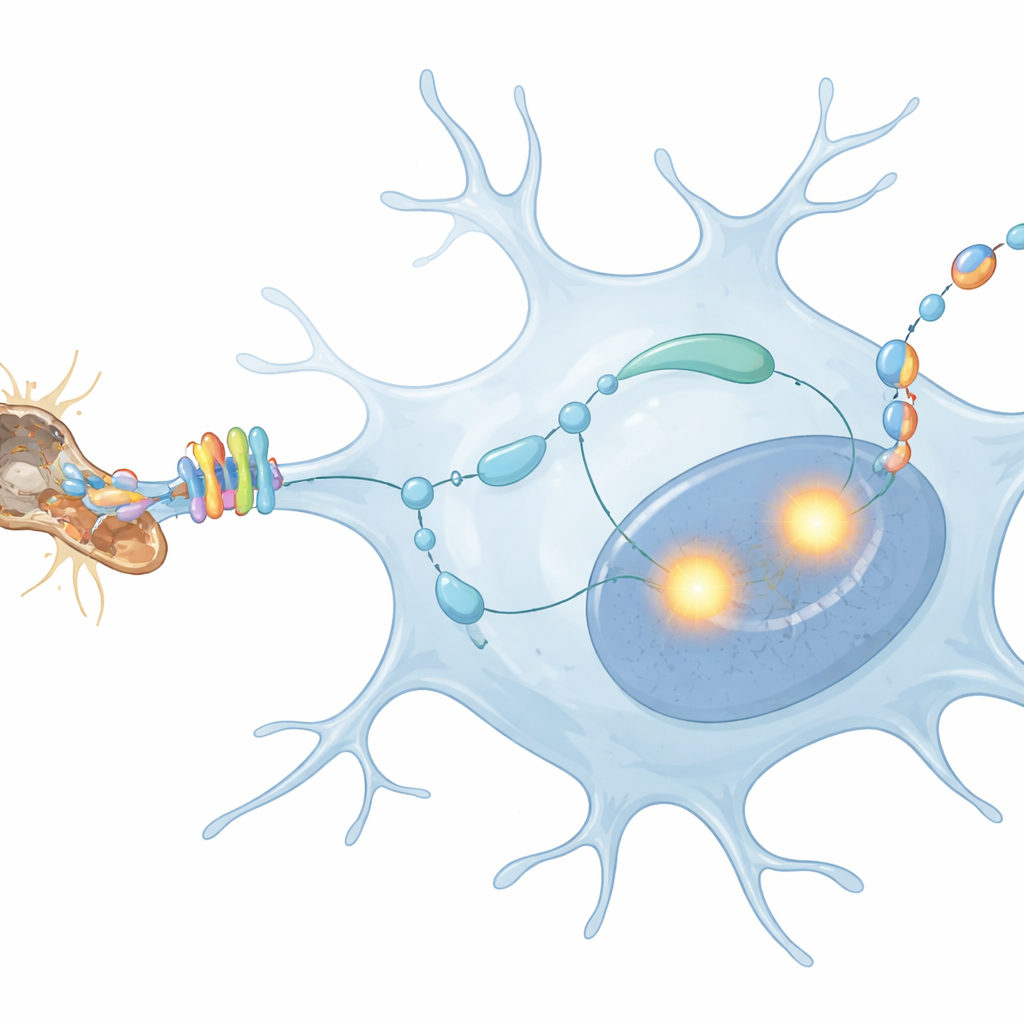
Varför detta självprat spelar roll för hjärnhälsan
Detta arbete avslöjar en händelsekedja där skräp från degenererande nervfibrer aktiverar MerTK på mikroglia, vilket sedan förstärker PU.1 och IRF8, vilka i sin tur driver mikroglia att producera TGFβ1 som återkopplar på dem själva. Detta självprat skärper och upprätthåller deras respons på neurodegeneration. För en allmän läsare är huvudbudskapet att hjärnans städare inte bara är passiva sopare; de lyssnar aktivt på sina egna signaler, och denna återkopplingsslinga kan påverka om deras handlingar hjälper till att skydda neuroner eller driver sjukdomar som Alzheimers framåt. Att förstå och eventuellt finjustera den här kretsen kan öppna nya vägar för att dämpa skadlig inflammation samtidigt som den fördelaktiga städningen som mikroglia utför bevaras.
Citering: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Nyckelord: mikroglia, neurodegeneration, Alzheimers sjukdom, hjärnans inflammation, TGF-beta signalering