Clear Sky Science · sv
Molekylär bestämningsfaktor för människans Nav1.7:s låga spänningsberoende inaktivering avslöjad av en effektbaserad Nav1.7-selektiv hämmare
Dämpa smärtsignalerna
Varför upplever vissa människor intensiv smärta av en lätt beröring, medan andra knappt känner något? En stor del av svaret ligger i små proteingateways i våra nervceller som styr elektriska signaler. Denna studie avslöjar hur en subtil strukturell särart i en sådan gateway, kallad Nav1.7, gör den särskilt viktig för att utlösa smärta — och hur en naturlig förening, Uvarigranol D, selektivt kan stänga ner den. Arbetet pekar mot en ny strategi för att utforma smärtstillande medel som tystar överaktiva smärtnervceller utan att sakta ner hjärtat eller dämpa hjärnan. 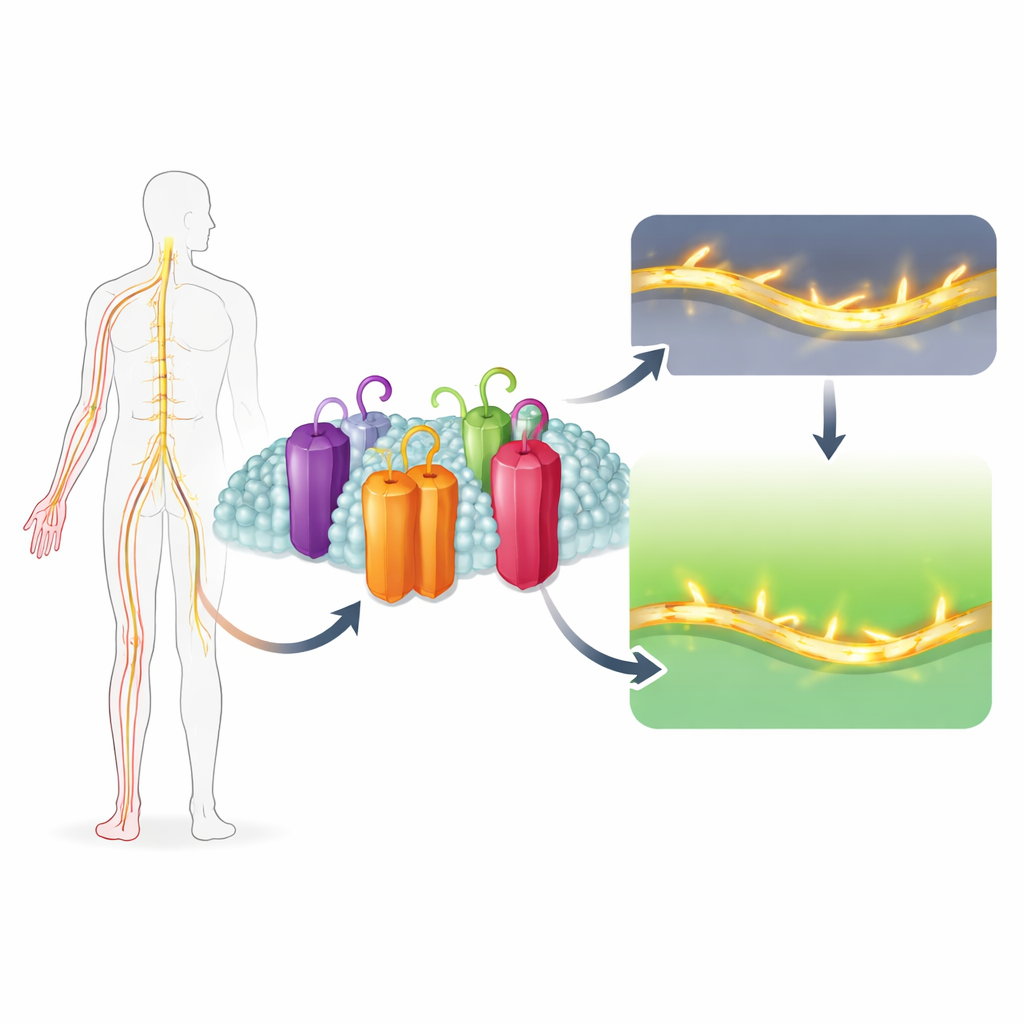
En speciell portvakt för smärta
Våra nerver avfyrar elektriska impulser med hjälp av natriumkanaler, mikroskopiska porer som tillfälligt öppnas för att låta positivt laddade natriumjoner strömma in i cellen. Det finns nio huvudvarianter av dessa kanaler hos människor, var och en anpassad till olika vävnader såsom hjärna, muskel, hjärta eller smärtsensoriska nerver. Nav1.7 är varianten som finns i perifera smärtfibrer. Den är ovanlig eftersom den kan slå på och av vid lägre spänningar än sina släktingar, vilket gör att den reagerar även på mycket små spänningsförändringar. Det gör Nav1.7 till en kraftfull förstärkare av svaga, smärtutlösande signaler. Genetiska studier visar att överaktiv Nav1.7 orsakar svåra ärftliga smärttillstånd, medan helt icke-funktionell Nav1.7 gör att människor inte kan känna smärta alls.
Att hitta en smärtselektiv blockerare
Läkemedelsutvecklare har länge velat rikta in sig på Nav1.7 för att behandla kronisk smärta, men den liknar andra natriumkanaler som är avgörande för hjärtrytm och hjärnfunktion. De flesta experimentella läkemedel binder många kanaltyper, vilket ger biverkningar eller misslyckas i kliniska prövningar. Forskarna skannade över 1 500 naturliga föreningar med ett cellbaserat test som upptäcker förändringar i membranspänning. De identifierade en molekylfamilj från växten Uvaria grandiflora och fokuserade på en förening kallad Uvarigranol D (UGD). UGD dämpade natriumströmmar i flera kanaltyper, men tystade nästan helt Nav1.7 medan den bara blockerade andra natriumkanaler till ungefär hälften även vid höga doser. Det innebär att dess selektivitet inte kommer från starkare bindning, utan från en mycket starkare effekt när den väl bundit.
En atomstor förändring gör Nav1.7 unik
För att förstå varför UGD är så effektiv på Nav1.7 byggde teamet kirala kanaler som bytte delar mellan Nav1.7 och en närbesläktad hjärnkanal, Nav1.2. Det identifierade en liten region nära porens yttre mynning, mellan två strukturella segment kallade S5 och S6 i domän III, som nyckelbestämmande för UGD:s fulla blockerande kraft. Jämförelse av aminosyrasekvenser visade att Nav1.7 ensam har en treonin vid position 1398, medan alla andra mänskliga natriumkanaler har en större metionin där. När forskarna bytte Nav1.7:s treonin mot metionin kunde UGD inte längre helt stänga kanalen; att byta metionin mot treonin i Nav1.2 fick den kanalen att bete sig som Nav1.7. Denna enda substitution skiftade också när kanalerna öppnade och stängde sig med spänningen: treonin gjorde att kanalen öppnade och inaktiverade vid mer negativa spänningar och gjorde det snabbare, egenskaper som gynnar att Nav1.7 befinner sig i ett icke-vilande tillstånd även nära den normala vilospänningen i smärtceller.
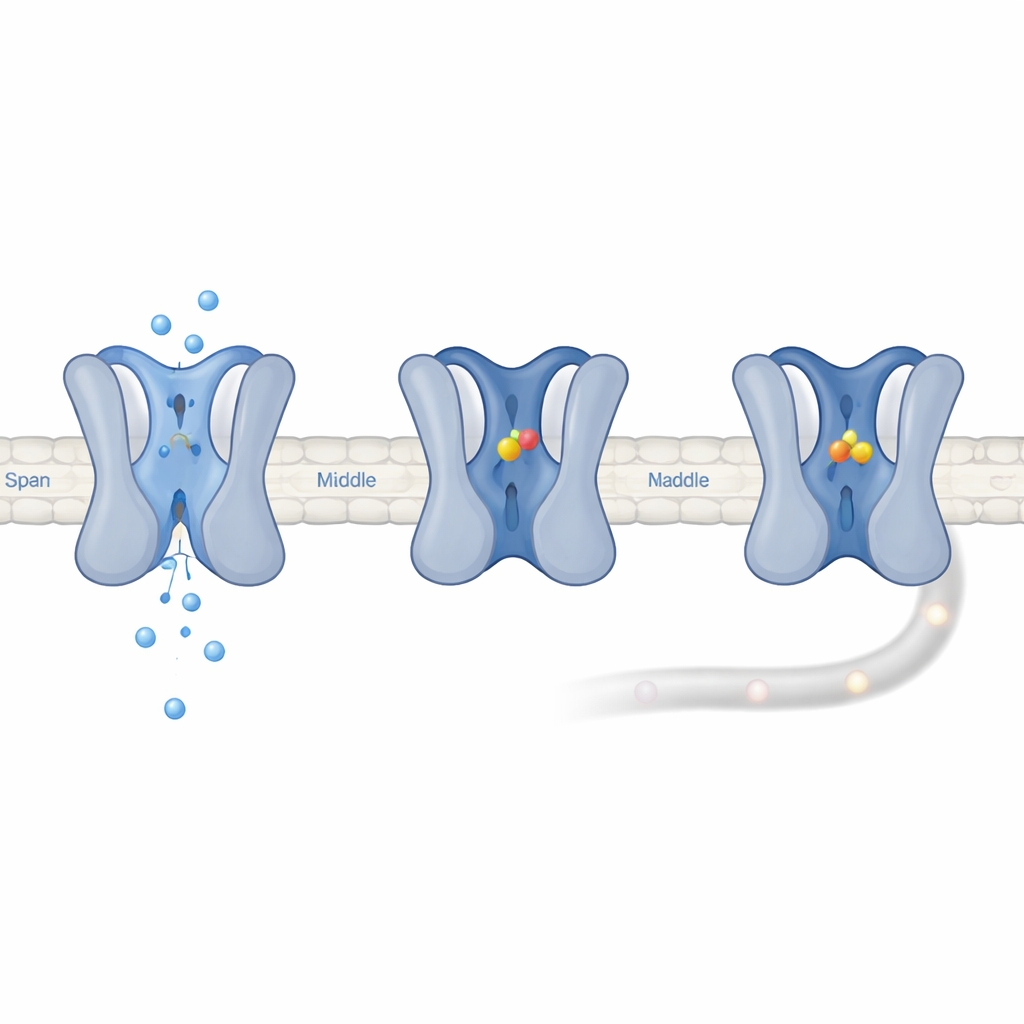
Låsa kanalen i ett viloläge
Elektriska inspelningar visade att UGD inte fäster vid Nav1.7 när den är stängd eller kortvarigt öppen. Istället föredrar den kanaler som gått in i ett långvarigt ”långsamt inaktiverat” tillstånd, där poren är stängd och tar hundratals millisekunder eller längre att återhämta sig från. När UGD var närvarande tog kanalerna ungefär tio gånger längre tid att ta sig ur detta tillstånd, vilket innebär att UGD stabiliserar det. Datorsimuleringar föreslog att UGD vilar i en ficka som bildas där en loop i domän III möter en helix i domän IV och gör viktiga kontakter med fem aminosyror. Mutation av någon av dessa rester försvagade UGD:s effekt, vilket bekräftar fickans betydelse. Eftersom Nav1.7:s treoninrika struktur gör att den går in i inaktiverade tillstånd vid lägre spänningar, befinner sig fler av dess kanaler i just det tillstånd som UGD föredrar att binda, vilket förklarar varför Nav1.7 fungerar som mycket mer undertryckt än sina släktingar även om bindningsstyrkan är liknande.
Från jonpore till smärtlindring
I slutändan är det som räknas hur dessa molekylära händelser påverkar verkliga celler. I råtters smärtsensoriska neuroner från dorsalrotsgangliet minskade UGD kraftigt antalet aktionspotentialer — de snabba spänningsspikarna som bär smärtinformation — och stoppade dem till slut helt vid låga mikromolära och submikromolära koncentrationer. I kontrast var humana hjärtliknande celler härledda från stamceller, som huvudsakligen använder en annan natriumkanal (Nav1.5) och vilar vid något lägre spänning, ungefär 60 gånger mindre känsliga. Detta tyder på att en ”effektselekteriv” blockerare som UGD kan dämpa smärtvägar långt mer än kardiella eller andra exciterbara vävnader helt enkelt på grund av hur ofta Nav1.7 befinner sig i sitt inaktiverade, läkemedelsgynnade tillstånd.
Vad detta betyder för framtida smärtbehandlingar
Studien visar att en liten strukturell detalj — en enda treonin — ligger bakom Nav1.7:s speciella låga spänningsbeteende och dess förmåga att generera ”tröskelströmmar”, de små signalerna som avgör om en smärtnerv ska avfyra. Genom att binda och stabilisera den inaktiverade formen av denna kanal utnyttjar UGD den inneboende tendensen och undertrycker Nav1.7 mycket starkare än andra natriumkanaler. För en lekman är slutsatsen att författarna har kartlagt en exakt svag punkt i kroppens smärtportvakt och visat ett sätt att trycka på den utan att i hög grad störa hjärt- eller hjärnkanaler. Denna insikt öppnar en väg för att designa nya smärtstillande medel som tystar överaktiva smärtnervceller genom att rikta in sig på spänningsbeteende och kanalens tillstånd, snarare än att bara jaga tajtare bindning till Nav1.7.
Citering: Zhao, F., Xi, C., Li, J. et al. Molecular determinant of low-voltage dependence of human Nav1.7 inactivation revealed by efficacy-based Nav1.7 selective inhibitor. Nat Commun 17, 2559 (2026). https://doi.org/10.1038/s41467-026-69184-8
Nyckelord: Nav1.7 natriumkanal, kronisk smärta, Uvarigranol D, tillståndsberoende hämning, spänningskänsliga natriumkanaler