Clear Sky Science · sv
Den redoxdrivna Na+-pumpande mekanismen i Vibrio cholerae NADH-quinone oxido-reduktas förlitar sig på dynamiska konformationsändringar
Hur kolerans kraftverk blev ett läkemedelsmål
Bakterien som orsakar kolera, Vibrio cholerae, överlever och förökar sig genom att driva ett litet molekylärt kraftverk i sitt cellmembran. Denna studie avslöjar, i enastående detalj, hur en av dess viktiga motorer—ett enzym kallat Na⁺-NQR—ändrar form medan det pumpar natriumjoner ut ur cellen. Att förstå denna molekylära maskineri tillfredsställer inte bara grundläggande nyfikenhet om hur livet omvandlar näring till användbar energi, utan pekar också på nya sätt att designa antibiotika som stänger ner skadliga bakterier utan att påverka humana celler.
En natriumdriven motor i bakterier
Många marina och sjukdomsframkallande bakterier förlitar sig på Na⁺-NQR som det första steget i sin respirationskedja, serien av reaktioner som utvinner energi ur näringsämnen. Na⁺-NQR sitter i det inre membranet och tar elektroner från ett bränslemolekyl som heter NADH, och för dem vidare längs en kedja av färgade ”hjälpmolekyler” (kallade kofaktorer) till kinon, en annan liten molekyl inbäddad i membranet. När elektroner flödar använder enzymet den energin för att pressa natriumjoner (Na⁺) från cellens insida till utsidan och skapar en natriumgradient. Denna gradient är som ett laddat batteri: den driver bakteriernas flagellmotor för rörelse, hjälper till att bilda ATP (cellens energivaluta) och driver upptag av näringsämnen samt utsöndring av läkemedel. Eftersom Na⁺-NQR endast finns i bakterier och skiljer sig mycket från det besläktade enzymet i våra mitokondrier är det ett attraktivt mål för högselektiva antibiotika.
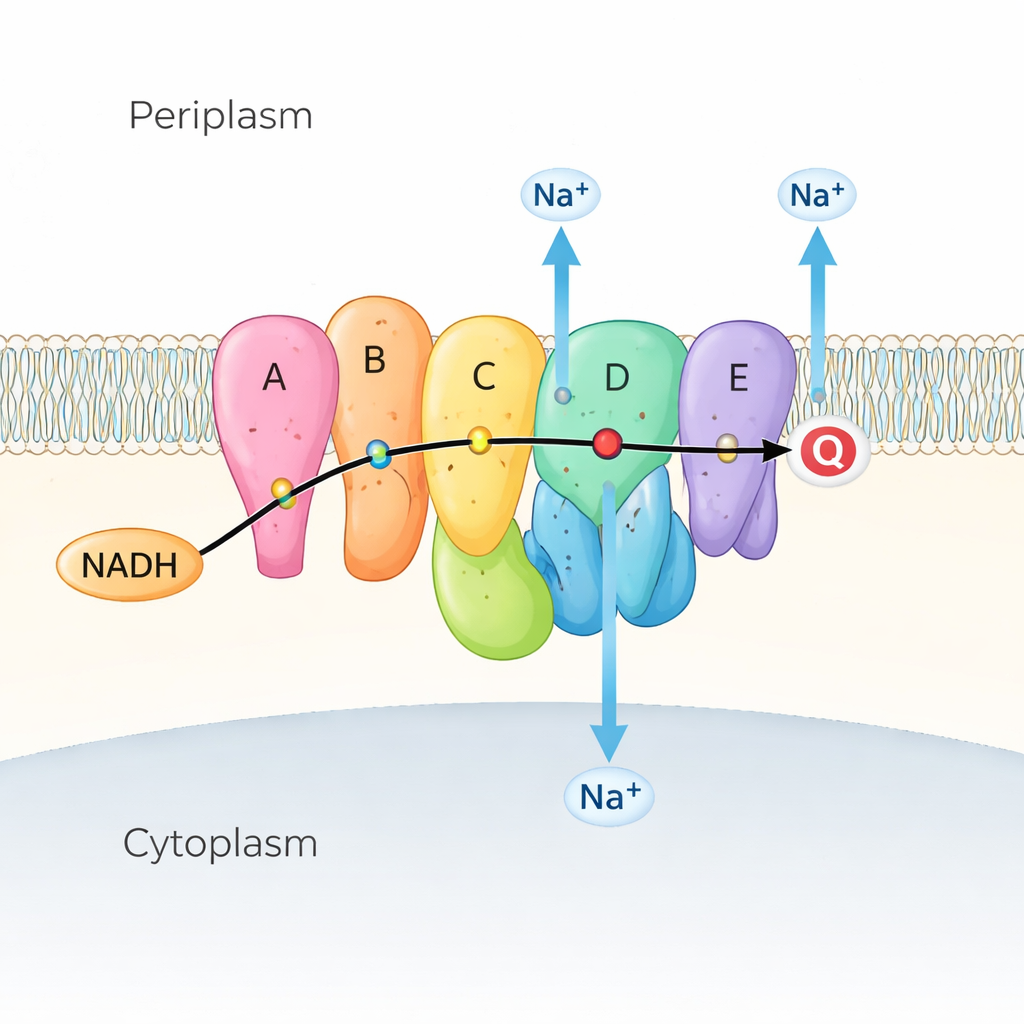
Att se maskinen röra sig
Tidigare röntgen- och kryoelektronmikroskopibilder visade var Na⁺-NQR:s subenheter och kofaktorer sitter, men avslöjade också en gåta: vissa kritiska elektronhopp var för långt isär för att elektroner effektivt skulle kunna förflytta sig om inte proteinet ändrade form. Författarna angriper detta genom att fånga Na⁺-NQR i många något olika tillstånd. De använde mutanter som tar bort specifika kofaktorer, läkemedel som stannar reaktionen i särskilda steg, och lösningar med och utan natrium. Med högupplöst kryo-EM och avancerad bildanalys kunde de separera och rekonstruera flera konformationer av samma enzym, vilket i praktiken förvandlade statiska ögonblicksbilder till en film av dess arbetscykel.
En flexibel arm och en förflyttande klämma
Ett centralt fynd rör en flexibel cytoplasmisk subenhet, NqrF, som bär två elektronbärande kofaktorer. Teamet identifierade tre positioner för dess ”ferredoxinliknande” domän—kallade ”upp”, ”mitten” och ”ner”. I det sällsynta men avgörande ”ner”-tillståndet svänger denna lilla domän in i en ficka bildad av två membransubenheter, NqrD och NqrE, och för järn–svavel-klustret tillräckligt nära för att överföra en elektron vidare. Samtidigt beter sig en periplasmisk (yttre) subenhet kallad NqrC som en rörlig klämma. I en konformation (”stabil”) ligger den intill en annan membransubenhet, NqrB, i position för att föra elektroner mot den slutliga kinonacceptorn. I en annan (”förskjuten”) konformation rör sig NqrC mot NqrD/E och för sitt flavinkofaktor närmare för att ta emot en elektron från deras järn–svavelcentrum. Dessa rörelser visar att NqrF och NqrC fungerar som dynamiska budbärare som överbryggar stora luckor i kofaktor kedjan.
Hur formförändringar pumpar natrium
Hjärtat i natriumpumpen ligger i de parvisa subenheterna NqrD och NqrE, som bildar en central bunt av membranöverskridande helixar. Genom att kombinera strukturer och atomnivå molekylär dynamiksimuleringar visar författarna att när järn–svavelklustret i NqrD/E reduceras (tar upp en elektron) skapas en negativt laddad plats som attraherar en Na⁺-jon och några vattenmolekyler från cytoplasmasidan och bildar en övergående bindningsficka. Hydrofoba aminosyror ovanför och nedanför denna ficka fungerar som inre och yttre grindar som styr åtkomsten till jonen. När NqrD/E växlar från en ”inåtöppen” till en ”utåtöppen” form rör sig Na⁺ mot periplasmasidan och släpps så småningom ut när järn–svavelklustret reoxideras. Simuleringarna visar att Na⁺ förblir delvis hydrerad men aldrig ser en kontinuerlig vattenfylld tunnel, vilket tyder på att enzymet är tätt förseglat mot oönskade protonläckor.
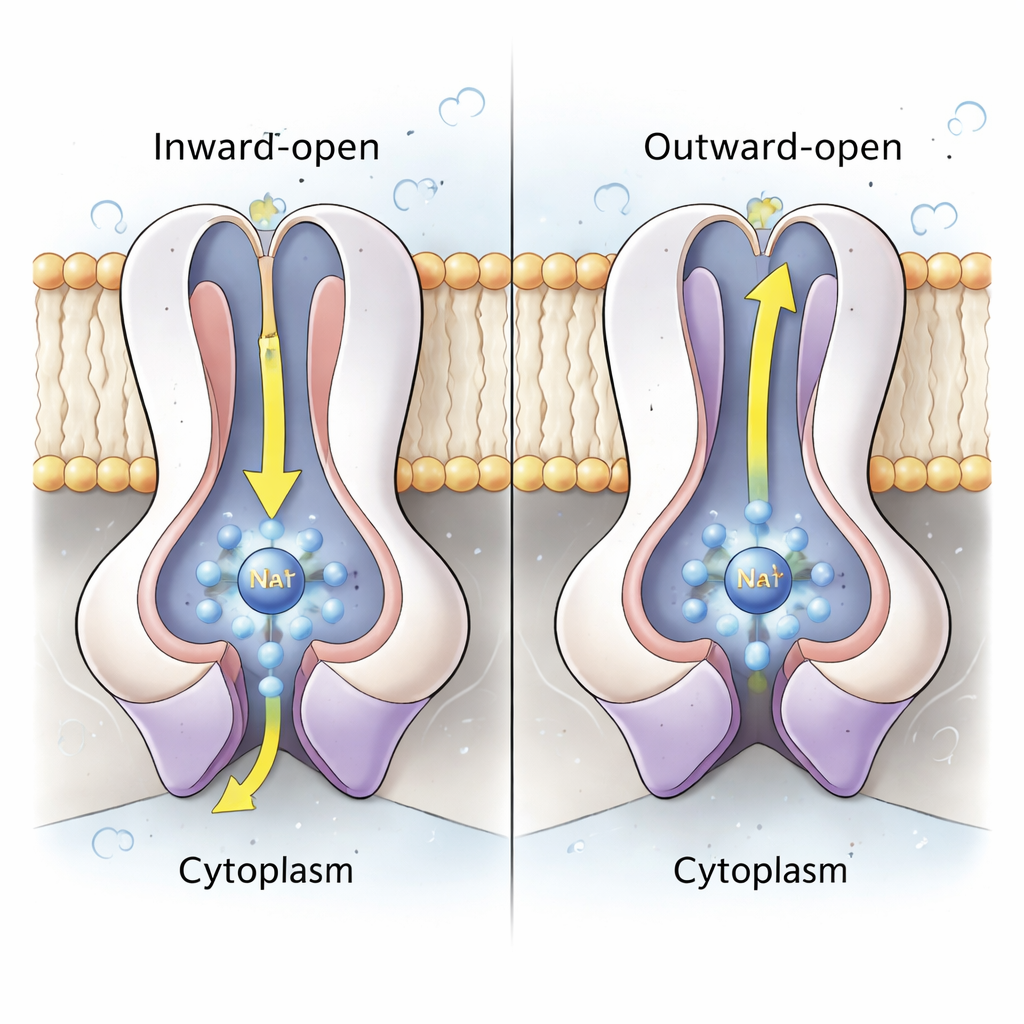
En koordinerad cykel som låser riktningen
Genom att kombinera alla sina strukturella tillstånd och simuleringar föreslår forskarna en sexstegs-cykel. NADH binder först och donerar elektroner till NqrF, som sedan överför en elektron till NqrD/E och utlöser Na⁺-upptag från cytoplasman och laddning av den centrala fickan. Den resulterande konformationsväxlingen av NqrD/E till den utåt-öppna formen både driver ut Na⁺ till periplasman och uppmuntrar NqrC att röra sig in i position för att ta emot elektronen. Efterföljande steg för elektroner vidare till de slutliga flavin- och riboflavinkofaktorerna och slutligen till kinon, som måste ta emot två elektroner för att bli kinol. Viktigt är att samma formförändringar som flyttar Na⁺ också alternerar mellan att lossa och stelna NqrF och NqrC, vilket gör framåtriktat elektronflöde sannolikt endast när Na⁺ pumpas utåt och motverkar bakåtglidning. Denna koppling hjälper enzymet att pumpa Na⁺ mot en redan existerande gradient och håller bakteriernas ”batteri” laddat.
Varför detta är viktigt för medicin och biologi
För en icke-specialist visar detta arbete hur livet bygger utsökt koreograferade maskiner av proteiner, där små förändringar i laddning utlöser stora, användbara rörelser. För forskning om infektionssjukdomar klargör det att Na⁺-translokation i Na⁺-NQR sker huvudsakligen genom NqrD/E-kärnan, inte genom den tidigare misstänkta NqrB-subenheten. Den insikten preciserar var framtida läkemedel bäst bör binda för att störa motorn som driver Vibrio cholerae och andra patogener samtidigt som humana enzymer skonas. Mer generellt ger studien en strukturell ritning för hur redoxreaktioner kan kopplas till jonpumpning—en designprincip som naturen återanvänder i många former av bioenergetiskt maskineri.
Citering: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Nyckelord: natriumpump, bakteriell respiration, Na+-NQR, cryo-EM, antibiotiska mål